Vinylacetat
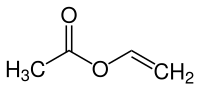
Vinylacetat (nach IUPAC-Nomenklatur: Ethenylacetat, systematisch auch als Ethenylethanoat bezeichnet) ist eine organisch-chemische Verbindung aus der Stoffgruppe der Carbonsäureester. Er liegt in Form einer farblosen Flüssigkeit mit süßlichem Geruch vor. Vinylacetat ist lichtempfindlich, es neigt dann dazu, spontan zu polymerisieren.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Vinylacetat | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Summenformel | C4H6O2 | |||||||||||||||
| Kurzbeschreibung |
farblose, lichtempfindliche, leichtentzündliche Flüssigkeit mit süßlichem Geruch[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 86,09 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
0,93 g·cm−3[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
72 °C[2] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
| |||||||||||||||
| Brechungsindex |
1,3956[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK | ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−349,2 kJ·mol−1[7] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Geschichte
Das monomere Vinylacetat wurde erstmals 1912 von Fritz Klatte bei Griesheim-Elektron dargestellt, indem er Acetylen in Gegenwart von Quecksilbersalz-Katalysatoren an Essigsäure addierte.[8]
Gewinnung und Darstellung
Die großtechnische Synthese von Vinylacetat erfolgt durch die selektive Gasphasenoxidation von Essigsäure mit Ethen in Gegenwart von Sauerstoff. Die Reaktion läuft dabei in dampfbeheizten Rohrbündelreaktoren bei Temperaturen von 150–160 °C und Drücken von 8–11 bar ab. Als Katalysatoren werden bimetallische Palladium-Gold-Schalenkatalysatoren eingesetzt.[9]
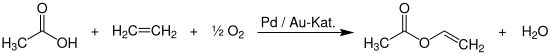
Die Selektivität bezüglich Vinylacetat beträgt 92 %, die Raum-Zeit-Ausbeute liegt bei ungefähr 900 g/l in der Stunde.[9]
Die Jahresnachfrage nach Vinylacetat beträgt in den Vereinigten Staaten ungefähr 1,14 Mio. Tonnen (Stand 2005).[6]
Eigenschaften
Physikalische Eigenschaften
Vinylacetat hat eine Viskosität von 0,43 mPa · s bei 20 °C, eine spezifische Wärmekapazität von 1,926 kJ/(kg · K) bei 20 °C, eine spezifische Verdampfungsenthalpie von 379,3 kJ/kg, eine Polymerisationswärme von 1035,8 kJ/kg (bei 76,8 °C), eine Verbrennungswärme 2082,9 kJ/mol bei 25 °C.[3] Die Dämpfe von Vinylacetat sind dreimal so schwer wie Luft. Mit Wasser bildet Vinylacetat ein Azeotrop, welches unter Normaldruck bei 66 °C siedet und 92,7 % Vinylacetat enthält.[3]
Chemische Eigenschaften
Vinylacetat polymerisiert sehr leicht unter dem Einfluss von verschiedenen Aktivatoren, z. B. Licht oder Peroxiden, sowie auch thermisch bei Erwärmung. Die Polymerisationswärme beträgt −88 kJ·mol−1 bzw. –1020 kJ·kg−1.[10] Als ein ungesättigter Ester sind eine Reihe von Additions- und Umesterungsreaktionen möglich.
Sicherheitstechnische Kenngrößen
Vinylacetat bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt bei −8 °C.[2][11] Der Explosionsbereich liegt zwischen 2,6 Vol.‑% (93 g/m³) als untere Explosionsgrenze (UEG) und 13,4 Vol.‑% (480 g/m³) als obere Explosionsgrenze (OEG).[2][11] Entsprechend der Dampfdruckfunktion ergibt sich ein unterer Explosionspunkt von −10 °C.[2] Die Grenzspaltweite wurde mit 0,93 mm bestimmt.[2] Es resultiert damit eine Zuordnung in die Explosionsgruppe IIA.[11] Die Zündtemperatur beträgt 385 °C.[2][11] Der Stoff fällt somit in die Temperaturklasse T2.
Verwendung
Vinylacetat ist ein Monomer und wird überwiegend zur Herstellung von Polyvinylacetat und in geringem Umfang Vinylacetat-Copolymeren (wie Ethylenvinylacetaten oder Ethylen-Vinylalkohol-Copolymeren) und Polyvinylalkohol verwendet. Diese Polymere finden in Form von flüssigen Dispersionen, Dispersionspulver, Festharzen und Lösungen ihre Anwendung, insbesondere als Bindemittel im Bau-, Farben- und Lacksektor und als Rohstoff für die Klebstoff-, Papier- und Textilindustrie.[12]
Sicherheitshinweise / Risikobewertung
Vinylacetat ist als krebserzeugend nach EG-Kategorie 3 (Stoffe, die wegen möglicher krebserzeugender Wirkung beim Menschen Anlass zur Besorgnis geben) eingestuft. An der Luft kann Vinylacetat leicht explosive Peroxide bilden, was durch Zugabe von Stabilisatoren (z. B. Hydrochinon oder Methylhydrochinon in einer Konzentration von 3 bis 20 ppm) unterdrückt wird.
Vinylacetat wurde 2016 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Hierbei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von Vinylacetat waren die Besorgnisse bezüglich Verbraucherverwendung, hoher (aggregierter) Tonnage und weit verbreiteter Verwendung sowie der möglichen Gefahren durch reproduktionstoxische und sensibilisierende Eigenschaften sowie als potentieller endokriner Disruptor. Die Neubewertung läuft seit 2019 und wird von Lettland durchgeführt.[13]
Weblinks
- Vinyl Acetate Council: Leitfaden zum sicheren Umgang mit Vinylacetat, April 2010 (pdf)
Einzelnachweise
- Eintrag zu VINYL ACETATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 28. Dezember 2020.
- Eintrag zu Vinylacetat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Juni 2018. (JavaScript erforderlich)
- Datenblatt bei Celanese Chemicals.
- Eintrag zu Vinyl acetate im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 108-05-4 bzw. Vinylacetat), abgerufen am 30. September 2019.
- Leitfaden zur sicheren Handhabung von Vinylacetat. (PDF; 956 kB) Vinyl Acetate Council, April 2010, S. 7, abgerufen am 29. Dezember 2017 (englisch).
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-25.
- Frank Bienewald, Edgar Leibold, Pavel Tužina, Günter Roscher: Vinyl Esters. In: Ullmann’s Encyclopedia of Industrial Chemistry. Wiley‐VCH Verlag GmbH & Co. KGaA., 13. September 2019, doi:10.1002/14356007.a27_419.pub2
- Eintrag zu Vinylacetat. In: Römpp Online. Georg Thieme Verlag, abgerufen am 26. Februar 2019..
- Berufsgenossenschaft Rohstoffe und chemische Industrie, Merkblatt R 008 Polyreaktionen und polymerisationsfähige Systeme, Ausgabe 05/2015, ISBN 978-3-86825-069-5.
- E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen – Band 1: Brennbare Flüssigkeiten und Gase, Wirtschaftsverlag NW – Verlag für neue Wissenschaft GmbH, Bremerhaven 2003.
- M. D. Lechner, K. Gehrke und E. H. Nordmeier: Makromolekulare Chemie, 4. Auflage, Birkhäuser Verlag, 2010, ISBN 978-3-7643-8890-4, S. 53, S. 58 u. S. 63.
- Community rolling action plan (CoRAP) der Europäischen Chemikalienagentur (ECHA): Vinyl acetate, abgerufen am 26. März 2019.


