Pitavastatin
Pitavastatin ist der Internationale Freiname (INN) für einen Arzneistoff aus der Gruppe der Statine, der zur Senkung erhöhter Gesamt-Cholesterin- und LDL-Cholesterin-Spiegel eingesetzt wird.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
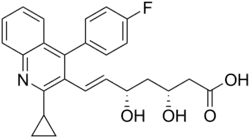 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Pitavastatin | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C25H24FNO4 | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
C10AA08 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 421,46 g·mol−1 | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Als Fertigarzneimittel wurde Pitavastatin im August 2009 in den USA und 2011 in Deutschland zugelassen.[2] Entwickelt wurde es von der japanischen Firma Kōwa Sōyaku (Kowa Pharmaceutical), in den EU-Ländern soll das Medikament von der Firma Recordati vermarktet werden.[3][4][3]
Klinische Angaben
Anwendungsgebiete (Indikationen)
Die Anwendung von Pitavastatin ist angezeigt zur Senkung erhöhter Gesamtcholesterin- und LDL-Cholesterin-Spiegel bei Patienten mit primärer Hypercholesterinämie oder kombinierter Hypercholesterinämie und Hypertriglyceridämie bei Patienten mit erhöhtem kardiovaskulärem Risiko.[5]
Gegenanzeigen (Kontraindikationen)
Die Anwendung von Pitavastatin ist kontraindiziert bei:
- Patienten mit einer bekannten Überempfindlichkeit gegen den Wirkstoff. Überempfindlichkeitsreaktionen – einschließlich Hautausschlag, Juckreiz (Pruritus) und Nesselsucht (Urtikaria) – wurden bei den klinischen Prüfungen beobachtet.
- Patienten mit aktiven Lebererkrankungen, die sich zum Beispiel durch ungeklärten und dauerhaften Anstieg der Aspartat-Aminotransferase (Leber-Transaminasen) äußern können.
- Die gleichzeitige Verabreichung von Ciclosporin-haltigen Medikamenten ist ebenfalls kontraindiziert.[5]
Pharmakokinetische Eigenschaften
Die Bioverfügbarkeit von Pitavastatin beträgt 80 %; Die Plasmaproteinbindung des Wirkstoffs beträgt 96 %. Pitavastatin wird hauptsächlich durch das Cytochrom P450-Isoenzym CYP2C9 metabolisiert.[6] Die Elimination aus dem Blut erfolgt mit einer terminalen Halbwertszeit#Biologische Halbwertszeit von 11 Stunden.
Sonstige Informationen
Chemische und pharmazeutische Informationen
Im Fertigarzneimittel wird Pitavastatin-Hemicalcium (Pitavastatin·Calcium (2:1)), CAS-Nummer 147526-32-7 mit folgenden chemisch-physikalischen Eigenschaften verwendet: Der Name nach IUPAC-Nomenklatur lautet: Calcium-(3R,5S,6E)-7-[2-cyclopropyl-4-(4-fluorphenyl)-3-chinolyl]-3,5-dihydroxyhept-6-enoat, die Summenformel ist C50H46CaF2N2O8 mit einer molaren Masse von 880,98 g·mol−1. Pitavastatin-Hemicalcium ist ein geruchloses, weißes bis blassgelbes, lichtempfindliches und hygroskopisches Pulver. Es ist leicht löslich in Pyridin, Chloroform, verdünnter Salzsäure und Tetrahydrofuran, löslich in Ethylenglycol, schwer löslich in Octanol, leicht löslich in Methanol, sehr schwer löslich in Wasser oder Ethanol, praktisch unlöslich in Acetonitril oder Diethylether. Der Schmelzpunkt beträgt 190–192 °C.[5]
Erste Entscheidung zu früher Nutzenbewertung
Im Rahmen der frühen Nutzenbewertung von Arzneimitteln hat der Gemeinsame Bundesausschuss (G-BA) ... die erste Entscheidung getroffen. Arzneimittel mit dem neuen Wirkstoff „Pitavastatin“ werden in das Festbetragssystem überführt, da für diese Präparate eine therapeutische Verbesserung als nicht belegt gilt.[7]
Weblinks
Einzelnachweise
- Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von {[(3R,5S,6E)-7-[2-cyclopropyl-4-(4-fluorophenyl)quinolin-3-yl]-3,5-dihydroxyhept-6-enoyl]oxy}calcio (3R,5S,6E)-7-[2-cyclopropyl-4-(4-fluorophenyl)quinolin-3-yl]-3,5-dihydroxyhept-6-enoate im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 6. Juli 2020.
- FDA Approves New Cholesterol-Lowering Drug. 3. August 2009. Abgerufen am 4. September 2009.
- Kowa Pharmaceutical Europe Co., Ltd.: Livazo(R) (pitavastatin), ein neues wirksames Statin mit positiver Wirkung auf mit Herzkrankheiten assoziierte Lipidfraktionen wird in Spanien eingeführt (Memento vom 14. April 2014 im Internet Archive)
- DAZ: Neuer Cholesterinsenker Pitavastatin. 2. August 2010. Abgerufen am 19. August 2011.
- FDA Label für LIVALO (Pitavastatin) (en, PDF, 241 kB) auf der Webseite der Food and Drug Administration FDA. S. 15. 3. August 2009. Abgerufen am 4. September 2009.
- Kajinami K, Mabuchi H, Saito Y: NK-104: a novel synthetic HMG-CoA reductase inhibitor. In: Expert Opin Investig Drugs. 9, Nr. 11, 2000, S. 2653–2661. doi:10.1517/13543784.9.11.2653. PMID 11060827.
- G-BA: Erste Entscheidung zu früher Nutzenbewertung – Verfahren stabil etabliert. 18. August 2011. Abgerufen am 26. Februar 2014.