Bromierung
Die Bromierung ist ein Spezialfall der Halogenierung und bezeichnet eine chemische Reaktion zur Einführung eines oder mehrerer Bromatome in eine organische Verbindung. Dabei kann es sich um eine Additions- oder eine Substitutionsreaktion handeln. Der Reaktionsmechanismus kann ionisch bzw. radikalisch verlaufen.

Als Substrate für eine Bromierung sind zahlreiche Verbindungen möglich:
- Alkane (radikalische Substitution)
- Alkene (ionische elektrophile Addition sowie Bromierung in Allylstellung)
- Alkine (ionische elektrophile Addition)
- Aromaten (ionische elektrophile Substitution sowie Bromierung in Benzylstellung)
In der chemischen Industrie wird häufig alternativ die Chlorierung durchgeführt, da Chlor billiger ist und eine geringere Molmasse hat. Im Labor hingegen wird in der Regel die Bromierung bevorzugt, da Brom zum einen leichter handhabbar ist (bei Raumtemperatur flüssig) und zum anderen durch seine geringere Reaktivität eine größere Selektivität besitzt.
Bromierung von Alkanen
Die radikalische Substitution ist eine schwierig zu kontrollierende Reaktion und erzeugt in der Regel alle möglichen Produkte und Isomere. Sie ist daher für die organische Synthese nur in Ausnahmefällen geeignet.[1]
Bromierung von Alkenen/Alkinen
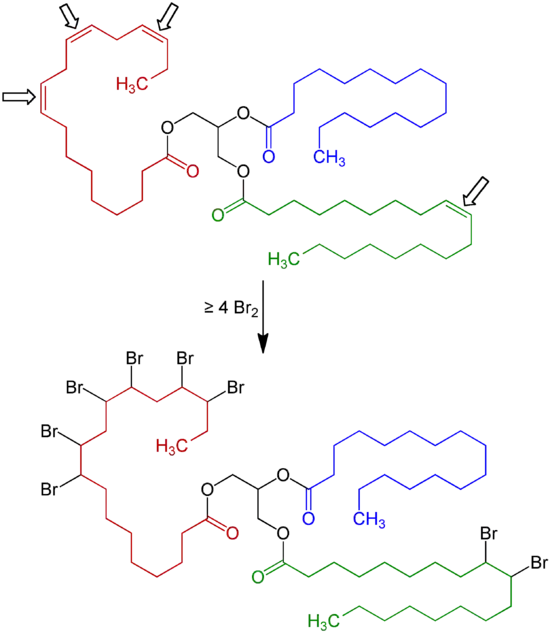
Die elektrophile Bromierung von Alkenen/Alkinen erfolgt an der Doppel-/Dreifachbindung und kann auch mit komplizierten Substraten mit mehreren funktionellen Gruppen durchgeführt werden. Die Addition von Brom an Alkenen/Alkinen verläuft mit hoher Atomökonomie.
Bromierung von Aromaten
Aromaten können in Abhängigkeit von den Reaktionsbedingungen entweder am Kern oder in der (aliphatischen) Seitenkette bromiert werden.
Die Bromierung am Kern ist ein Beispiel für die elektrophile Substitution.
Eine Substitution an der Seitenkette findet bevorzugt in benzylischer Position statt (d. h. in direkter Nachbarschaft zum Ring), da benzylische Radikale durch den aromatischen Ring stabilisiert werden.
Bei UV-Strahlung und/oder hohen Temperaturen erfolgt die Bromierung in der Seitenkette {SSS-Regel: Sonne (UV-Strahlung), Siedehitze (hohe Temperatur), Seitenkette}.
Bei Zusatz eines Katalysators (meist eine Lewissäure beispielsweise FeBr3) und niedrigen Temperaturen erfolgt Kernsubstitution (KKK-Regel: Katalysator, Kälte, Kernsubstitution).
Bromierung in Allyl- oder Benzylstellung
Als eine Besonderheit gilt die Einführung eines Bromatoms in allylischer oder benzylischer Position. Die Bromierung an dieser Stelle wird auch als Wohl-Ziegler-Reaktion bezeichnet. Es handelt sich hierbei um eine radikalische Substitution, bei der als Reagens NBS (N-Bromsuccinimid) eingesetzt wird, um die Bromkonzentration klein zu halten und eine elektrophile Addition an die Doppelbindung oder den Aromaten so zu unterdrücken.
Einzelnachweise
- Ivan Ernest: Bindung, Struktur und Reaktionsmechanismen in der organischen Chemie, Springer-Verlag, 1972, S. 297–306, ISBN 3-211-81060-9.