Ependymom
Ependymome sind meist langsam wachsende Tumoren des zentralen Nervensystems, die morphologisch Ähnlichkeiten mit den die Hirnhöhlen und den Rückenmarkskanal auskleidenden Ependymzellen haben. Zwei Drittel der Ependymome sitzen infratentoriell am 4. Ventrikel, das übrige Drittel liegt supratentoriell und zumeist in der periventrikulären weißen Substanz. Obwohl sie bevorzugt im Kinder- und Jugendalter auftreten, können Ependymome in jedem Lebensalter vorkommen.[1]
| Klassifikation nach ICD-10 | |
|---|---|
| C71.7 | Hirnstamm, IV. Ventrikel, Infratentoriell o.n.A. |
| C72.0 | Rückenmark |
| ICD-10 online (WHO-Version 2019) | |
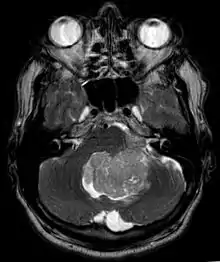
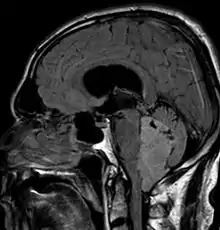
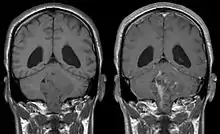
Symptome
Durch ihre Lokalisation in der Nähe der Ventrikel behindern Ependymome häufig den Fluss der Cerebrospinalflüssigkeit, was zu einer Erhöhung des Hirndrucks führen kann. Daraus können sich anhaltende Kopfschmerzen, Übelkeit und Erbrechen sowie ein Hydrozephalus ergeben.
Diagnose
In Kernspintomografie-Aufnahmen des Kopfes stellt sich das Ependymom typischerweise als umschriebene Läsion mit Bezug zum Ventrikelsystem dar, die ein heterogenes Signalmuster mit zystischen Anteilen aufweist sowie mäßig und girlandenartig Kontrastmittel anreichert. In 50 % sind in der Schnittbildgebung Verkalkungen zu erkennen. Zytologische Untersuchung der Cerebrospinalflüssigkeit sowie Tumorbiopsie können zur Diagnosefindung beitragen.
Pathologie
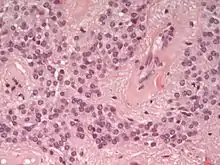
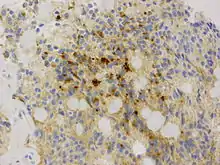
Ependymome werden nach der WHO-Klassifikation der Tumoren des zentralen Nervensystems dem Grad II zugeordnet, anaplastische Ependymome dem Grad III. Das namentlich verwandte Ependymoblastom gehört dagegen in die Gruppe der Primitiven Neuroektodermalen Tumoren (PNET), die nicht histogenetisch mit den Ependymomen verwandt sind. Eine Sonderform ist das überwiegend spinal (im Bereich des Filum terminale) lokalisierte sogenannte myxopapilläre Ependymom, das in der Regel eine günstigere Prognose hat (WHO-Grad I).[2]
Intraoperativ stellen sich Ependymome meist als gut abgrenzbare, weißliche Masse dar. Histologisch handelt es sich um gliale Tumoren mit ependymaler Differenzierung, das heißt, die Tumorzellen neigen wie die Ependymzellen dazu, Oberflächen zu bilden. Diagnostisch sind sogenannte ependymale Rosetten, in denen mehrere Tumorzellen ein zentrales Lumen bilden. Typisch sind auch perivaskuläre Pseudorosetten, in denen die um Blutgefäße gelagerten Tumorzellen feine fibrilläre Fortsätze auf diese hin ausrichten. Als gliale Tumoren exprimieren Ependymome (insbesondere im Bereich der perivaskulären Pseudorosetten) das saure Gliafaserprotein (GFAP). In der immunhistochemischen Färbung für das epitheliale Membran-Antigen (EMA) lassen sich darüber hinaus häufig intrazytoplasmatische Mikrolumina nachweisen.
In Einzelfällen können Ependymome auch ungewöhnliche histologische Eigenschaften wie Riesenzellen,[3] Zysten[4] oder Inseln mit neuronaler Differenzierung[5] aufweisen.
Therapie
Die Lokalisation direkt beim Hirnstamm erschwert eine Operation ungemein; sie ist jedoch die wirkungsvollste Therapie. Die Bedeutung der Strahlentherapie bei vollständig entfernten Ependymomen ist unklar, sicher scheint jedoch, dass Patienten, bei denen eine vollständige Resektion nicht erreicht werden konnte, von einer Strahlentherapie profitieren können. Außerhalb kontrollierter klinischer Studien kommt einer adjuvanten Chemotherapie normalerweise keine wesentliche Bedeutung zu. Allerdings kann bei kleinen Kindern durch eine Chemotherapie die in dieser Altersgruppe nebenwirkungsreiche Strahlentherapie möglicherweise hinausgeschoben werden. Aktuelle Daten sprechen für diese Annahme.[6] Insbesondere bei Kindern sollte eine Therapie im Rahmen klinischer Studien angestrebt werden.
Prognose
Da Ependymome aufgrund ihrer Lokalisation häufig nur inkomplett reseziert werden, ist das Ausmaß der Resektion von besonderer Bedeutung für die Prognose.[7][8][9][10] Die neuropathologische Klassifizierung, auch unter Einschluss einer zentralen neuropathologischen Begutachtungsstelle, hingegen wurde in der Untersuchung von Robertson und Mitarbeitern als nicht prognostisch relevant eingestuft.[7] Andere Untersuchungen kamen zu entgegengesetzten Ergebnissen mit prognostisch ungünstiger Bedeutung von Zelldichte (Zellularität), Mitosendichte (Mitosenanzahl pro Gesichtsfeld), endotheliale Proliferation und Differenzierungsgrad.[11] Je nach durchgeführter Untersuchung bzw. Studie können die histologischen Prognosefaktoren jedoch variieren.[9][12][13] Neben der Histologie bzw. neuropathologischen Klassifizierung spielt offensichtlich auch das Alter eine prognostische Rolle. Kinder im Alter von weniger als 3 Jahren tendieren zu einer schlechteren Prognose.[8]
Einzelnachweise
- Lord et al.: Fourth ventricle ependymoma in father and son. In: Br J Neurosurg, 2007;1-3. PMID 17952721
- Prayson & Suh: Subependymomas: clinicopathologic study of 14 tumors, including comparative MIB-1 immunohistochemical analysis with other ependymal neoplasms. In: Arch Pathol Lab Med, 1999;123(4):306-9. PMID 10320142
- Zec et al.: Giant cell ependymoma of the filum terminale. A report of two cases. In: Am J Surg Pathol, 1996;20(9):1091-101. PMID 8764746
- Arsene et al.: Highly cystic brain tumor: rare histological features in an ependymoma. In: Neuropathology, 2007;27(4):378-82. PMID 17899693
- Rodriguez et al.: Ependymomas with neuronal differentiation: a morphologic and immunohistochemical spectrum. In: Acta Neuropathol, 2007;113(3):313-24. PMID 17061076
- Grundy et al.: Primary postoperative chemotherapy without radiotherapy for intracranial ependymoma in children: the UKCCSG/SIOP prospective study. Lancet Oncol. 2007;8(8):696-705. PMID 17644039
- Robertson et al.: Survival and prognostic factors following radiation therapy and chemotherapy for ependymomas in children: a report of the Children's Cancer Group. In: J Neurosurg. 1998;88(4):695-703. PMID 9525716
- Agaoglu et al.: Ependymal tumors in childhood. In: Pediatr Blood Cancer. 2005;45(3):298-303. PMID 15770637
- Spagnoli et al.: Combined treatment of fourth ventricle ependymomas: report of 26 cases. In: Surgical Neurology. 2000;54(1):19-26. PMID 11024503
- Pollack IF, et al.: Intracranial ependymomas of childhood: long-term outcome and prognostic factors. In: Neurosurgery. 1995;37(4):655-66. PMID 8559293
- Figarella-Branger et al.: Prognostic factors in intracranial ependymomas in children. In: J Neurosurg. 2000;93(4):605-13. PMID 11014538
- Prayson: Clinicopathologic study of 61 patients with ependymoma including MIB-1 immunohistochemistry. In: Ann Diagn Pathol. 1999;3(1):11-8. PMID 9990108
- Kurt et al.: Identification of relevant prognostic histopathologic features in 69 intracranial ependymomas, excluding myxopapillary ependymomas and subependymomas. In: Cancer. 2006;106(2):388-95. PMID 16342252