Alkoholdehydrogenase
Alkoholdehydrogenasen (ADH) sind Enzyme, die sowohl die Reaktion von Alkoholen zu den entsprechenden Aldehyden oder Ketonen und auch die Rückreaktion dieser (Aldehyd zu Alkohol) katalysieren. Beispiele hierfür sind der letzte Schritt der Alkoholischen Gärung durch Hefe, bei der Acetaldehyd zu Ethanol umgewandelt wird, als auch die umgekehrte Variante (Ethanol zu Acetaldehyd), die im menschlichen Körper im Rahmen des Alkoholabbaus stattfindet. Es handelt sich in jedem Fall um Redoxreaktionen. Alkoholdehydrogenasen kommen in allen Lebewesen vor.
| Alkoholdehydrogenase | ||
|---|---|---|
| ||
| ADH1A | ||
| Sekundär- bis Quartärstruktur | Homodimer | |
| Kofaktor | Zn2+ | |
| Isoformen | 7 | |
| Enzymklassifikation | ||
| EC, Kategorie | 1.1.1.1, Oxidoreduktase | |
| Substrat | Alkohol + NAD+ | |
| Produkte | Carbonylverbindung + NADH + H+ | |
Die katalysierten Reaktionen
Es reagieren ausschließlich primäre und sekundäre Alkohole; tertiäre Alkohole reagieren nicht mit NAD+.
Primärer Alkohol
Ein primärer Alkohol reagiert mit NAD+ zu einem Aldehyd und NADH und umgekehrt (Gleichgewichtsreaktion):
Sekundärer Alkohol
Aus einem sekundären Alkohol und NAD+ entstehen Keton und NADH und umgekehrt (Gleichgewichtsreaktion):
ADH-Isoenzyme im Menschen
Im Humanstoffwechsel koexistieren mindestens fünf unterschiedliche Alkoholdehydrogenasen. Alle sind Dimere aus zwei Polypeptidketten, wobei jede Untereinheit zwei Zinkionen (Zn2+) enthält und zwischen 374 und 386 Aminosäuren lang ist. Eines dieser Ionen ist essenziell für die Funktion des Enzyms: Es ist am aktiven Zentrum lokalisiert und stabilisiert die Hydroxygruppe des Alkohols.
| Klasse | Mögliche Untereinheit | Eigenschaften | ||
|---|---|---|---|---|
| Gen-Name | UniProt | OMIM | ||
| I | ADH1A | P07327 | 103700 | Ethanol- und Methanoloxidation |
| ADH1B | P00325 | 103720 | ||
| ADH1C | P00326 | 103730 | ||
| II | ADH4 | P08319 | 103740 | 3,4-Dihydroxyphenylglycol- und 4-Hydroxy-3-methoxyphenylglycol-Biosynthese, sowie Benzaldehyd-Hydrogenierung (im Abbau von Adrenalin und Noradrenalin)[1] Retinol-Metabolismus[2] |
| III | ADH5 | P11766 | 103710 | Glutathion-abhängige Formaldehyd-Dehydrogenierung (EC 1.1.1.284)[3] |
| IV | ADH6 | P28332 | 103735 | Ethanoloxidation, Benzylalkohol[4] |
| V | ADH7 | P40394 | 103700 | Retinoloxidation, Ethanoloxidation (nur hohe Konzentrationen) |
Klasse-I ADH
Die Alkoholdehydrogenase 1 (ADH1) katalysiert den Abbau toxischer Alkohole im menschlichen Körper, sowie bei vielen Tierarten. Das im Magen und Leber vorhandene Enzym katalysiert hauptsächlich die Oxidation von Ethanol zu Acetaldehyd unter Beteiligung des Cofaktors NAD+:

Im menschlichen Körper wirkt ADH1 vor allem in der Leber, allerdings auch im Magen. Auf diese Weise wird beispielsweise in alkoholischen Getränken enthaltenes Ethanol zunächst zu Acetaldehyd, und schließlich durch das Enzym Aldehyddehydrogenase 2 (ALDH2) zu Essigsäure oxidiert. Diese wird dann im Citratzyklus zu Wasser und Kohlenstoffdioxid abgebaut. Für das Einschleusen in den Citratzyklus ist das Enzym Acetyl-CoA-Synthetase notwendig, welches unter ATP-Verbrauch Acetyl-CoA bildet.
Die Menge des ADH1-Enzyms im Körper ist von Person zu Person unterschiedlich und bestimmt, wie schnell der getrunkene Alkohol im Körper abgebaut wird. Wie viel Alkohol ein Mensch verträgt (im Sinne von „Trinkfestigkeit“) ist von vielen Faktoren abhängig, z. B. der Gewohnheit, mit einem hohen Alkoholgehalt umzugehen. Im Allgemeinen haben Ostasiaten, indigene Völker Amerikas und Aborigines Australiens eher geringe Mengen ADH im Körper, und Frauen weniger als Männer.[5][6]
Alkoholdehydrogenase 1 ist verantwortlich für die Toxizität anderer Alkohole: zum Beispiel oxidiert sie Methanol zu dem wesentlich giftigeren Produkt Methanal (Formaldehyd) sowie Ethylenglycol zu Glycolaldehyd und Glyoxalsäure. Die konventionelle Behandlung dieser Art von Vergiftungen besteht in der Applikation von Ethanol (kompetitive Hemmung von ADH1 durch Ethanol), der bevorzugt in der Leber umgesetzt wird. Solange der Ethanolabbau stattfindet, wird das Methanol durch die Nieren ausgeschieden. Somit tritt keine Vergiftung des Körpers durch das Methanal auf. Außerdem existiert mit Fomepizol (4-Methylpyrazol) die Möglichkeit ADH1 kompetitiv zu hemmen. Ein weiterer Inhibitor ist 2-Fluorethanol. Außerdem hemmen alle Rheumamittel/Schmerzmittel vom Typ der NSAR die ADH mehr oder minder stark.[7]
Funktionen
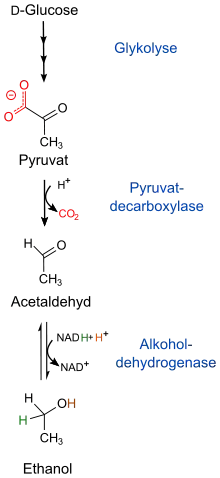
In Hefen und vielen Bakterien spielt die Alkoholdehydrogenase eine wichtige Rolle in der Gärung (vgl. Abbildung):
Pyruvat aus der Glykolyse wird in Acetaldehyd und Kohlenstoffdioxid umgesetzt, was eine Pyruvatdecarboxylase (EC 4.1.1.1) katalysiert. Anschließend wird der Aldehyd durch die ADH unter Verbrauch von NADH zu Ethanol reduziert. Auf diese Weise wird für die Glykolyse benötigtes NAD+ regeneriert. ADH aus Hefe ist größer als die menschliche und besteht aus vier Untereinheiten. Ihr aktives Zentrum besitzt Zink als Metallion. Dennoch sind die Enzyme aus Pilz und Mensch nahe verwandt.[8]
In Insekten wie der Fruchtfliege kommt eine der menschlichen nicht verwandte Alkoholdehydrogenase vor, an die kein Metallion gebunden ist.[9]
Eine dritte Klasse der Alkoholdehydrogenasen enthält Eisen als Zentralion. Diese existieren in Bakterien, und eine (anscheinend inaktive) Form wurde in Hefe gefunden.[10]
Literatur
- Chu-Fang Chou, Ching-Long Lai, Yen-Chun Chang, Gregg Duester, Shih-Jiun Yin: Kinetic mechanism of human class IV alcohol dehydrogenase functioning as retinol dehydrogenase. In: Journal of Biological Chemistry. Band 277, Nr. 28, Juli 2002, S. 25209–25216, doi:10.1074/jbc.M201947200, PMID 11997393.
- Roth, K.: Chemische Köstlichkeiten. 1. Auflage. Weinheim: Wiley-VCH, 2010, ISBN 978-3-527-32752-2, S. 206–215.
- Fuchs, G. (Hrsg.): Allgemeine Mikrobiologie. 9. Auflage. Stuttgart: Thieme, 2014, ISBN 978-3-13-444609-8, S. 262.
Weblinks
Einzelnachweise
- G. Mårdh, A. L. Dingley, D. S. Auld, B. L. Vallee: Human class II (pi) alcohol dehydrogenase has a redox-specific function in norepinephrine metabolism. In: Proceedings of the National Academy of Sciences of the United States of America. Band 83, Nr. 23, Dezember 1986, S. 8908–8912, doi:10.1073/pnas.83.23.8908, PMID 3466164, PMC 387042 (freier Volltext).
- Sílvia Martras, Rosana Alvarez, Oriol Gallego, Marta Domínguez, Angel R. de Lera, Jaume Farrés, Xavier Parés: Kinetics of human alcohol dehydrogenase with ring-oxidized retinoids: effect of Tween 80. In: Archives of Biochemistry and Biophysics. Band 430, Nr. 2, 15. Oktober 2004, S. 210–217, doi:10.1016/j.abb.2004.07.002, PMID 15369820.
- K. Engeland, J. O. Höög, B. Holmquist, M. Estonius, H. Jörnvall, B. L. Vallee: Mutation of Arg-115 of human class III alcohol dehydrogenase: a binding site required for formaldehyde dehydrogenase activity and fatty acid activation. In: Proceedings of the National Academy of Sciences of the United States of America. Band 90, Nr. 6, 15. März 1993, S. 2491–2494, doi:10.1073/pnas.90.6.2491, PMID 8460164, PMC 46113 (freier Volltext).
- C. S. Chen, A. Yoshida: Enzymatic properties of the protein encoded by newly cloned human alcohol dehydrogenase ADH6 gene. In: Biochemical and Biophysical Research Communications. Band 181, Nr. 2, 16. Dezember 1991, S. 743–747, doi:10.1016/0006-291x(91)91253-9, PMID 1755855.
- Alexander Parlesak, Michael Hans-Ulrich Billinger, Christiane Bode, Johann Christian Bode: Gastric alcohol dehydrogenase activity in man: influence of gender, age, alcohol consumption and smoking in a caucasian population. In: Alcohol and Alcoholism (Oxford, Oxfordshire). Band 37, Nr. 4, 2002, ISSN 0735-0414, S. 388–393, doi:10.1093/alcalc/37.4.388, PMID 12107043.
- K. Dohmen, E. Baraona, H. Ishibashi, G. Pozzato, M. Moretti, C. Matsunaga, K. Fujimoto, C. S. Lieber: Ethnic differences in gastric sigma-alcohol dehydrogenase activity and ethanol first-pass metabolism. In: Alcoholism, Clinical and Experimental Research. Band 20, Nr. 9, Dezember 1996, ISSN 0145-6008, S. 1569–1576, doi:10.1111/j.1530-0277.1996.tb01701.x, PMID 8986205.
- Marisa Battistella: Fomepizole as an antidote for ethylene glycol poisoning. In: The Annals of Pharmacotherapy. Band 36, Nr. 6, Juni 2002, S. 1085–1089, doi:10.1345/aph.1A397, PMID 12022913.
- Vladimir Leskovac, Svetlana Trivić, Draginja Pericin: The three zinc-containing alcohol dehydrogenases from baker’s yeast, Saccharomyces cerevisiae. In: FEMS yeast research. Band 2, Nr. 4, 2002, ISSN 1567-1356, S. 481–494, doi:10.1111/j.1567-1364.2002.tb00116.x, PMID 12702265.
- P. W. Heinstra, G. E. Thörig, W. Scharloo, W. Drenth, R. J. Nolte: Kinetics and thermodynamics of ethanol oxidation catalyzed by genetic variants of the alcohol dehydrogenase from Drosophila melanogaster and D. simulans. In: Biochimica et Biophysica Acta. Band 967, Nr. 2, 1988, S. 224–233, doi:10.1016/0304-4165(88)90013-x, PMID 3142528.
- Motoaki Yabe, Kazuyuki Shitara, Jun Kawashima, Hirofumi Shinoyama, Akikazu Ando, Takaaki Fujii: Purification and Properties of an Alcohol Dehydrogenase Isozyme from a Methanol-using Yeast, Candida sp. N-16. In: Bioscience, Biotechnology, and Biochemistry. Band 56, Nr. 2, 1992, S. 338–339, doi:10.1271/bbb.56.338.