Adenosin
Adenosin (A, Ado) ist ein Nukleosid und besteht aus der Nukleinbase Adenin und dem Zucker β-D-Ribose. Das Analogon mit Desoxyribose ist das Desoxyadenosin. Es ist Bestandteil der energiereichen Verbindungen ATP, ADP, AMP, der Ribonukleinsäure (RNA), verschiedenen Cofaktoren (z. B. Coenzym A, NADPH, NADH) und auch in einem Neuromodulator.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
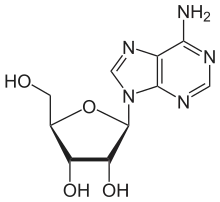 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Adenosin | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C10H13N5O4 | |||||||||||||||||||||
| Kurzbeschreibung |
weißer und geruchloser Feststoff[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
C01EB10 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 267,24 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Dichte |
0,31 g·cm−3[2] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Eigenschaften
Adenosin ist ein weißer und geruchloser Feststoff, der sich in Ethanol praktisch nicht löst, dagegen in heißem Wasser löslich ist.
Biologische Bedeutung
Adenosin ist Bestandteil der Ribonukleinsäure (RNA) und bildet dort mit Uridin, Dihydrouridin oder Pseudouridin ein Basenpaar.
Zudem hemmt Adenosin als körpereigener Botenstoff Entzündungsprozesse und kann somit vor Gewebeschäden schützen.[4]
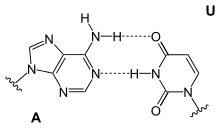 |
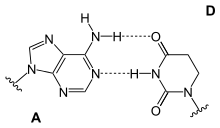 |
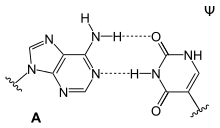 |
| A-U-Basenpaar | A-D-Basenpaar | A-Ψ-Basenpaar |
Pharmazeutische Bedeutung
Wirkung
Adenosin blockiert die Ausschüttung von allen belebenden und aktivierenden Neurotransmittern wie zum Beispiel Dopamin, Acetylcholin oder Noradrenalin. Dies bewirkt eine Dilatation (Weitung der Blutgefäße), wodurch der Blutdruck sinkt. Adenosin verringert außerdem die Herzfrequenz und verlängert die Überleitungszeit im AV-Knoten. Dies geschieht durch die Aktivierung eines Gi-modulierten Kaliumkanals über A1-Adenosinrezeptoren.
Adenosin triggert weiterhin den Nucleus praeopticus ventrolateralis im Hypothalamus, der die Weck- sowie Wachzentren des Gehirns durch den Neurotransmitter GABA hemmt, und wirkt damit schlafinduzierend.
Adenosin fällt als Abbauprodukt des energiereichen Adenosintriphosphats (ATP) an, das von den Körperzellen für die unterschiedlichen biologischen Prozesse verbraucht wird. Je höher dadurch die Adenosin-Konzentration steigt – je mehr Energie die Zellen also verbrauchen – desto mehr nimmt der Schlafdruck zu. Beim Schlafen wird Adenosin wieder ab- und ATP aufgebaut. Der Schlafdruck sinkt wieder. Dieser Kreislauf beginnt am Folgetag von neuem. Zusammen mit dem tageszeitabhängig freigesetzten Hormon Melatonin, dem körpereigenen Taktgeber, steuert Adenosin gemäß dem Schlafmodell von Borbély den Schlaf.[5][6]
Vermittelt werden die Adenosin-Effekte über Adenosinrezeptoren, insbesondere den Isoformen A1 und A2.
Die Xanthine Coffein, Theobromin und Theophyllin sowie der künstliche Arzneistoff Istradefyllin wirken als Antagonisten verschiedener Adenosinrezeptoren. Durch Hemmung der Rezeptoren im Nucleus praeopticus ventrolateralis ist auch deren schlafunterdrückender Effekt mitbegründet.[7][8]
Untersuchungen haben gezeigt, dass bestimmte Bestandteile des Baldrians, die so genannten Lignane, häufig auch als Schlaflignane bezeichnet, agonistisch an Adenosinrezeptoren wirken und dadurch beruhigende und schlaffördernde Effekte auslösen können.[9][10][11][12] Daher wird Baldrian bereits seit längerer Zeit in der Behandlung von Schlafstörungen eingesetzt.
Indikation
Adenosin ist zur Beendigung einer AV-Knoten-Reentrytachykardie indiziert. Es blockiert die Erregungsüberleitung vom Vorhof zum Ventrikel, wodurch ein einige Sekunden dauernder Herzstillstand ausgelöst wird. Die physiologische Halbwertszeit (HWZ) von Adenosin liegt im Bereich von Sekunden. Mit Theophyllin existiert ein Antidot.
Zur pharmakologischen Belastung bei der Myokardszintigrafie wird überwiegend Adenosin eingesetzt.
Handelspräparate
Adenoscan (D), Adrekar (D), Krenosin (CH), Generika (D, A)
ViaSpan Organkonservierungslösung (A), Vita-Gerin "Geistlich" (A)
Verwandte Verbindungen
Weblinks
Einzelnachweise
- Eintrag zu ADENOSINE in der CosIng-Datenbank der EU-Kommission, abgerufen am 26. März 2020.
- Datenblatt Adenosin (PDF) bei Carl Roth, abgerufen am 28. November 2013.
- Wissenschaft-Online-Lexika: Eintrag zu Adenosin im Lexikon der Chemie; abgerufen am 28. November 2013.
- B. N. Cronstein: Adenosine, an endogenous anti-inflammatory agent. In: J Appl Physiol. Band 76, 1994, S. 5–13.
- Alexander A. Borbély: A Two Process Model of Sleep Regulation. Human Neurobiol 1982; 1:195-204.
- Alexander A. Borbély et al.: The Two-Process Model of Sleep Regulation: A Reappraisal. J Sleep Res 2016; 25:131–143.
- C. Cajochen: Schlafregulation. In: Somnologie – Schlafforschung und Schlafmedizin, Volume 13, Nummer 2, Juni 2009, S. 64–71 (doi:10.1007/s11818-009-0423-7).
- Wolfgang Hauber: Adenosin: ein Purinnukleosid mit neuromodulatorischen Wirkungen. Neuroforum 3/02, S. 228–234 (PDF, 212 kB).
- Britta Schumacher et al.: Lignans isolated from valerian: Identification and characterization of a new olivil derivative with partial agonistic activity at A(1) adenosine receptors. J Nat Prod 2002; 65:1479-1485.
- Christa E. Müller et al.: Interactions of valerian extracts and a fixed valerian-hop extract combination with adenosine receptors. Life Sciences 2002; 71:1939-1949.
- E. A. Abourashed et al.: In vitro binding experiments with a Valerian, hops and their fixed combination extract (Ze91019) to selected central nervous system receptors. Phytomedicine 2004; 11:633–638.
- Cica Vissiennon et al.: Valerian Extract Ze 911 Inhibits Postsynaptic Potentials by Activation of Adenosine A1 Receptors in Rat Cortical Neurons. Planta Med 2006; 72:579-583.