Thiophenol
Thiophenol ist eine organische Schwefelverbindung, eine farblose giftige Flüssigkeit mit üblem Geruch. Es ist ein wichtiger Ausgangsstoff für die organische Synthese. Thiophenole sind eine Stoffgruppe von Verbindungen, die an einem Benzolring eine Thiolgruppe (–SH) aufweisen.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
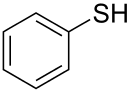 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Thiophenol | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C6H6S | ||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit unangenehmem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 110,18 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
1,08 g·cm−3 (20 °C)[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
169 °C[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| pKS-Wert |
6,62 (25 °C)[2] | ||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Brechungsindex |
1,5893 (20 °C)[4] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
Schweiz: 0,5 ml·m−3 bzw. 2,3 mg·m−3[5] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Gewinnung
Thiophenol kann unter anderem hergestellt werden durch:
- Reduktion von Benzolsulfonylchlorid mit Zink[6]
- Versetzen von Phenyl-Grignard-Verbindungen oder Phenyllithium mit Schwefel und anschließendes Ansäuern
Eigenschaften
Thiophenol hat die Formel C6H5–SH. Es liegt bei Raumtemperatur als mäßig flüchtige, aber extrem übelriechende und giftige Flüssigkeit vor. Thiophenole sind stärker sauer als Phenole, die entsprechenden Sauerstoffverbindungen.
Reaktionen
Mit Alkyliodiden ergeben sich Thioether[7] Oxidation erzeugt Diphenyldisulfid, das mit Natriumborhydrid wieder zu Thiophenol reduziert werden kann. Daher kann Thiophenol bei chemischen Reaktionen als Quelle für Wasserstoff dienen. Mit Chlor entsteht Phenylsulfenylchlorid.[8] Durch Reaktion von Thiophenol mit Alkalihydroxiden (Natriumhydroxid, Kaliumhydroxid) entstehen die entsprechenden Salze (Thiophenolate). Bei der Umsetzung mit Carbonsäurechloriden in Gegenwart von Basen wie Triethylamin entstehen Thiolester.[9]
Unfälle
In der Nacht auf den 16. Februar 2011 wurden aus Unachtsamkeit etwa 30 Liter Thiophenol auf dem Gelände einer Spedition im nordhessischen Homberg (Efze) freigesetzt. Etwa 180 Personen wurden mit den Dämpfen kontaminiert, 101 davon mussten ins Krankenhaus gebracht werden.[10][11]
Siehe auch
Thiophenol ist formal das Monomer von Polyphenylensulfid, das aber industriell nicht aus dem Monomer erzeugt wird.
Einzelnachweise
- Eintrag zu Thiophenol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 23. Juli 2016. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Dissociation Constants of Organic Acids and Bases, S. 8-45.
- Brockhaus ABC Chemie. VEB F. A. Brockhaus Verlag, Leipzig 1965, S. 1411.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-36.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 108-98-5 bzw. Thiophenol), abgerufen am 2. November 2015.
- R. Adams, C. S. Marvel: Thiophenol In: Organic Syntheses. 1, 1921, S. 71, doi:10.15227/orgsyn.001.0071; Coll. Vol. 1, 1941, S. 504 (PDF).
- O. Campopiano: Thiophenol. In: L. Paquette (Hrsg.): Encyclopedia of Reagents for Organic Synthesis J. Wiley & Sons, New York 2004.
- A. G. M. Barrett, D. Dhanak, G. G. Graboski, S. J. Taylor: (Phenylthio)nitromethane In: Organic Syntheses. 68, 1990, S. 8, doi:10.15227/orgsyn.068.0008; Coll. Vol. 8, 1993, S. 550 (PDF).
- Gerd Buchholz, Jürgen Martens, Klaus Praefcke: 2- und 4-Azathioxanthone durch Photoumlagerung von Thionicotinsäure-S-arylestern. In: Angewandte Chemie. Band 86, 1974, S. 562; Angewandte Chemie International Edition English. Band 13, 1974, S. 550.
- Großalarm und mehr als 30 Verletzte bei Giftunfall. In: faz.net, 16. Februar 2011. (faz.net)
- Gefahrgutunfall: Zahl der Verletzten steigt auf 101. auf: nh24.de. (Memento vom 19. Februar 2011 im Internet Archive), abgerufen am 17. Februar 2011.




