Stammzelle
Als Stammzellen werden allgemein Körperzellen bezeichnet, die sich in verschiedene Zelltypen oder Gewebe ausdifferenzieren können. Je nach Art der Stammzelle und ihrer Beeinflussung haben sie das Potenzial, sich in jegliches Gewebe (embryonale Stammzellen) oder in bestimmte festgelegte Gewebetypen (adulte Stammzellen) zu entwickeln.
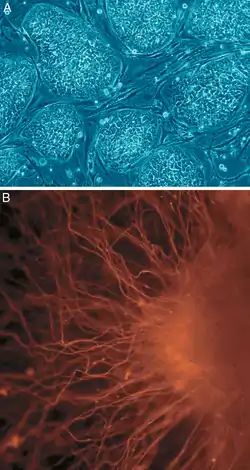
Stammzellen sind in der Lage, Tochterzellen zu generieren, die selbst wiederum Stammzelleigenschaften besitzen, aber auch solche mit größerer Ausdifferenzierung.[1] Hierzu befähigt sie ein noch nicht vollständig geklärter Mechanismus asymmetrischer Zellteilung. Über das jeweilige Schicksal der Zellen entscheidet dabei vor allem das biologische Milieu, in dem sie sich befinden.
Stammzellen werden vor allem durch ihr ontogenetisches Alter und ihr Differenzierungspotenzial unterschieden: die ontogenetisch frühesten Stammzellen sind die pluripotenten embryonalen Stammzellen, aus denen später die primitiven Keimstammzellen sowie die somatischen Stamm- und Progenitorzellen (oder Vorläuferzellen) hervorgehen. Phylogenetisch gehen die Stammzellen auf den letzten gemeinsamen eukaryotischen Vorfahren (LECA) zurück.[2]
Auch Pflanzen besitzen Stammzellen. Diese befinden sich an der Spitze des Sprosses im sogenannten Apikalmeristem sowie an den Wurzelspitzen im Wurzelmeristem. Im Gegensatz zu fast allen tierischen und menschlichen Zellen besitzen bei Pflanzen praktisch alle Zellen die Fähigkeit, einen kompletten Organismus zu regenerieren.
Embryonale Stammzellen
Embryonale Stammzellen (ES-Zellen) sind in vivo und in vitro in der Lage, sich in Zellen aller drei Keimblätter (Entoderm, Ektoderm und Mesoderm) sowie in Zellen der Keimbahn auszudifferenzieren. Sie werden daher als pluripotent bezeichnet. ES-Zellen werden für experimentelle Zwecke – nach Befruchtung der Eizelle im Embryo-Entwicklungsstadium der Blastozyste – aus der inneren Zellmasse (ICM; auch Embryoblast genannt) gewonnen.[3]
ES-Zellen wurden erstmals 1981 isoliert – aus Blastozysten der Maus. Sie neigen in vitro dazu, spontan zu differenzieren. Dies kann durch Faktoren unterbunden werden, welche die Selbsterneuerung der Zellen fördern. Mehrere solcher Stoffe wurden seit Ende der 1980er Jahre identifiziert, maßgeblich durch die Gruppe um Austin Smith in Edinburgh. ES-Zellen können daher im Prinzip unbegrenzt vermehrt werden, was unter anderem auch mit der hohen Aktivität des Enzyms Telomerase zusammenhängt. Damit unterscheiden sie sich von anderen (sogenannten primären) Körperzellen, die ihre Teilungsaktivität in der Kulturschale meist nach kurzer Zeit einstellen (replikative Seneszenz).
ES-Zellen bilden im Embryo die Vorläufer für sämtliche Körperzellen, nicht jedoch für die embryonalen Anteile der Plazenta. 2003 konnte im Mausmodell zudem erstmals gezeigt werden, dass ES-Zellen auch zu Keimzellen (Gameten, in der genannten Studie zu Eizellen) differenzieren können.[4]
Eine bemerkenswerte Eigenschaft von ES-Zellen der Maus besteht darin, dass sie in Präimplantationsembryonen wieder eingeführt werden können und nach deren Transfer in scheinschwangere Tiere am Aufbau aller fötalen Gewebe beteiligt werden. Dies kann für die zielgerichtete Ausschaltung bestimmter Gene in Mäusen benutzt werden. Knock-out-Mäuse, die sich unter Nutzung von ES-Zellen deutlich schneller produzieren lassen als mit herkömmlichen Techniken, sind von hohem Wert für die Erforschung von Genfunktionen und werden auch als menschliche Krankheitsmodelle verwendet.
Weiterhin können ES-Zellen in vitro mehr oder weniger gezielt zu verschiedensten Zelltypen ausdifferenziert werden, z. B. in Nervenzellen. Dieses Gebiet wurde insbesondere ab 1998 mit der erstmaligen Etablierung von humanen ES-Zellen (hES-Zellen) durch James Thomson und John D. Gearhart belebt. hES-Zellen werden im Allgemeinen aus sogenannten überzähligen Embryonen gewonnen, die durch In-vitro-Fertilisation entstanden sind, nicht mehr für Fortpflanzungszwecke benötigt werden und daher tiefgefroren gelagert werden. Das Hauptinteresse der Forschung an hES-Zellen gilt der Differenzierung in spezialisierte Zellen, um diese für mögliche Zellersatztherapien verfügbar zu machen.
ES-Zellen werden möglicherweise eines Tages in der Medizin als Ersatzmaterial dienlich sein können. Die Krankheit Morbus Parkinson konnte unter Nutzung differenzierter hES-Zellen zumindest in Tierversuchen bereits behandelt werden. Solche und andere – vor allem im Tiermodell gewonnenen – Erkenntnisse wurden jedoch noch nicht bei größeren Säugetieren bestätigt. Trotzdem hat die US-amerikanische Firma Geron bereits erste klinische Studien unter Nutzung von hES-Zellen für die Therapie von Rückenmarksverletzungen für 2008 angekündigt. Prinzipiell bedürfen die bisherigen Ergebnisse jedoch noch einer strengen Überprüfung, so dass im Gegensatz zu den adulten Stammzellen (s. u.) eine mögliche klinische Anwendung noch weit entfernt ist.[5] So können hES-Zellen beispielsweise nach Transplantation in Versuchstiere Tumoren bilden, so dass vor einem klinischen Einsatz sichergestellt sein muss, dass die Transplantate keine undifferenzierten hES-Zellen mehr enthalten. Von großer Relevanz könnte auch die immunologisch bedingte Abstoßung entsprechender Transplantate durch den Empfänger sein, ein aus der Transplantationsmedizin hinlänglich bekanntes Problem.
Eine ethisch weitgehend unbedenkliche Quelle für embryonale Stammzellen könnten unbefruchtete Eizellen darstellen, die im Rahmen von Fruchtbarkeitsbehandlungen anfallen und nicht befruchtet werden. Durch elektrische oder chemische Reize können diese Eizellen zur Teilung angeregt werden (Parthenogenese), woraus zum Beispiel Herzmuskelzellen gezüchtet werden können.[6]
Klonen
Neben der Gewinnung von ES-Zellen aus IVF-Blastozysten ist auch eine Gewinnung von ES-Zellen durch Klonen von Embryonen möglich. Grundlage für diese Möglichkeit war das erste erfolgreiche Klonen eines Säugetiers im Jahr 1996, des Schafs „Dolly“. Unter Nutzung dieser Technik kann durch Übertragung des Zellkerns aus einer Körperzelle in eine unbefruchtete, von der inneren Zellmasse befreite Eizelle ein früher Embryo entstehen, aus dem ES-Zellen angelegt werden können. Die Methode hätte bei der Anwendung auf den Menschen den Vorteil, dass mit dem Spender genetisch (und damit immunologisch) identische ES-Zellen zur Verfügung stünden.
Die Forschung an embryonalen Stammzellen gelang auch durch gefälschte Ergebnisse in den Fokus der Öffentlichkeit: Im Jahr 2004 publizierte das Forschungsteam um den südkoreanischen Tiermediziner Hwang Woo-suk, es sei erstmals gelungen, einen menschlichen Embryo zu klonen und auf diese Weise Stammzelllinien zu gewinnen (Therapeutisches Klonen). 2005 folgte eine Publikation, ebenfalls in der angesehenen Fachzeitschrift Science, der zufolge die weltweit ersten maßgeschneiderten embryonalen Stammzellen für schwerstkranke Patienten etabliert worden seien. Beide Publikationen stellten sich als weitgehend gefälscht heraus.
Einen möglichen Durchbruch im Therapeutischen Klonen von Primaten stellen die erstmals im Juni 2007 vorgestellten Ergebnisse eines US-amerikanischen Forscherteams um Shoukhrat Mitalipov dar.[7] Dem Team gelang es, Rhesusaffen zu klonen und aus den erhaltenen Embryonen zwei Linien embryonaler Stammzellen zu gewinnen. Angewandt wurde dabei das gleiche Verfahren wie bei dem Schaf „Dolly“. Diese Ergebnisse wurden am 14. November 2007 von unabhängiger Seite bestätigt.[8]
Ethische Kontroverse
Die Art der Gewinnung menschlicher embryonaler Stammzellen (abgekürzt oft: hES-Zellen; h = human) nach In-vitro-Fertilisation führte zu einer hitzigen, bis heute andauernden ethischen Debatte.
Die Verwendung von menschlichen embryonalen Stammzellen in der Forschung und Medizin wird von einem Teil der Gesellschaft abgelehnt, da zu ihrer Gewinnung die Zerstörung von frühen menschlichen Embryonen erforderlich ist („verbrauchende“ Embryonenforschung). Grundsätzlich geht es bei der Diskussion in Deutschland vor allem um die Frage, ob der frühe Embryo als menschliches Wesen unter den Würdeschutz des Grundgesetzes fällt und damit sein Leben keinerlei Abwägungen unterliegen dürfe. Die Gegner der Stammzellenforschung bemühen dabei oftmals die so genannten SKIP-Argumente, um von ihrer Position zu überzeugen.[9] Die Befürworter der Forschung an embryonalen Stammzellen führen hingegen häufig das Argument des möglicherweise sehr hohen positiven Potentials der Forschung mit humanen embryonalen Stammzellen ins Feld: Die Wissenschaftler erhoffen sich unter anderem eine Heilung schwerer Krankheiten (Parkinson-Krankheit, Diabetes mellitus, Querschnittlähmung) sowie die Möglichkeit, zerstörte Organe nachwachsen zu lassen. Konkrete Hinweise auf solche therapeutischen Erfolge gibt es allerdings zum gegenwärtigen Zeitpunkt lediglich aus Tierexperimenten mit Nagern.
Die Deutsche Bischofskonferenz (katholisch) vertritt die Meinung, dass menschliches Leben ab der Befruchtung der Eizelle vorliege. Dementsprechend gebühre dem Menschen ab der Befruchtung eine Würde, die eine Zerstörung der befruchteten Eizelle verbiete.[10] Ebenso äußerte sich die Kongregation für die Glaubenslehre unter Joseph Ratzinger 1987 in der Instruktion Donum Vitae.[11] Papst Johannes Paul II. äußerte sich u. a. hierzu in der Enzyklika Evangelium vitae 1995 und griff die entsprechenden Aspekte der Fragestellung aus Donum Vitae auf.[12] Die päpstliche Akademie für das Leben gab 2000 eine entsprechende Erklärung heraus, die sich insbesondere mit technischen Fragen der Stammzellforschung auseinandersetzt.[13] Eine der letzten katholischen Stellungnahmen diesbezüglich war die Erklärung Dignitas personae der Römischen Glaubenskongregation.[14]
Ebenso gibt es theologische Überzeugungen, dass bereits der frühe Embryo beseelt sei. Dieser Embryo habe eine Seele und stehe deshalb unter besonderem Schutz. Darauf Bezug nehmend weisen manche Befürworter der Stammzellforschung darauf hin, dass man im Anschluss an Thomas von Aquin in der katholischen Kirche bis in die Neuzeit glaubte, dass die Beseelung des Embryos schrittweise erfolge (Sukzessivbeseelung) und die höchste Form der Seele, die „anima intellectiva“, erst ca. drei Monate nach der Empfängnis übertragen werde. Endgültig hat die katholische Kirche erst in der Bulle Apostolicae Sedis (1869, unter Pius IX.) die Lehre von der vollen Menschwerdung am 80. Tag aufgegeben.
Die evangelische Kirche hingegen möchte die Dialogfindung unterstützen, um einen Konsens in dieser Frage zu finden. Einig sind sich die Vertreter der evangelischen Kirche darüber, dass für die Isolierung embryonaler Stammzellen keine Embryonen hergestellt werden dürfen. Zur Frage der generellen Verwendung von schon bestehenden embryonalen Stammzellen hat sie bisher noch nicht Stellung bezogen; sie möchte die Grundlagenforschung an embryonalen Stammzellen „so schnell wie möglich hinter sich lassen“.[15]
Beim Streit um den moralischen Status des Embryos werden zusammengefasst und ergänzt unter anderem folgende Zeitpunkte[16] diskutiert:
- Moment der Empfängnis (Kernverschmelzung)
- Differenzierung von Embryo und Plazenta
- Zeitpunkt, ab dem eine Mehrlingsbildung ausgeschlossen ist
- Nidation
- Erste Ausbildung von Hirnzellen
- Geburt
- Erste Wochen nach der Geburt
Europäischer Gerichtshof
Menschliche embryonale Stammzellen, für deren Gewinnung Embryonen zerstört werden müssen, so der Europäische Gerichtshof (EuGH) am 18. Oktober 2011, dürfen nicht patentiert werden, da es sich bei befruchteten Eizellen bereits um menschliches Leben handle. Mit diesem Urteil entschied der EuGH einen Patentstreit zwischen dem Neurobiologen Oliver Brüstle und Greenpeace.[17]
Deutschland
Nach dem Embryonenschutzgesetz ist es in Deutschland verboten, menschliche Embryonen (also auch Blastozysten, die als Quelle für embryonale Stammzellen dienen) für Forschungszwecke herzustellen, zu klonen oder zu zerstören. Die Forschung an importierten embryonalen Stammzellen ist jedoch unter Auflagen möglich und wurde zunächst durch das Stammzellgesetz vom Juli 2002 geregelt. Dieses Gesetz und insbesondere die darin enthaltene Regelung, dass nur embryonale Stammzellen nach Deutschland importiert werden durften, die vor dem 1. Januar 2002 gewonnen worden waren (Stichtagsregelung), war von Beginn an umstritten. Im Frühjahr 2008 debattierte der Deutsche Bundestag über eine Novellierung des Stammzellgesetzes, in der neben der Verschiebung des Stichtages auch die völlige Freigabe des Imports sowie das Verbot der Stammzellforschung mit embryonalen Stammzellen in Gruppenanträgen vorgeschlagen wurde.[18] Am 11. April 2008 beschloss der Deutsche Bundestag einen neuen Stichtag, so dass nun Stammzellen importiert werden dürfen, die vor dem 1. Mai 2007 gewonnen wurden.[19]
Das Robert Koch-Institut führt gemäß § 11 Stammzellgesetz (StZG) ein öffentlich zugängliches Register. Dieses enthält Angaben zu genehmigten Forschungsvorhaben nach dem StZG und zu den humanen embryonalen Stammzell-Linien enthalten sind, deren Import und Verwendung genehmigt worden ist.[20]
Österreich
In Österreich ist die Forschung an importierten pluripotenten embryonalen Stammzellen nach geltendem Recht ohne Einschränkungen erlaubt. Dies gilt auch für das therapeutische Klonen. Verboten wäre jedoch gemäß § 9 des Fortpflanzungsmedizingesetzes die Gewinnung von embryonalen Stammzellen, sofern diese in Österreich stattfände. Die Verwendung von totipotenten Stammzellen ist nur zu Zwecken der Fortpflanzung erlaubt.[21]
Polen
In Polen wird die Forschung an menschlichen Embryonen bestraft, wenn diese zur Zerstörung des Embryos in vitro führt. Dies wird mit der Abtreibung gleichgesetzt und kann mit Freiheitsstrafen von bis zu drei Jahren geahndet werden. Zur Forschung mit embryonalen Stammzellen aus dem Ausland gibt es keine bindende gesetzliche Regelung. Zurzeit gilt die Richtlinie vom 13. Januar 2004; sie besagt, dass „Forschung an embryonalen Stammzellen nur dann zugelassen werden sollte, wenn sie die Rettung menschlichen Lebens zum Ziel hat.“[22] Hier bietet die Definition des „menschlichen Lebens“ jedoch viel Interpretationsspielraum.
Schweiz
In der Schweiz dürfen Wissenschaftler aus überzähligen menschlichen Embryonen (das heißt aus solchen, die in der Fortpflanzungsmedizin keine Verwendung finden) Stammzellen gewinnen und mit den Zellen forschen. Der Schweizer Bundesrat verabschiedete im Februar 2005 ein entsprechendes Gesetz, nachdem sich zuvor in einer Volksabstimmung mehr als 66 Prozent der Schweizer Wähler für dieses Gesetz ausgesprochen hatten.[23] Voraussetzung gemäß Art. 5 ff. Stammzellforschungsgesetz ist, dass die Einwilligung des Spenderpaares vorliegt, die Spende unentgeltlich erfolgt und keine der Personen, für deren Forschungsprojekt die Zellen gewonnen werden, am Fortpflanzungsverfahren beteiligt war. Das Klonen von menschlichen Zellen ist verboten.
Großbritannien
In Großbritannien ist sowohl die Erzeugung von menschlichen embryonalen Stammzellen als auch das Klonen menschlicher Embryonen zu Forschungszwecken erlaubt.
Vereinigte Staaten
In den USA wurde die Forschung an embryonalen Stammzellen mit öffentlichen Mitteln des Bundes bis Ende 2009 nur gefördert, wenn die verwendeten Stammzelllinien schon vor August 2001 existierten. Im Juli 2006 hatten der US-Senat und das Repräsentantenhaus zwar für eine Aufhebung dieser Einschränkung gestimmt; dagegen hat Präsident Bush jedoch sein Veto eingelegt.[24][25][26] Für die Forschungsförderung der Bundesstaaten und für privat finanzierte Forschung hatte diese Einschränkung allerdings keine Gültigkeit.[27] Daher konnte Kalifornien 2004 in einer Volksabstimmung beschließen, die embryonale Stammzellforschung mit drei Milliarden Dollar zu fördern.[28] Im März 2009 hatte Präsident Obama angekündigt, dass er die Stammzellenforschung wieder mit Staatsgeldern fördern wolle. Diese Ankündigung wurde im Dezember 2009 durch die zuständigen Behörden umgesetzt, indem sie die Nutzung von zunächst 13 Linien embryonaler Stammzellen freigaben.[29] Im August 2010 wurde diese Förderung von einem US-Gericht wieder blockiert, da sie gegen ein Gesetz verstoße, das die Zerstörung menschlicher Embryonen verbietet.[30]
Postembryonale Stammzellen
Die Gruppe der postembryonalen Stammzellen umfasst all jene Stammzellen, die nach Abschluss der Embryonalentwicklung im Organismus von Säugetieren vorkommen. Nach ihrem ontogenetischen Alter werden sie weiterhin in fötale, neonatale und adulte Stammzellen unterteilt.
Das Differenzierungspotential von postembryonalen Stammzellen ist nach gegenwärtiger Erkenntnis auf die Ausreifung genetisch determinierter Gewebe – etwa der Haut, der Leber oder des hämatopoetischen Systems – beschränkt. Sie werden daher im Gegensatz zu den ES-Zellen nicht mehr als pluripotent, sondern nur noch als multipotent bezeichnet.
Adulte Stammzellen
Während embryonale Stammzellen nur im frühen Embryo vorkommen, sind adulte (vom lateinischen für erwachsen, auch somatisch genannte) Stammzellen im Organismus nach der Geburt (postnatales Stadium) vorhanden. Aus diesen Zellen werden während der gesamten Lebensdauer des Organismus neue spezialisierte Zellen gebildet. Adulte Stammzellen, die in Organen (besonders im Knochenmark, in der Haut, aber auch im Fettgewebe, in der Nabelschnur und im Nabelschnurblut, im Menstruationsblut,[31] im Gehirn, der Leber oder der Bauchspeicheldrüse) zu finden sind, haben aber im Allgemeinen in Zellkultur ein deutlich geringeres Selbsterneuerungsvermögen und ein eingeschränkteres Differenzierungspotential als embryonale Stammzellen. So können sich neurale Stammzellen zu allen Zelltypen des Nervengewebes (Neuronen, Glia etc.), wohl aber nicht zu Leber- oder Muskelzellen entwickeln. Ein Keimblatt-überschreitendes Differenzierungspotential bestimmter Stammzelltypen (Fähigkeit zur Transdifferenzierung) wurde in verschiedenen Studien beobachtet, ist jedoch höchst umstritten.
Adulte Stammzellen sind in jedem Individuum verfügbar, so dass die Perspektive des Ersatzes durch körpereigene, d. h. autologe Zellen gegeben ist und sie sich dadurch für die Technik des Tissue Engineering anbieten. Auch scheint die Neigung zur malignen Entartung bei Implantation adulter Stammzellen geringer zu sein als bei embryonalen Stammzellen. Eine Entartung konnte bei der klinischen Verwendung von adulten Stammzellen bisher nicht beobachtet werden.
Die Gewinnung von adulten Stammzellen und von Progenitorzellen aus dem Knochenmark erfolgt mittels Punktion des Beckenknochens unter Vollnarkose oder neuerdings verstärkt mittels der Stammzellapherese. Die Gewinnung von Nabelschnurblutstammzellen erfolgt nach der Abnabelung des Kindes, durch die Entnahme des restlichen, noch in Nabelschnur und Plazenta befindlichen Bluts. Die Gewinnung von multipotenten Stammzellen aus der Haut erfolgt mittels einer kleinen Hautbiopsie in örtlicher Betäubung im ambulanten Bereich. Danach werden die Stammzellen aus dem Gewebeverband gelöst und stehen zur weiteren Verwendung oder der Lagerung über viele Jahre als Vorsorge, wie schon heute von deutschen Unternehmen angeboten, zur Verfügung. Im Rahmen einer normalen Eigenblutspende können zirkulierende Endotheliale Vorläuferzellen gewonnen werden. Das Potential dieser autologen (körpereigenen) Vorläuferzellen für die Therapie von Herz- und Gefäßerkrankungen wird derzeit in klinischen Studien untersucht. Der Vorteil der Verwendung autologer Vorläuferzellen liegt in der fehlenden Immunogenität, d. h. die transplantierten Zellen werden vom Immunsystem nicht als fremd erkannt.
Der niederländische Immunologe und Molekularbiologe Hans Clevers hat 2009 ein Verfahren zur Vermehrung adulter Stammzellen entwickelt, mit dem er rudimentäre Organe im Miniaturformat (sogenannte Organoide) züchten kann, wofür er im September 2016 den mit 750.000 Euro dotieren Körber-Preis für die Europäische Wissenschaft erhielt.[32][33] Der Preisträger interessiert sich besonders für die Signale, die Stammzellen zur Teilung anregen. Mittels eines von ihm entdeckten Rezeptors (Lgr5), der nur bei Stammzellen vorkommt, konnte er diese aus entnommenem Darmgewebe isolieren.[34] Aus Tumorgewebe können Mini-Organe erzeugt werden, an denen Medikamente getestet werden. 2013 war Clevers in der Lage, Darm-Stammzellen von Patienten, die an der Erbkrankheit Mukoviszidose leiden, mithilfe des Genome Editing von diesem Gendefekt zu befreien.[35]
Künstlich reprogrammierte Stammzellen
Kazutoshi Takahashi und Shinya Yamanaka von der Universität Kyōto und Forscher von der Universität Wisconsin berichteten 2006 bzw. 2007 in Cell und Science, es sei ihnen gelungen, Körperzellen erwachsener Menschen in induzierte pluripotente Stammzellen (iPS) umzuwandeln.[36] Dabei seien vier zentrale, ruhende Entwicklungsgene in den Zellen aktiviert worden, so dass sie in eine Art embryonalen Zustand zurückversetzt wurden. Aus den künstlich reprogrammierten Stammzellen konnten die Forscher in der Petrischale gereifte Zellen, z. B. Herzmuskel- und Nervenzellen, heranzüchten.[37][38]
Zur erstmaligen Reprogrammierung wurden die Gene Oct-4, Sox-2, c-Myc und Klf-4 mit Retroviren in die Zellen geschleust (Transduktion). Im Tierversuch entwickelte ein Fünftel der verwendeten Mäuse Tumoren, vermutlich, weil zwei der verwendeten Gene krebsfördernd sein können (sog. Protoonkogene). Um bei medizinischer Anwendung ein Risiko durch eingebrachte krebsfördernde Gene auszuschließen, werden alternative Methoden zur Reprogrammierung gesucht. Geforscht wird u. a. an kleinen Molekülen (z. B. Peptiden), die die natürlich im Erbgut der Zelle vorkommenden Stammzellgene aktivieren.[39] Um eine Tumorbildung zu vermeiden, versuchen Forscher außerdem die Methode der Geneinschleusung mit Retroviren und die Nutzung der Protoonkogene c-Myc und Klf-4 zu vermeiden, indem die Einschleusung mit nicht-integrierenden Adenoviren und alternativen Genen (Nanog, lin-28) durchgeführt wird.[40][41]
Im Gegensatz zu Retroviren wird die gewünschte Gensequenz durch Adenoviren nicht in das Genom der Wirtszelle integriert, womit die Integrität des Wirtsgenoms erhalten bleibt.
Darüber hinaus ist es gelungen, iPS-Zellen durch Transfektion nur eines Pluripotenzgens aus Zellen zu erzeugen, die die übrigen drei Gene natürlich exprimieren.[42]
Im Dezember 2007 berichteten Forscher um Jacob Hanna vom Whitehead Institute for Biomedical Research im US-amerikanischen Cambridge, dass es gelungen sei, mit iPS-Zellen Mäuse zu heilen, die an Sichelzellenanämie gelitten hatten. In den aus dem Schwanz mittels Reprogrammierung gewonnenen iPS-Zellen ersetzten die Forscher das veränderte Gen, welches die Sichelzellenanämie auslöst durch die gesunde Erbanlage mittels homologer Rekombination. Aus den so behandelten Stammzellen wurden blutbildende Vorläuferzellen gezüchtet, die sich zu verschiedenen Blutzellen und Zellen des Immunsystems weiterentwickeln können. Die Vorläuferzellen wurden in die erkrankten Mäuse transplantiert, wo sie offenbar zu gesunden Blutzellen heranwuchsen. Wie das Team berichtet, verschwanden die Symptome der Versuchstiere durch die Behandlung nahezu vollständig.[43] Diese und verwandte Veröffentlichungen sind allerdings mit gewissem Vorbehalt zu betrachten. Es sind mehrere unklare Angaben zu Proteinen, zur zellulären Biochemie und zu Zellprozessen zu finden, wie z. B. zum Homöoboxprotein NANOG oder zu c-Myc bezüglich Krebsentstehung.
In Deutschland forschen u. a. Hans Schöler, Direktor am Max-Planck-Institut für molekulare Biomedizin in Münster und Oliver Brüstle, Direktor des Instituts für Rekonstruktive Neurobiologie der Universität Bonn über iPS-Zellen. Die beiden Wissenschaftler leiten gemeinsam das Netzwerk Stammzellforschung NRW.[44] Ihre Erwartungen richten sich aus der Stammzellforschung heraus auf die Entwicklung von Medikamenten, die sie mittelfristig als besonders vielversprechend ansehen.
Stammzellmedizin
Seit über 40 Jahren werden die blutbildenden Stammzellen des Knochenmarks in der Behandlung von Leukämie und von Lymphomen eingesetzt (siehe auch Stammzelltransplantation). Während einer Chemotherapie z. B. werden die meisten schnell wachsenden Zellen durch zytotoxische Bestandteile zerstört. Dadurch werden nicht nur die Krebszellen abgetötet; auch die Stammzellen, die andere Körperzellen reparieren sollten, werden durch die Therapie in Mitleidenschaft gezogen. Besonders betroffen sind hierbei die blutbildenden Stammzellen. Deshalb werden vor der Chemotherapie Stammzellen aus dem Knochenmark des Patienten (durch sogenannte autologe Transplantation) oder von einem passenden Spender gewonnen (sogenannte allogene Transplantation). Nach Abschluss der chemotherapeutischen Behandlung werden die blutbildenden Stammzellen injiziert. Diese Stammzellen produzieren dann große Mengen an roten und weißen Blutkörperchen, wodurch das Blut gesund erhalten werden kann und Infektionen besser abgewehrt werden können.
Nicht blutbildende adulte Stammzellen sind innerhalb einzelner Studien bereits mit Erfolg bei Lähmungen nach Wirbelsäulenverletzungen und bei Morbus Parkinson eingesetzt worden. Bei erfolgreichen klinischen Studien konnten Stammzellen aus dem Knochenmark Patienten nach Herzinfarkt oder bei Multipler Sklerose zu einer besseren Regeneration verhelfen. Inzwischen hat man auch in der Haut multipotente Stammzellen entdeckt, die sich potentiell in allen Organgeweben des Menschen entwickeln und hier zur Regeneration beitragen können.
Im Oktober 2010 begann in den USA eine erste klinische Testphase, in der geklärt werden soll, ob erfolgreiche Experimente mit querschnittgelähmten Ratten auf frisch am Rückenmark verletzte Menschen übertragbar sind.[45]
Stammzellforschung
Derzeit gelingt es in Versuchen an Ratten, Gehirntumoren durch die Injektion von adulten Stammzellen zu behandeln. Wissenschaftler der Harvard University haben die Zellen gentechnisch so verändert, dass sie eine andere, gleichzeitig injizierte Substanz in einen Krebszellen tötenden Stoff umwandeln. Die Größe der Tumoren konnte um 80 Prozent reduziert werden.
Stammzellen scheinen außerdem in der Lage zu sein, Zellen, die durch einen Herzinfarkt geschädigt wurden, zu erneuern. An der Columbia-Presbyterian University ist es gelungen, die Herzfunktion nach einem Infarkt bei Mäusen durch die Injektion von Knochenmark-Stammzellen um 33 Prozent zu verbessern. Das zerstörte Gewebe regenerierte sich zu 68 Prozent wieder. Allerdings wird mittlerweile davon ausgegangen, dass dieses auf parakrine oder andere Effekte der transplantierten Zellen zurückzuführen ist, eine Transdifferenzierung hämatopoetischer Stammzellen zu Kardiomyozyten fand jedoch nicht statt.[46]
Die Anwendung autologer Stammzellen bei Herzschäden wird in verschiedenen Herzzentren europaweit in klinischen Studien untersucht. Inwieweit tatsächlich Herzmuskelzellen regeneriert werden ist bisher ungeklärt. In Deutschland wird u. a. am Klinikum der Universität Frankfurt in einer klinischen Studie der Nutzen von Stammzellen für die Regeneration des Herzens erforscht. Adulte Stammzellen werden hier durch Zentrifugation aus Blut gewonnen, durch anschließende Ausbringung auf Fibronectin-Platten kultiviert und auf diesen selektiv angereichert; sie haften auf den Platten an, so dass andere Zellen abgespült werden können. Nach drei Tagen Kultivierung können sie von den Platten abgelöst und – mit Hilfe geeigneter Nährmedien – ins Herz eingebracht werden. In vergleichbarer Weise können adulte Stammzellen auch aus Muskelgewebe aus der Haut gewonnen werden, allerdings dauert hier die Kultivierung nicht drei, sondern ungefähr 20 Tage.
Ein weiterer wichtiger Anwendungsbereich für adulte Stammzellen ist die Regeneration von Knorpel und Knochen. Verschiedene renommierte Forschungsinstitute in Israel, England und Slowenien haben relevante klinische Daten publiziert.
Die Forschung mit pluripotenten Stammzellen hat jedoch 2011 einen massiven Rückschlag erlitten, der schlimmstenfalls zum Ende des bisherigen Hoffnungsträgers der regenerativen Medizin führen könnte. Wissenschaftler der University of California, San Diego School of Medicine und des Scripps Research Institute wiesen schwere genetische Veränderungen in pluripotenten Stammzelllinien nach. Demnach weisen humane embryonale Stammzellen (hESC) und induzierte pluripotente Stammzellen (iPSC) häufiger Genom-Aberrationen auf als ihre normalen Zellpendants. In den untersuchten hESCs lagen erhebliche Duplikationen vor, während die iPSCs erhebliche Deletionen aufwiesen. Die Auswirkungen dieser genetischen Veränderungen auf potenzielle klinische Anwendungen sind jedoch noch unklar.[47][48]
Am 15. Mai 2013 wurde in Cell berichtet, dass es erstmals gelungen sei, im Wege des Zellkerntransfers pluripotente menschliche Stammzellen zu gewinnen und zu spezialisierten Zellen der Bauchspeicheldrüse sowie zu Blut-, Herz-, Leber- und Nervenzellen fortzuentwickeln.[49]
Mittlerweile gibt es auf Basis von embryonalen Stammzellen neue Therapiemöglichkeiten. Seit April 2011, laufen die einzigen zwei von der US-FDA (Food and Drug Administration) genehmigten Patientenversuche.[50] Hier werden ältere Patienten mit trockener Makuladegeneration (AMD) und jüngere Patienten mit Stargardt Dystrophy (SMD) mit (RPE)-Zellen behandelt, d. h. ihnen werden 50–200.0000 Retinal Pigment Epithel (RPE)-Zellen in die Retina eines Auges injiziert. Diese Zellen werden aus embryonalen Stammzellen gewonnen, ohne dass ein Embryo zerstört wird (patentierte Blastomertechnik, ähnlich der PID-Diagnostik). Mittlerweile sind über 40 Patienten in vier Augenkliniken der USA und zwei in Großbritannien behandelt worden. Im Oktober 2014 erschien in The Lancet ein Peer-Review Artikel.[51] Ihm zufolge habe die Mehrzahl der Patienten signifikante Sehverbesserungen aufgewiesen. Dies hat die US-FDA dazu bewogen, auch für jüngere Patienten eine Versuchsreihe zu genehmigen. Grundsätzlich beginnen solche Versuche mit älteren Patienten, die schon eine fortgeschrittene Erkrankung ihrer Sehleistung haben. Vorrangig geht es um die sichere Verwendung der Therapie.
Stammzellengewinnung aus dem Zahnmark der Milchzähne
Das Milchzahngebiss eignet sich als Quelle der Stammzellengewinnung.[52] Die im Zahnmark befindlichen Zellen können extrahiert, mit einem speziellen Wachstumsmittel kultiviert und schließlich für medizinisch Zwecke konserviert werden.[53] Die Stammzellen können in der Zahnmedizin für die Regeneration der dentalen Pulpa bei Erwachsenen eingesetzt werden. Mithilfe einer Verpflanzung von Stammzellen im Rahmen eines Tissue Engineerings können sich Teile der Wurzelkanäle wieder erneuern.[54]
Literatur
Bücher
- Thomas Heinemann, Jens Kersten: Stammzellforschung. Naturwissenschaftliche, rechtliche und ethische Aspekte. Sachstandsberichte des DRZE. Band 4. Verlag Karl Alber, Freiburg 2007, ISBN 978-3-495-48196-7.
- DRZE/ Wissenschaftliche Abteilung im Auftrag des Kompetenznetzwerks Stammzellforschung NRW (Hrsg.): Dossier Stammzellforschung. Zentrale nationale und internationale gesetzliche Richtlinien und Übereinkommen sowie Stellungnahmen nationaler und internationaler Institutionen.
- Elmar Brähler (Hrsg.): Vom Stammbaum zur Stammzelle. Reproduktionsmedizin, Pränataldiagnostik und menschlicher Rohstoff. 2002.
- Achim Limbeck: Embryonenschutzgesetz und Forschung an menschlichen Stammzellen. Eine strafrechtliche Untersuchung der Forschung an menschlichen Stammzellen, insbesondere vor dem Hintergrund des Embryonenschutzgesetzes, 2006, ISBN 3-9810745-9-9. (Umfangreiche Wiedergabe des Forschungsstandes sowie der mit der Forschung verbundenen strafrechtlichen Problematik).
- Eberhard J. Wormer: Mehr Wissen über Stammzellen. Mit Einführungsbeiträgen von Werner Kaufmann, Detlev Ganten, Gerd Kempermann. Lingen, Köln 2003, ISBN 3-937490-00-0.
- Mike S. Schäfer: Wissenschaft in den Medien. Die Medialisierung naturwissenschaftlicher Themen. Wiesbaden: Verlag für Sozialwissenschaften. 2007, ISBN 978-3-531-15592-0.
- Anna M. Wobus u. a.: Stammzellforschung und Zelltherapie. Stand des Wissens und der Rahmenbedingungen in Deutschland. Mit Beiträgen von Christine Hauskeller und Jochen Taupitz. München 2006, ISBN 3-8274-1790-2.
- Gerd Kempermann: Neue Zellen braucht der Mensch. Die Stammzellforschung und die Revolution der Medizin. Piper Verlag, München 2008, ISBN 978-3-492-05179-8.
Aufsätze
- Michael Feld, Jürgen Hescheler: Stammzellen: Potente Zellen. In: Spektrum der Wissenschaft. Mai 2003, S. 66–73.
- Michael Groß: Die Insel der Stammzellforscher. In: Nachrichten aus der Chemie. 52(12), 2004, S. 1261–1263, ISSN 1439-9598.
- Lars Grotewold: Wie bleiben Zellen pluripotent? Bilanz eines Vierteljahrhunderts Stammzellforschung. In: Naturwissenschaftliche Rundschau. 58(8), 2005, S. 413–419.
- Stem Cells. In: Nature Band 441, Heft 7097, vom 29. Juni 2006, S. 1059–1102 (eine sehr ausführliche Übersicht zum Stand der Forschung, auf englisch)
- Stephan Ernst: Mensch oder Material? Theologisch-ethische Anmerkungen zu den Ebenen des Diskurses um die Stammzellforschung. In: Würzburger medizinhistorische Mitteilungen 23, 2004, S. 457–470.
- Davor Solter: From teratocarcinomas to embryonic stem cells and beyond: a history of embryonic stem cell research. In: Nature Reviews Genetics. (7), 2006, S. 319–327.
- Peter Löser, Anna M. Wobus: Aktuelle Entwicklungen in der Forschung mit humanen embryonalen Stammzellen. In: Naturwissenschaftliche Rundschau. 60(5), 2007, S. 229–237.
- Alexander A. Maximow: Der Lymphozyt als gemeinsame Stammzelle der verschiedenen Blutelemente in der embryonalen Entwicklung und im postfetalen Leben der Säugetiere. Demonstrationsvortrag, gehalten in der außerordentlichen Sitzung der Berliner Hämatologischen Gesellschaft am 1. Juni 1909. In: Folia Haematologica. 8.1909, S. 125–134 (jetzt open access).
Weblinks
Historisches
- Remarks to trace the scientific steps that eventually led to the recognition of the blood stem cell as an important entity of its own Anmerkungen von Theodor M. Fliedner in Stem Cells, Band 16 (6), 1998, S. 357–360.
Gesellschaftliches
- „Stammzellforschung – ein kontroverses Thema für einen anspruchsvollen Unterricht“
- Kompetenznetzwerk Stammzellforschung NRW
- Blickpunkt „Forschung mit humanen embryonalen Stammzellen“ (Deutsches Referenzzentrum für Ethik in den Biowissenschaften)
- Stammzellen-Debatte.de: Informationen zur Debatte über embryonale und adulte Stammzellen, therapeutisches und reproduktives Klonen (InteressenGemeinschaft Kritische Bioethik Deutschland)
- Artikel über den Status der Stammzelle und die bioethische Diskussion in Deutschland im NOVO-Magazin.
- Andrew Siegel: Ethics of Stem Cell Research. In: Edward N. Zalta (Hrsg.): Stanford Encyclopedia of Philosophy.
Einzelnachweise
- Sean J. Morrison, Nirao M. Shah, David J. Anderson: Review: Regulatory mechanisms in stem cell biology. In: Cell. Band 88, Nr. 3, 1997, S. 287–298, doi:10.1016/S0092-8674(00)81867-X. PMID 9039255. (Volltext; PDF; 260 kB) (PDF)
- Eugene V. Koonin: The origin and early evolution of eukaryotes in the light of phylogenomics. In: Genome Biology. 2010. 11:209. doi:10.1186/gb-2010-11-5-209
- Beddington, Robertson: An assessment of the developmental potential of embryonic stem cells in the midgestation mouse embryo. In: Development. Band 105, 1989, S. 733–737.
- K. Hubner u. a.: Derivation of oocytes from mouse embryonic stem cells. In: Science. Band 300, 2003, S. 1251–1256.
- Passier, Mummery: Origin and use of embryonic and adult stem cells in differentiation and tissue repair. In: Cardivascular Research. Band 58, 2003, S. 324–335.
- Michael Didié u. a.: Parthenogenetic stem cells for tissue-engineered heart repair. In: Journal of Clinical Investigation. Band 123, Nr. 3, 2013, S. 1285–1298, doi:10.1172/JCI66854.
- Monkey stem cells cloned. In: Nature. Nr. 447, 20. Juni 2007, S. 891.
- Kathrin Zinkant: Biomedizin: Die Klonprüfung. In: Zeit Online. 1. Oktober 2009 (zeit.de [abgerufen am 17. Mai 2016] Nr. 46.): „Ein australisches Forscherteam hat die Primatenstammzellen genetisch geprüft und bestätigt, dass es sich ganz sicher um geklonte ES-Zellen der Versuchsaffen aus Oregon handelt.“
- G. Damschen, D. Schönecker: Der moralische Status menschlicher Embryonen. de Gruyter, Berlin 2002.
- Kommentar der DBK zum Stammzellen-Urteil des Europäischen Gerichtshofes.
- Die Instruktion Donum Vitae.
- Enzyklika Evangelium Vitae.
- Erklärung der päpstlichen Akademie für das Leben.
- Dignitas Personae.
- Stellungnahme zur Verschiebung des Stichtages zum Import von ES-Zellen.
- Stephan Ernst: Mensch oder Material? Theologisch-ethische Anmerkungen zu den Ebenen des Diskurses um die Stammzellforschung. In: Würzburger medizinhistorische Mitteilungen 23, 2004, S. 457–470; hier: S. 461–466.
- EuGH bremst Stammzellenforscher. auf: www.orf.at 18. Oktober 2011.
- www.bundestag.de (Memento vom 10. März 2009 im Internet Archive) Übersicht über die verschiedenen Gesetzentwürfe zur Debatte des Bundestages am 14. Februar 2008.
- Tagesschau: Bundestag lockert Stammzellgesetz (Memento vom 20. Februar 2009 im Internet Archive) vom 11. April 2008.
- rki.de
- austria.gv.at
- Witold Jacorzynski, Marcin Kozlowski: Auf dem Weg nach (n)irgendwo: Die polnische Stammzellforschung. In: Wolfgang Bender u. a.: Grenzüberschreitungen: kulturelle, religiöse und politische Differenzen im Kontext der Stammzellenforschung weltweit = Crossing borders. (= Darmstädter interdisziplinäre Beiträge. 10). agenda-Verlag, Münster 2005, ISBN 3-89688-258-9, S. 471.
- Schweiz erlaubt Gewinnung embryonaler Stammzellen. auf: www.3sat.de
- Denise Stevens: Embryonic stem cell research: will President Bush's limitation on federal funding put the United States at a disadvantage? A comparison between U.S. and international law. In: Houston Journal of International Law. 25, Nr. 3, 2003, S. 623–653. PMID 15199940.
- Veto gegen Stammzellenforschung. In: Stern, 20. Juli 2006.
- Michael Minkenberg: Die Christliche Rechte und die amerikanische Politik von der ersten bis zur zweiten Bush-Administration. In: Bundeszentrale für politische Bildung. B 46/2003.
- http://www.answers.com/topic/stem-cell.
- California gives go-ahead to stem-cell research, MSNBC, 3. November 2004.
- USA forschen nach acht Jahren wieder an Stammzellen. auf: orf.at, 3. Dezember 2009: „Erneut Forschung mit embryonalen Stammzellen in USA“.
- US-Gericht blockiert Obamas Stammzellen-Politik. auf welt.de, 24. August 2010.
- Bild der Wissenschaft. Ausgabe 2/2010.
- Hans Clevers – Körber-Preisträger 2016 (Video). Abgerufen am 7. September 2016.
- Hans Clevers – Körber-Preisträger 2016 (Pressemeldung). Abgerufen am 29. November 2018.
- Toshiro Sato, Hans Clevers et al.: Single Lgr5 stem cells build cryptvillus structures in vitro without a mesenchymal niche. In: Nature. 459, Nr. 7244, 2009, S. 262–265. bibcode:2009Natur.459..262S. doi:10.1038/nature07935. PMID 19329995.
- Körber-Preis für Stammzellenforscher: Ersatzorgane aus der Petrischale (Beitrag der ARD-Tagesschau vom 07.09.2016 13:31 Uhr). Abgerufen am 8. September 2016.
- K. Takahashi, S. Yamanaka: Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors. In: Cell. 126, Nr. 4, 25. August 2006, S. 663–676. doi:10.1016/j.cell.2006.07.024. PMID 16904174.
- Wendepunkt der Forschung: Künstliche Herstellung von Stammzellen gelungen. In: Frankfurter Allgemeine Zeitung. 20. November 2007.
- Gretchen Vogel: Researchers Turn Skin Cells Into Stem Cells. In: ScienceNOW. 20. November 2007, sciencemag.org.
- Reprogrammierte Hautzellen: Der Königsweg zur Stammzelle. In: Frankfurter Allgemeine Zeitung. 7. Juni 2007.
- M. Stadtfeld, M. Nagaya u. a.: Induced pluripotent stem cells generated without viral integration. In: Science. Band 322, Nummer 5903, November 2008, S. 945–949, ISSN 1095-9203. doi:10.1126/science.1162494. PMID 18818365.
- M. Nakagawa, M. Koyanagi u. a.: Generation of induced pluripotent stem cells without Myc from mouse and human fibroblasts. In: Nature biotechnology. Band 26, Nummer 1, Januar 2008, S. 101–106, ISSN 1546-1696. doi:10.1038/nbt1374. PMID 18059259.
- J. B. Kim, V. Sebastiano u. a.: Oct4-induced pluripotency in adult neural stem cells. In: Cell. Band 136, Nummer 3, Februar 2009, S. 411–419, ISSN 1097-4172. doi:10.1016/j.cell.2009.01.023. PMID 19203577.
- Gretchen Vogel: Reprogrammed Skin Cells Strut Their Stuff. In: ScienceNOW. 6. Dezember 2007, sciencemag.org.
- Netzwerk Stammzellforschung NRW.
- Stammzelltherapie für Querschnittsgelähmte. 13. Oktober 2010.
- Murry, Soonpaa u. a.: Haematopoietic stem cells do not transdifferentiate into cardiac myocytes in myocardial infarcts. In: Nature. 428, 2004, S. 664–668.
- Vlad Georgescu: Stammzellen: Die Unberechenbaren. In: DocCheckNews. 16. Februar 2011, (online)
- Louise C. Laurent u. a.: Dynamic Changes in the Copy Number of Pluripotency and Cell Proliferation Genes in Human ESCs and iPSCs during Reprogramming and Time in Culture. In: Cell Stem Cell. 8 2011, S. 106–118, doi:10.1016/j.stem.2010.12.003, online (PDF-Dokument; 1,81 MB).
- Masahito Tachibana u. a.: Human Embryonic Stem Cells Derived by Somatic Cell Nuclear Transfer. In: Cell. Online-Veröffentlichung vom 15. Mai 2013, doi:10.1016/j.cell.2013.05.006.
- ongoing-clinical-trials (Memento vom 31. März 2015 im Internet Archive). Website von OCATA Therapeutics. Abgerufen am 28. März 2015.
- Steven D. Schwartz u. a.: Human embryonic stem cell-derived retinal pigment epithelium in patients with age-related macular degeneration and Stargardt's macular dystrophy: follow-up of two open-label phase 1/2 studies. In: The Lancet. Band 385, Nr. 9967, 2015, S. 509–516, doi:10.1016/S0140-6736(14)61376-3.
- Suseela Keerti Popuri: Concerns of a Pediatric Dentist in Dental Stem Cells: An Overview. Hrsg.: The open dentistry journal. 2018, S. 596–604.
- J. Jobst: Stammzellengewinnung aus Milchzähnen. In: Kigorosa. Roman Safreider, 14. Januar 2019, abgerufen am 11. März 2019.
- G. Schmalz: Auf dem Weg zur neuen Pulpa: können wir die Pulpa regenerieren? Hrsg.: Österreichischer Zahnärztekongress 2012 und Symposium für Kinderzahnheilkunde. Volume 109. Springer Wien, September 2012, S. 52–96.