Schichtstruktur
Von einer Schichtstruktur kann gesprochen werden, wenn die Wechselwirkungen zwischen den Bausteinen innerhalb einer Ebene (Schicht) größer sind, als die Wechselwirkungen zwischen den Ebenen. Dies ist bei einigen Kristallstrukturen der Fall. Innerhalb der Schichten sind meistens polare, kovalente Bindungen vorhanden, was in eine zweidimensionale Verknüpfung resultiert. Zwischen den Schichten herrschen relativ schwache Van-der-Waals-Kräfte. Dies zeigt sich in unterschiedlichen Atomabständen und führt zu einer guten Spaltbarkeit parallel zu den Schichten. Bekannte Beispiele für Verbindungen mit Schichtstruktur sind Glimmer, Graphit und Montmorillonit.[1][2]
Beispiele für Verbindungen mit Schichtstruktur
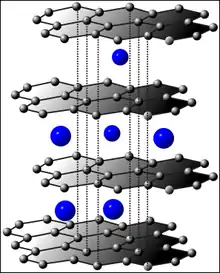
Graphit
Graphit besteht aus Schichten von Kohlenstoff-Atomen und kann als das einfachste Beispiel für eine Schichtstruktur genannt werden. Der Abstand zwischen den Kohlenstoff-Atomen innerhalb einer Schicht beträgt 142 pm, der Abstand zwischen den Schichten ist mit 335 pm deutlich größer. Die Schichten werden durch schwache Van-der-Waals-Kräfte zusammengehalten. Mit der Schichtstruktur lässt sich die Leitfähigkeit von Graphit erklären, die parallel zu den Schichtebenen etwa 5000-mal größer ist als senkrecht zu den Ebenen.[3][4]
Übergangsmetallhalogenide
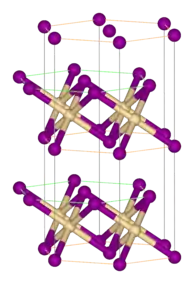
Cadmiumiodid-Struktur (CdI2)
Cadmiumiodid kristallisiert in einer Schichtstruktur im hexagonalen Kristallsystem und ist namensgebend für den CdI2-Strukturtyp. Die Struktur ist aus übereinander gestapeltem Schichtsystemen aufgebaut. Innerhalb dieser Schichten liegen kovalente Bindungen mit Ionenbildungsanteilen vor, wobei die Cadmium-Atome oktaedrisch koordiniert sind. Die Iodidionen bilden eine hexagonal-dichteste Kugelpackung, in der nur jede zweite Oktaederlückenschicht mit Cadmiumionen besetzt ist. Die Anionenschichten treten in der Schichtenfolge ABAB auf.[2][5]
Beispiele für Verbindungen, die in der Cadmiumiodid-Struktur kristallisieren, sind Titan(II)-chlorid, Titan(II)-iodid und Magnesiumbromid.
Cadmiumchlorid-Struktur (CdCl2)
Bei der Cadmiumchlorid-Struktur handelt es sich ebenfalls um eine Schichtstruktur. Die Cadmiumionen besetzen Oktaederlücken jeder zweiten Schicht und die Chloratome sind kubisch dichtest gepackt. Während in der Cadmiumiodid-Struktur die Schichten genau übereinander liegen, sind sie in der Cadmiumchlorid-Struktur gegeneinander verschoben (Schichtenfolge ABCABC).[2][6]
Vertreter der Cadmiumchlorid-Struktur sind beispielsweise Magnesiumchlorid, Nickel(II)-bromid und Zinkiodid.
Metalldisulfide
Viele Metalldisulfide kristallisieren in der CdI2-Struktur und sind aus einer Sulfidschicht, einer Metallschicht und wieder einer Sulfidschicht aufgebaut (S–M–S). Die Metallatome besetzen jede zweite Oktaederlückenschicht der hexagonal dichtesten Anionenpackung. Dies trifft beispielsweise auf die Verbindungen Titan(IV)-sulfid, Zirkonium(IV)-sulfid und Platin(IV)-sulfid zu.
Einige Metalldisulfide kristallisieren auch in der MoS2-Struktur, wo die Metallatome trigonal-prismatische Lücken zwischen paarweise gestapelten Anionenschichten (AA, BB oder CC) besetzen. Beispiele hierfür sind Niob(IV)-sulfid und Wolfram(IV)-sulfid.
Iod
Wie bereits aus der Schuppengestalt des festen Iods erkennbar, bildet Iod im festen Zustand ein Schichtstruktur aus. Die Iod-Mokelüle liegen innerhalb der Schichten alle in einer Ebene. Dabei ist der Abstand zweier Iod-Atome von benachbarten Iod-Molekülen innerhalb einer Schicht um 20 bis 80 pm kleiner als der Abstand zwischen den Schichten. Innerhalb der Schichten kommen sich die Iod-Moleküle viel näher (bis zu 349,6 pm) als der doppelte Van-der-Waals-Radius (430 pm), jedoch nicht so nahe wie bei normalen kovalenten Bindungen. Zwischen den Iod-Molekülen liegen daher erhebliche elektronische Wechselwirkungen, welche die Halbleitereigenschaft und den Metallglanz festen Iods bedingen. Festes Brom und Chlor sind entsprechend festem Iod aufgebaut, jedoch mit weniger drastisch verkürztem Abstand zwischen den Halogenmolekülen.[7][8]
 Festes, kristallines Iod
Festes, kristallines Iod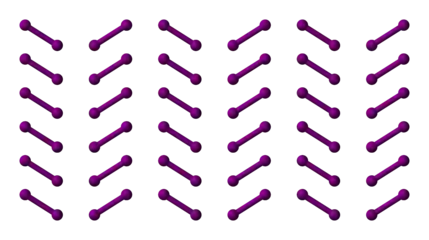 Struktur einer Schicht im festen Iod
Struktur einer Schicht im festen Iod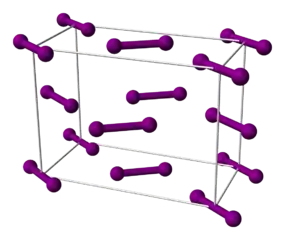 Dreidimensionale Struktur von festem Iod
Dreidimensionale Struktur von festem Iod
Schichtsilikate
Bei den Schichtsilikaten ist jedes SiO4-Tetraeder in einer Ebene über drei Ecken mit Nachbartetraedern verknüpft. Dadurch bilden sich zweidimensionale Schichten des Anions [Si4O10]4− aus. Wenn zwischen den Schichten lediglich Van-der-Waals-Kräfte auftreten (z. B. bei Talk und Kaolinit), ergeben sich weiche Minerale mit Schichten, die leicht gegeneinander verschiebbar sind. Werden die Schichten durch Kationen zusammengehalten, führt dies zu einer größeren Härte bei gleichzeitiger guter Spaltbarkeit parallel zu den Schichten. Dies ist beispielsweise bei der Struktur der Glimmer der Fall.[9][10]
 Biotit (Glimmergruppe)
Biotit (Glimmergruppe) Talk
Talk Kaolinit
Kaolinit
Anwendungen
.svg.png.webp)
Feststoffe mit Schichtstruktur wie Graphit oder Molybdän(IV)-sulfid werden häufig als Schmiermittel verwendet. Dabei können sich die Kohlenstoff- oder Sulfidschichten blätterartig parallel zu den Schichten verschieben.[11]
Ein weiterer Anwendungsschwerpunkt liegt in der Möglichkeit, zwischen den Schichten Substanzen einzulagern (Interkalation). Solche Interkalationsverbindungen finden eine wichtige praktische Anwendung in vielen Bereichen, z. B. der Lithium-Ionen-Batterie, wo Lithium-Atome zwischen die Graphitschichten interkaliert werden. Als elektrische Leiter werden zudem Kalium- und Polybromid-Graphit-Einlagerungsverbindungen genutzt. Neben anorganischen Stoffen lassen sich auch eine Reihe an organischen Verbindungen in Substanzen mit Schichtstrukturen einlagern. Ein Anwendungsbeispiel hierfür ist die Adsorption von Ferrocen an einzelne molekulare Molybdän(IV)-sulfidschichten. Das Adsorbat kann anschließend als elektrisch leitender Film auf eine Glasunterlage gezogen werden.[3][4]
Einzelnachweise
- Eintrag zu Schichtstrukturen. In: Römpp Online. Georg Thieme Verlag, abgerufen am 15. November 2018.
- Erwin Riedel, Christoph Janiak: Anorganische Chemie. 8. Auflage. De Gruyter, Berlin 2011, ISBN 978-3-11-022567-9, S. 138–139.
- James E. Huheey, Ellen A. Keiter, Richard L. Keiter: Anorganische Chemie : Prinzipien von Struktur und Reaktivität. 3. Auflage. De Gruyter, Berlin 2003, ISBN 3-11-017903-2, S. 879–880.
- Michael Binnewies, Maik Finze, Manfred Jäckel, Peer Schmidt, Helge Willner: Allgemeine und Anorganische Chemie. 3. Auflage. Springer Spektrum, Berlin 2016, S. 485–486, doi:10.1007/978-3-662-45067-3.
- Michael Binnewies, Maik Finze, Manfred Jäckel, Peer Schmidt, Helge Willner: Allgemeine und Anorganische Chemie. 3. Auflage. Springer Spektrum, Berlin 2016, S. 90–91, doi:10.1007/978-3-662-45067-3.
- James E. Huheey, Ellen A. Keiter, Richard L. Keiter: Anorganische Chemie: Prinzipien von Struktur und Reaktivität. 3. Auflage. De Gruyter, Berlin 2003, ISBN 3-11-017903-2, S. 296–298.
- James E. Huheey, Ellen A. Keiter, Richard L. Keiter: Anorganische Chemie: Prinzipien von Struktur und Reaktivität. 3. Auflage. De Gruyter, Berlin 2003, ISBN 3-11-017903-2, S. 980–981.
- A. F. Holleman, Egon Wiberg: Lehrbuch der anorganischen Chemie. 101. Auflage. De Gruyter, Berlin 1995, ISBN 3-11-012641-9, S. 447–448.
- Eintrag zu Silikate. In: Römpp Online. Georg Thieme Verlag, abgerufen am 16. November 2018.
- Erwin Riedel, Christoph Janiak: Anorganische Chemie. 8. Auflage. De Gruyter, Berlin 2011, ISBN 978-3-11-022567-9, S. 540.
- Marc-Denis Weitze, Christina Berger: Werkstoffe für Mobilität. In: Technik im Fokus. Springer, Berlin, Heidelberg 2013, ISBN 978-3-642-29540-9, S. 119–135, doi:10.1007/978-3-642-29541-6_5.
