Cadmiumchlorid
Cadmiumchlorid ist eine chemische Verbindung des Cadmiums und zählt zu den Chloriden. Das farblose Salz kristallisiert in einer charakteristischen trigonalen Kristallstruktur, die als Strukturtyp für zahlreiche weitere Verbindungen dient.
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
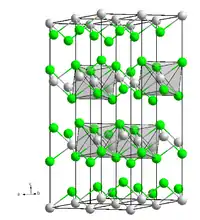 | |||||||||||||||||||
| _ Cd2+ _ Cl− | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Cadmiumchlorid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Verhältnisformel | CdCl2 | ||||||||||||||||||
| Kurzbeschreibung |
weißer, geruchloser Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 183,32 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
960 °C[1] | ||||||||||||||||||
| Löslichkeit |
1400 g·l−1 in Wasser[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Zulassungsverfahren unter REACH |
besonders besorgniserregend: krebserzeugend, erbgutverändernd, fortpflanzungsgefährdend (CMR), ernsthafte Auswirkungen auf die menschliche Gesundheit gelten als wahrscheinlich[4] | ||||||||||||||||||
| MAK |
aufgehoben, da cancerogen[1] | ||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Wasserfreies Cadmiumchlorid kann durch Reaktion von erhitztem Cadmium mit Chlorgas gewonnen werden.
Auch durch das Auflösen von Cadmium oder Cadmiumcarbonat in Salzsäure und Auskristallisieren lässt sich Cadmiumchlorid gewinnen. Dabei entsteht ein Cadmiumchlorid-Hydrat, das mit Thionylchlorid entwässert werden kann.[5]
Ebenfalls möglich ist die Darstellung durch Reaktion von Cadmium mit Chlorwasserstoff bei 450 °C[6]
oder einer Lösung von Cadmiumacetat in wasserfreier Essigsäure (oder deren Gemisch mit Essigsäureanhydrid) mit Acetylchlorid.[6]
Eigenschaften
Cadmiumchlorid bildet farblose, hygroskopische und sehr gut wasserlösliche Kristalle. Es kristallisiert in einer Schichtstruktur im trigonalen Kristallsystem in der Raumgruppe R3m (Raumgruppen-Nr. 166) mit den Gitterparametern a = 3,85 Å und c = 17,46 Å.[7] Diese Struktur besteht aus einer kubisch-dichtesten Packung von Chloridanionen, in denen sich die Cadmiumkationen in die Oktaederlücken jeder zweiten Schicht einordnen (Schichtfolge ABCABC, Koordinationstyp = 6:3). Damit sind die Cadmiumionen oktaedrisch von sechs Chloridionen umgeben. Jedes Chloridion bildet die Spitze einer trigonalen Pyramide mit drei Cadmiumionen als Grundfläche. Die CdCl2-Struktur dient häufig als Referenzstruktur. In dieser Struktur kristallisieren vor allem Übergangsmetallchloride wie Mangan(II)-chlorid, Eisen(II)-chlorid oder Zinkchlorid, aber auch Magnesiumchlorid, Zinkbromid und Nickel(II)-iodid.[8]
Verwendung
Cadmiumchloridlösungen adsorbieren Schwefelwasserstoff. Es wird außerdem in der Galvanotechnik, Mikroskopie, Photographie und als Ausgangsmaterial für die Herstellung von Cadmiumpigmenten genutzt.[9]
Cadmiumchlorid wirkt als Katalysator in Biginelli-Reaktionen für die Herstellung von 3,4-Dihydropyrimidin-2(1H)-onen.[10]
Sicherheitshinweise
Cadmiumchlorid ist eine sehr giftige und umweltgefährliche Substanz, die karzinogen, mutagen und reproduktionstoxisch wirken kann. Die Substanz ist in einatembarer Form nach Anhang II, Nr. 6 der deutschen Gefahrstoffverordnung (GefStoffV) als besonders gefährlicher krebserzeugender Stoff eingestuft und darf nur in geschlossenen Anlagen hergestellt oder verwendet werden.[11] Eine akut toxische Wirkung besteht in einer starken Reizwirkung auf den Respirationstrakt nach dem Einatmen von Dämpfen oder Aerosolen bis zum Lungenödem. Eine chronische Vergiftung führt zur Schädigung von Nieren, Leber und Lungen. Optisches Merkmal einer Cadmiumvergiftung ist die Ausbildung eines gelben Saums an den Zahnhälsen durch sulfidische Cadmiumverbindungen. Für Ratten wird eine LD50 von 88 mg/kg (oral, wasserfreies Cadmiumchlorid) angegeben. Darüber hinaus ist es extrem giftig für viele Wasserorganismen (Bakterien, Algen, Krustentiere).[3]
Einzelnachweise
- Datenblatt Cadmiumchlorid bei AlfaAesar, abgerufen am 29. August 2010 (PDF) (JavaScript erforderlich)..
- Eintrag zu Cadmium chloride im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag zu Cadmiumchlorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- Eintrag in der SVHC-Liste der Europäischen Chemikalienagentur, abgerufen am 16. Juli 2014.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1490.
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 1040.
- D.E. Partin, M. O'Keeffe: The Structures and Crystal Chemistry of Magnesium Chloride and Cadmium Chloride. In: Journal of Solid State Chemistry. 1991, 95, S. 176–183, doi:10.1016/0022-4596(91)90387-W.
- Erwin Riedel, Christoph Janiak: Anorganische Chemie. 7. Auflage. 2007, de Gruyter, ISBN 978-3-11-018903-2, S. 138.
- Cadmiumchlorid. In: Römpp Chemie-Lexikon. Thieme Verlag, Stand März 2002.
- A. Venkat Narsaiah, A. K. Basak, K. Nagaiah: Cadmium Chloride: An Efficient Catalyst for One-Pot Synthesis of 3,4-Dihydropyrimidin-2(1H)-ones. In: Synthesis. 2004, 8, S. 1253–1256, doi:10.1055/s-2004-822383.
- Gefahrstoffverordnung (GefStoffV) – Stand: April 2017.


