Wolfram(IV)-sulfid
Wolfram(IV)-sulfid ist eine chemische Verbindung aus der Gruppe der Wolframverbindungen und Sulfide.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
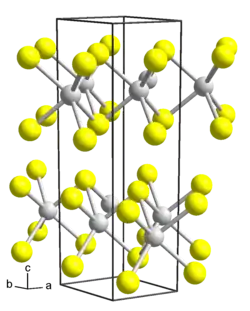 | ||||||||||||||||
| _ W4+ _ S2− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Wolfram(IV)-sulfid | |||||||||||||||
| Verhältnisformel | WS2 | |||||||||||||||
| Kurzbeschreibung |
grau-bläulicher geruchloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 247,97 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
7,5 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Wolfram(IV)-sulfid kann direkt aus den Elementen
oder durch Reaktion von Wolfram(VI)-oxid mit Schwefel gewonnen werden.[3]
Eigenschaften
Wolfram(IV)-sulfid ist ein grau-bläulicher bis schwarzer geruchloser Feststoff, welcher schwer löslich in Wasser ist.[1] Es besitzt eine hexagonale Kristallstruktur mit der Raumgruppe P63/mmc (Raumgruppen-Nr. 194) (a = 3,132, c = 12,323 Å). Eine trigonale Form (Raumgruppe R3m (Nr. 160), a = 3,158, c= 18,49 Å) ist ebenfalls bekannt[4]. Es besitzt Katalysator- und Detektoreigenschaften.[3]
Einzelnachweise
- Eintrag zu Wolframdisulfid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. Februar 2017. (JavaScript erforderlich)
- Mindat: Tungstenit
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 1574.
- Eintrag Tungstenit im Handbook of Mineralogy.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. The authors of the article are listed here. Additional terms may apply for the media files, click on images to show image meta data.
