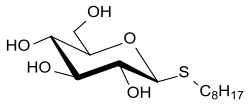
n-Octyl-β-D-1-thioglucopyranosid
n-Octyl-β-D-1-thioglucopyranosid (Octylthioglucosid, OTG) ist ein Thioglucosid und ein mildes nichtionisches Tensid für die Solubilisierung von Proteinen, insbesondere von Membranproteinen.[3][4]
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | n-Octyl-β-D-1-thioglucopyranosid | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C14H28O5S | |||||||||||||||||||||
| Kurzbeschreibung |
weißer, kristalliner Feststoff[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 308,43 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Vorkommen und Darstellung
n-Alkyl-Thioglycoside vom Typ des n-Octyl-β-D-thioglucopyranosids haben keine natürlich vorkommende Vertreter. Als natürliche S-Glycoside verbreitet sind hingegen die Senfölglycoside.
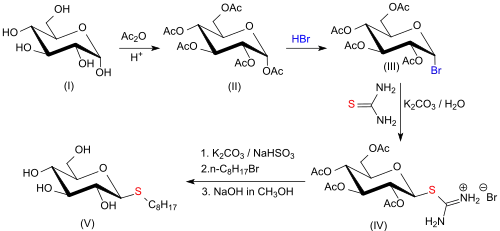
Die Synthese von n-Octyl-β-D-thioglucopyranosid[5] geht aus von D-Glucose (I), die mit Acetanhydrid und konzentrierter Schwefelsäure zum α-D-Glucopyranose-pentaacetat (Pentaacetylglucose) (II)[6] peracetyliert wird.
Pentaacetylglucose reagiert mit Bromwasserstoff zu 2,3,4,6-Tetra-O-acetyl-α-D-glucopyranosylbromid (Acetobromglucose) (III)[7], die mit Thioharnstoff in Aceton fast quantitativ das Isothiuroniumsalz 2,3,4,6-Tetra-O-acetyl-β-D-glucopyranosyl-1-isothiuroniumbromid (IV) bildet.
Das nach Neutralisation des Salzes und Reduktion mit Natriumsulfit zum Thiol im Alkalischen entstehende nukleophilere Thiolat-Anion reagiert ebenfalls fast quantitativ mit 1-Bromoctan zum n-Octyl-2,3,4,6-tetra-O-acetyl-1-thio-β-D-glucopyranosid (peracetyliertes Octylthioglucosid) (V), aus dem die alkalische Deacetylierung mittels Natriumhydroxid in Methanol quantitativ das Zielprodukt n-Octyl-1-thio-β-D-glucopyranosid (VI) in einer Gesamtausbeute von ca. 80 % erzeugt.
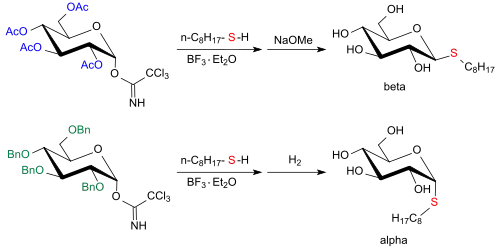
Bei der Trichloracetimidat-Methode nach Richard R. Schmidt bildet sich aus dem peracetylierten O-(α-D-Glucopyransyl)trichloracetimidat mit 1-Octanthiol unter Bortrifluoriddiethyletherat-Katalyse unter Inversion (Chemie) (nach Deacetylierung) ausschließlich das n-Octyl-1-thio-β-D-glucopyranosid, während das perbenzylierte O-(α-D-Glucopyransyl)trichloracetimidat unter Retention (Chemie) (nach Debenzylierung) ausschließlich in das n-Octyl-1-thio-α-D-glucopyranosid umgewandelt wird.[8]
Durch Reaktion von D-Glucose mit 1-Octanthiol mit Olah’s Reagens[9] (70 % Fluorwasserstoff HF in Pyridin) entsteht hingegen das anomere Gemisch n-Octyl-1-thio-α, β-D-glucopyranosid in 95%iger Ausbeute, das 44 % α-Anomeres und 56 % β-Anomeres enthält.[10]

Das reine α-Octylthioglucosid ist durch Reaktion von Pentaacetyl-β-D-glucose (aus D-Glucose, Acetanhydrid und Natriumacetat) in organischen Lösungsmitteln bei erhöhten Temperaturen mit 1-Octanthiol und Bortrifluorid-Etherat und anschließende Deacetylierung[11][12] zugänglich.

Eigenschaften
n-Octyl-β-D-1-thioglucopyranosid ist ein farb- und geruchloser, hygroskopischer, kristalliner Feststoff, der sich leicht in Wasser und niedrigen Alkoholen löst. Im Vergleich zu dem bereits früher als Detergens für biochemische Anwendungen eingeführten O-Glucosid n-Octyl-β-D-glucopyranosid, erscheint das analoge S-Glucosid OTG durch seine höhere Stabilität, besonders gegen Abbau durch β-Glucosidasen, besonders geeignet.
| Vergleich S-Octylglucosid mit O-Glucosid[3] | ||||||||||||
| Eigenschaften | Kritische Mizellkonzentration (CMC) | Solubilisierungsvermögen | Dialysierbarkeit | Chem. Stabilität | β-Glucosidase-Stabilität | Transparenz bei 280 nm | Denaturierungstendenz | Chem. Analytik | ||||
| n-Octyl-β-D-thiogluco-pyranosid | 9 mM (+) | ++ | + | + | + | + | + | + | ||||
| n-Octyl-β-D-gluco-pyranosid | 23–25 mM + | ++ | ++ | (−) | − | + | + | + | ||||
++ sehr gut + gut (+) eingeschränkt gut (−) schwach − schlecht
Der in Publikationen aus den 1980er Jahren vorgebrachte Kostenvorteil für Octylthioglucosid besteht wegen der in jüngerer Zeit entwickelten effizienten enzymatischen Synthesewege für O-Octylglucosid (direkt aus D-Glucose, 1-Octanol mittels β-Glucosidase)[13] offensichtlich nicht mehr.
Das α-anomere Octylthioglucosid zeigt flüssigkristalline Eigenschaften unter Ausbildung einer smektischen Phase A.[12]
Anwendungen
Nichtionische Detergentien solubilisieren Membranproteine schonend und unter (weitgehendem) Erhalt ihrer physiologischen Funktion durch Wechselwirkung mit den in die Lipiddoppelschichten von Zellmembranen eingebetteten hydrophoben Membranbereichen.[14] Oberhalb der so genannten kritischen Mizellkonzentration CMC [OTG: 9 mM, bzw. 0,2772 % (w/v)] bilden sich gemischte Mizellen aus Membranproteinen und Tensidmolekülen, wobei OTG-Konzentrationen von 1,1 – 1,2 % (w/v) für die Solubilisierung von Membranproteinen aus E. coli eingesetzt wurden.[4][5] Es wurde keine Denaturierung der Membranproteine nach Solubilisierung mit Octylthioglucosid gefunden.[3]
Für die Analyse der biologischen Aktivität von Membranproteinen ist es oft erforderlich, die Proteine in die Lipiddoppelschichten von Liposomen zu rekonstituieren. Dabei wird die Lösung des solubilisierten Proteins in Gegenwart von Phospholipiden oder Membranlipidmischungen zur Entfernung des Tensids der Dialyse oder Ionenaustauschchromatographie unterworfen. So kann unter Standardbedingungen nach 6 Stunden 95 % des OTG aus einer 43 mM-Tensidlösung entfernt werden.[4]
Octylthioglucosid (15 mM) ist seinem O-Analogon Octylglucosid (OT) deutlich überlegen bei der Solubilisierung und der Stabilisierung gegenüber thermischer und lichtinduzierter Denaturierung der lichtgetriebenen Protonenpumpe Bacteriorhodopsin aus den Biomembranen von Halobakterien.[15]
Einzelnachweise
- Datenblatt Octyl-β-D-1-thioglucopyranoside ≥ 98.0 % bei Sigma-Aldrich, abgerufen am 25. Februar 2017 (PDF).
- Datenblatt n-Octyl-beta-D-thioglucopyranoside, 98.0 % bei AlfaAesar, abgerufen am 25. Februar 2017 (PDF) (JavaScript erforderlich).
- T. Tsuchiya, S. Saito: Use of n-Octyl-β-D-thioglucoside, a new nonionic detergent, for solubilization and reconstitution of membrane proteins. In: J. Biochem. Band 96, Nr. 5, 1984, S. 1593–1597, doi:10.1093/oxfordjournals.jbchem.a134989.
- S. Saito, T. Tsuchiya: Characteristics of n-octyl-β-D-thioglucopyranoside, a new nonionic detergent useful for membrane biochemistry. In: Biochem. J. Band 222, 1984, S. 829–832, doi:10.1042/bj.2220829.
- S. Saito, T. Tsuchiya: Synthesis of Alkyl-β-D-thioglucopyranoside, a series of new nonionic detergents. In: Chem. Pharm. Bull. Band 33, Nr. 2, 1985, S. 503–508, doi:10.1248/cbp.33.503.
- C.E. Redemann, C. Niemann: Acetobromoglucose [2,3,4,6-Tetraacetyl-α-d-glucopyranosyl bromide] In: Organic Syntheses. 22, 1942, S. 1, doi:10.15227/orgsyn.022.0001; Coll. Vol. 3, 1955, S. 11 (PDF).
- R.U. Lemieux: Methods in Carbohydrate Chemistry, Vol. 2, Reactions of Carbohydrates. Hrsg.: R.L. Whistler, M.L. Wolfrom, J.N. BeMiller. Academic Press Inc., New York 1963, S. 221–222.
- R.R. Schmidt, M. Stumpp: Glycosylimidate. 8. Synthese von 1-Thio-glycosiden. In: Liebigs Ann. Chem. Band 1983, Nr. 7, 1983, S. 1249–1256, doi:10.1002/jlac.198319830717.
- G.A. Olah, J.G. Shih, G.K.S. Prakash: Fluorine-containing reagents in organic synthesis. In: J. Fluorine Chem. Band 33, Nr. 1–4, 1986, S. 377–396, doi:10.1016/S0022-1139(00)85282-3.
- Patent US5118804: Process for preparing alkyl-1-thioglycosides and alkyl-glycosides, anomer mixtures thereof. Angemeldet am 31. Juli 1990, veröffentlicht am 2. Juni 1992, Anmelder: Beghin-Say, S.A., Erfinder: J. Defaye, A. Gadelle, C. Pedersen.
- Patent EP1041080B1: Process for the preparation of pentaacetyl-beta-D-glucopyranose. Angemeldet am 18. Februar 2000, veröffentlicht am 4. Oktober 2000, Anmelder: Nisshin Flour Milling Co., Ltd., Erfinder: M. Tsuji, H. Yamazaki.
- H.A. van Doren, R. van der Geest: Synthesis and liquid crystalline properties of the n-alkyl-1-thio-α-D-glucopyranosides, a new homologous series of carbohydrate mesogens. In: Carbohydrate Research. Band 194, 1989, S. 71–77, doi:10.1016/0008-6215(89)85007-4.
- A. Ducret, J.-F. Carrière, M. Trani, R. Lortie: Enzymatic synthesis of octyl glucoside by almond β-gluconidase in organic media. In: Can. J. Chem. Band 80, Nr. 6, 2002, S. 653–656, doi:10.1139/v02-081.
- OTG, 1-S-Octyl-β-D-Thioglucopyranoside (Octylthioglucose) 28351. (PDF; 44 kB) (Nicht mehr online verfügbar.) Pierce Chemical Co., Januar 1998, archiviert vom Original am 12. März 2017; abgerufen am 26. Februar 2017 (englisch). Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- A. Asada, M. Sonoyama: Solubilization and structural stability of bacteriorhodopsin with a mild nonionic detergent, n-octyl-β-thioglucoside. In: Biosc. Biotechnol. Biochem. Band 75, Nr. 2, 2011, S. 376–378, doi:10.1271/bbb.100726.