Jonone
Die Jonone (auch Ionone, Betonung auf der zweiten Silbe: Jonone) bilden eine Stoffgruppe, die die Einzelsubstanzen α-, β- und γ-Jonon umfasst und von Terpenen abgeleitet sind. Die Substanzen haben einen veilchenartigen Geruch und sind weit verbreitete Naturstoffe, die in vielen Pflanzen vorkommen.
Vorkommen
Alle drei Jononarten sind in Ölen diverser Pflanzen, insbesondere in Beeren, Tee und Tabak, gefunden worden. Veilchenöl enthält ca. 22 % α-Jonon, β-Jonon wird beispielsweise im Hennastrauch gefunden, die Tamarinde enthält γ-Jonon. β-Jonon ist ein Abbauprodukt von β-Carotin.
Vom α-Jonon werden beide Enantiomere [(R)-α-Jonon und (S)-α-Jonon] in der Natur gefunden.
Eine Übersicht über die Einzelsubstanzen und deren Eigenschaften gibt die folgende Tabelle.
| Jonone | ||||||
| Name | α-Jonon | β-Jonon | γ-Jonon | |||
| Strukturformel | -alpha-Ionon.svg.png.webp) (R)-α-Jonon -alpha-Ionon.svg.png.webp) (S)-α-Jonon |
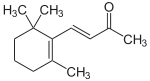 β-Jonon |
-gamma-Ionon.svg.png.webp) (R)-γ-Jonon -gamma-Ionon.svg.png.webp) (S)-γ-Jonon | |||
| Andere Namen |
|
|
| |||
| MIXED IONONES (INCI)[1] | ||||||
| CAS-Nummer | 127-41-3 (rac) 24190-29-2 (R) 14398-36-8 (S) | 79-77-6 | 24190-32-7 | |||
| 8013-90-9 (Gemisch) | ||||||
| PubChem | 5282108 | 638014 | 5363741 | |||
| Summenformel | C13H20O | |||||
| Molare Masse | 192,30 g·mol−1 | |||||
| Aggregatzustand | flüssig | |||||
| Kurzbeschreibung | farblose bis gelbliche, viskose Flüssigkeit (R)-Enantiomer: mit veilchenartigem, himbeerartigem, blumigem Geruch[2] |
farblose Flüssigkeit mit holzig-veilchenartigem Geruch[3] |
– | |||
| Dichte | 0,93 g·cm−3[4] | 0,95 g·cm−3[5] | – | |||
| Schmelzpunkt | – | −49 °C[5] | – | |||
| Siedepunkt | 237 °C[4] | 126–128 °C (16 hPa)[6] | – | |||
| Dampfdruck | 0,13 Pa (20 °C)[4] | – | – | |||
| Löslichkeit | sehr schlecht in Wasser[7] | – | ||||
| Optische Aktivität | [α]D23: +347° (D)[8] |
[α]D27: 0°[8] | – | |||
| Brechungsindex | 1,5016 (20 °C) (D)[8] |
1,5198 (20 °C)[8] | – | |||
| GHS- Kennzeichnung |
|
|
| |||
| H- und P-Sätze | 334 | 315 | siehe oben | |||
| keine EUH-Sätze | keine EUH-Sätze | siehe oben | ||||
| 261‐342+311 | keine P-Sätze | siehe oben | ||||
Gewinnung und Darstellung
Die Jonone können entweder aus entsprechenden Pflanzenölen gewonnen oder auch synthetisch hergestellt werden.

1893 wurde von Wilhelm Haarmann für die Firma Haarmann & Reimer ein Verfahren zu Synthese von α- und β-Jonon aus Citral entwickelt und patentiert. Danach wird Citral im basischen Milieu mit Aceton kondensiert. Hierbei entsteht Pseudojonon.

Dieses lässt sich beim Erwärmen mit verdünnter Säure zu einem Gemisch aus α- und β-Jonon cyclisieren.
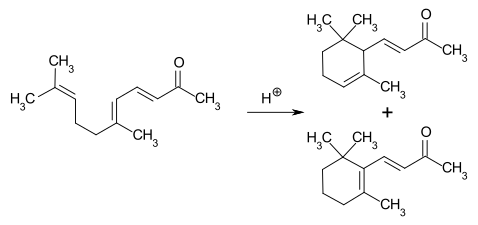
Je nach Reaktionsbedingungen ändert sich das Verhältnis von α- zu β-Jonon. Bei der Cyclisierung mit Phosphorsäure entsteht hauptsächlich α-Jonon, mit Schwefelsäure β-Jonon.
Durch die Umsetzung von Pseudojonon mit Bortrifluorid und konzentrierter Essigsäure lässt sich mit hoher Ausbeute reines β-Jonon herstellen.
Durch Ultraviolettstrahlung lässt sich die normalerweise in der trans-Konfiguration vorliegende Doppelbindung der Seitenkette in die cis-Konfiguration überführen.
Verwendung
Jonon wird in großen Mengen in der Riechstoffindustrie, zumeist in Blumen- oder Phantasie-Kompositionen, eingesetzt. Je nach Anwendungsbereich werden hier Isomerengemische oder einzelne Isomere, welche sich alle im Duft unterscheiden, verwendet. Auch für die Herstellung von Aromen werden im geringeren Umfang Jonone eingesetzt.
Auch dienen sie zur Herstellung der in der Parfümerie wichtigen Damascenonen und Isomethyljononen (α-Isomethylionon).
β-Jonon ist außerdem eine wichtige Ausgangssubstanz für die Produktion von Retinol und Carotinen.
Biologische Bedeutung
Jonone können vom Menschen noch in sehr geringen Konzentrationen gerochen werden. Für β-Jonon liegt die Geruchsschwelle bei 10−7 mg pro Liter Luft oder 0,1 ppb, für (R)-γ-Jonon bei 11 ppb und bei (S)-γ-Jonon 0,07 ppb.[11]
Sicherheitshinweise
Der LD50-Wert (Ratte, oral) liegt für α-Jonon bei 4590 mg·kg−1, für β-Jonon bei 2920 mg·kg−1.
Jonone besitzen ein allergenes Potential und sollten deshalb wenn möglich mit Handschuhen gehandhabt werden.
α-Jonon ist außerdem in der Wassergefährdungsklasse 2 (wassergefährdend) eingeteilt.
Einzelnachweise
- Eintrag zu MIXED IONONES in der CosIng-Datenbank der EU-Kommission, abgerufen am 13. November 2021.
- Bernd Schäfer: Naturstoffe in der chemischen Industrie. Spektrum Akademischer Verlag, 2007, ISBN 978-3-8274-1614-8, S. 73.
- Eintrag zu Jonone. In: Römpp Online. Georg Thieme Verlag, abgerufen am 25. Mai 2014.
- Datenblatt α-Jonon (PDF) bei Merck, abgerufen am 20. Februar 2010.
- Datenblatt β-Jonon (PDF) bei Carl Roth, abgerufen am 20. Februar 2010.
- Datenblatt β-Jonon bei Sigma-Aldrich, abgerufen am 20. Februar 2010 (PDF).
- Datenblatt Jonone bei Acros, abgerufen am 20. Februar 2010.
- CRC Handbook of Chemistry and Physics, 60th Edition, CRC Press, 1980.
- Datenblatt a-Ionone bei Sigma-Aldrich, abgerufen am 3. Mai 2011 (PDF).
- Bernd Schäfer: Naturstoffe in der chemischen Industrie. Spektrum Akademischer Verlag, 2007, ISBN 978-3-8274-1614-8, S. 64–65.
- Elisabetta Brenna, Claudio Fuganti, Stefano Serra, Philip Kraft: Optically Active Ionones and Derivatives: Preparation and Olfactory Properties. In: Eur. J. Org. Chem. 2002, S. 967–978.
Literatur
- Dieter Martinetz, Roland Hartwig: Taschenbuch der Riechstoffe. 1. Auflage. Verlag Harri Deutsch, Frankfurt am Main 1998, ISBN 3-8171-1539-3.
- Eberhard Breitmaier: Terpene. (= Teubner Studienbücher). 1. Auflage. Stuttgart u. a. 1999, ISBN 3-519-03548-0.
- Eintrag zu Jonone. In: Römpp Online. Georg Thieme Verlag, abgerufen am 25. Mai 2014.
- Hans Beyer, Wolfgang Walter, Wittko Francke: Lehrbuch der Organischen Chemie. 23. Auflage. S. Hirzel Verlag, Stuttgart/ Leipzig 1998, ISBN 3-7776-0808-4.

