Artemisinin
Artemisinin ist ein sekundärer Pflanzenstoff aus der chemischen Gruppe der Sesquiterpene, der in den Blättern und Blüten des Einjährigen Beifußes (Artemisia annua) vorkommt. Charakteristika der Artemisininstruktur sind ein Trioxanringsystem und eine Peroxidbrücke. Halbsynthetisch hergestellte Abkömmlinge des Artemisinins werden in Form von Kombinationstherapien weltweit zur Behandlung von Infektionen mit multiresistenten Stämmen von Plasmodium falciparum, dem Erreger der Malaria tropica, eingesetzt.[5] Die Verwendung pflanzlicher Artemisia-Präparate (z. B. in Form von Tees) zur Vorbeugung oder Behandlung von Malaria ist gemäß einer Stellungnahme der WHO nicht empfehlenswert.[6]
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
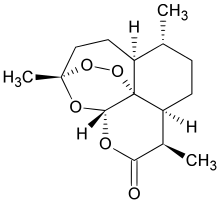 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Artemisinin | |||||||||||||||||||||
| Andere Namen |
(3R,5aS,6R,8aS,9R,12S,12aR)-Octahydro-3,6,9-trimethyl-3,12-epoxy-12H-pyrano[4,3-j]-1,2-benzodioxepin-10(3H)-on | |||||||||||||||||||||
| Summenformel | C15H22O5 | |||||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
P01BE01 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 282,34 g·mol−1 | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
| |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Gewinnung

Der Einjährige Beifuß, aus dem Artemisinin gewonnen wird, wird in China, Vietnam und in ostafrikanischen Ländern angebaut. Die Gewinnung erfolgt durch die Extraktion getrockneter Blätter und Blüten mit n-Hexan, worin der Wirkstoff, der überwiegend in den ätherischen Öldrüsenschuppen lokalisiert ist, gut löslich ist. Alternative Lösungsmittel wurden ebenfalls evaluiert, um das n-Hexan zu ersetzen, haben aber bisher noch keine praktische Anwendung gefunden.[7] Auf einer Anbaufläche von einem Hektar lassen sich bis zu zwei Tonnen Blattmaterial ernten, die zwei bis drei Kilogramm des Extraktes liefern. Der Artemisiningehalt in der Wildtyp-Pflanze liegt zwischen 0,1 und 0,4 % bezogen auf das Trockengewicht. Züchtungen mit einem Wirkstoffgehalt bis zu 1,4 % sind bekannt. Aus dem eingedampften Rohextrakt, einem gelben, viskosen Öl, wird Artemisinin durch Umkristallisation gewonnen. Dieses Verfahren ist relativ teuer und folglich der Preis für Artemisinin sehr hoch.
Großtechnische Herstellung
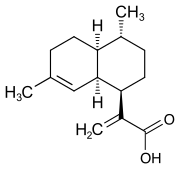
Peter Seeberger und François Lévesque stellten Anfang 2012 ein neues, sehr einfaches Verfahren zur Gewinnung von Artemisinin aus Artemisininsäure vor.[8] Artemisininsäure lässt sich in größeren Mengen aus dem Einjährigen Beifuß gewinnen als Artemisinin. Im Jahr 2013 veröffentlichten Paddon und Mitarbeiter einen Prozess zur kostengünstigen Herstellung von Artemisininsäure mithilfe von genmanipulierter Bierhefe (Saccharomyces cerevisiae), der nicht durch Patente belastet ist.[9]
Seit April 2013 ist im norditalienischen Garessio eine Anlage der Firma Sanofi in Betrieb, die pro Jahr bis zu 40 Tonnen Artemisinin herstellen soll. Die Anlage ist Resultat eines Projektes der Bill-und-Melinda-Gates-Stiftung, der Organisation One World Health (jetzt Path) und weiterer Partner, das seit 2004 lief. Artemisinin wird halbsynthetisch durch photochemische Oxidation aus fermentativ produzierter Artemisininsäure dargestellt. Die Anlage arbeitet in einem semi-kontinuierlichen Verfahren. Die Tonnage der Anlage soll auf 60 Tonnen pro Jahr erhöht werden. 10 bis 15 Prozent der produzierten Menge Artemisinin werden direkt verkauft, der Rest wird zum Wirkstoff Artesunat (AS) umgesetzt, der in fixer Kombination zusammen mit Amodiaquin (AQ), ebenfalls ein Antimalariawirkstoff, im Malariatherapeutikum ASAQ eingesetzt wird.[10] Allerdings wurde in der Anlage, die auf gentechnisch veränderter Hefe basiert, im Jahr 2015 keinerlei Artemisinin hergestellt. Zudem wolle Sanofi die Anlage verkaufen, berichtete Nature im Februar 2016. Gründe seien der niedrige Preis für natürliches Artemisinin und die mangelnde Nachfrage von Herstellern von Malaria-Medikamenten.[11]
Eigenschaften
Die Verbindung kann in zwei polymorphen Formen auftreten. Das Polymorph I schmilzt bei 151,4 °C mit einer Schmelzwärme von 78,4 J·g−1, das Polymorph II bei 153,9 °C mit 70,5 J·g−1.[2] Beide Formen stehen enantiotrop zueinander. Bei 130 °C kann mittels Röntgenpulverdiffraktometrie und DSC ein Festphasenübergang von Polymorph I zu Polymorph II beobachtet werden.[2] Das Polymorph I kristallisiert in einem orthorhombischen Kristallgitter mit der Raumgruppe P212121 (Raumgruppen-Nr. 19), Polymorph II in einem triklinen Kristallgitter mit der Raumgruppe P1 (Raumgruppen-Nr. 1).[12]
Analytik
Zur zuverlässigen qualitativen und quantitativen Bestimmung von Artemisinin wird die Kopplung der HPLC mit der Massenspektrometrie nach geeigneter Probenvorbereitung eingesetzt.[13]
Einsatz als Medikament
Wirkungsweise
Artemisinin besitzt eine Peroxidstruktur, die für die Wirkung gegen Malaria ausschlaggebend ist.[14] Bei hoher Konzentration an Eisenionen wird dieses Peroxid instabil und zerfällt in freie Radikale. Solche hohen Konzentrationen werden in Erythrozyten, aber auch in Plasmodien gefunden, die Eisen akkumulieren. Gelangt Artemisinin in mit Plasmodien infizierte Erythrozyten, zerstören die gebildeten Radikale möglicherweise den Parasiten. Jedoch gibt es Hinweise, dass Artemisinin-Derivate spezifischer wirken, indem sie beispielsweise pfATP6, eine Ca-ATPase, hemmen.
Derivate
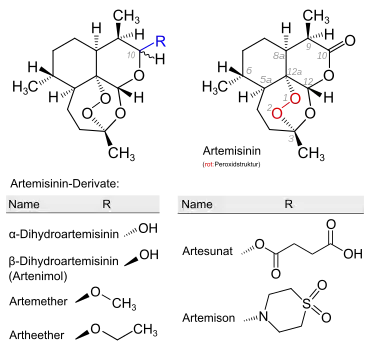
Auf der Suche nach wirkungsvolleren Derivaten wurde erkannt, dass die Peroxidgruppe Artemisinins erhalten bleiben muss. Nach Reaktion mit Natriumborhydrid wurde zunächst Dihydroartemisinin erzeugt, was Grundlage verschiedener öl- und wasserlöslicher Derivate ist.[14] Diese partialsynthetischen Derivate sind beispielsweise Artemether, Artesunat und Artemotil. Ihre Aktivität nimmt nach der Resorption allerdings schnell ab, was auf eine rasche Metabolisierung zurückgeführt wird. Um dieses Problem zu lösen, wird zusätzlich eine Komedikation gegeben:[14]
- Artemether wird zusammen mit Lumefantrin eingesetzt, das die Metabolisierung hemmt und gleichzeitig einen antiplasmodialen Effekt aufweist.[15] Die Halbwertszeit des Lumefantrins beträgt drei bis sechs Tage.
- Bei Artesunat gibt es folgende Kombinationstherapien: Artesunat/Mefloquin, Artesunat/Amodiaquin und Artesunat/Sulfadoxin/Pyrimethamin.
- Piperaquin kommt als Komedikation bei Dihydroartemisinin zur Verwendung.
Diese Kombinationstherapien werden mit ACT für Artemisinin-based combination therapy („Artemisinin-basierte Kombinationstherapie“) abgekürzt.[5]
Entwicklung von Resistenzen
In den Jahren 2008 und 2009 wurden Anzeichen für die Entwicklung von Resistenzen gegenüber Kombinationstherapien mit Artesunat in Pailin (Westkambodscha),[16][17] unabhängige Resistenzentwicklungen gegenüber Plasmodium falciparum 2012 in Westthailand beschrieben.[18]
Inzwischen breiten sich Resistenzen in Südostasien und China aus, bis 2016 wurden keine Resistenzen außerhalb dieses Bereichs gefunden. Die Mutationen konzentrieren sich um zwei geografische Foci, einer im Grenzgebiet zwischen Myanmar, Südchina und den westlichen Grenzregionen Thailands, der andere in Kambodscha, Laos und Vietnam. Dabei zeigen sich Mutationen im Plasmodium-Gen der β-Propeller-Domäne des Kelch-Proteins K13, das für ein hoch konserviertes Protein (PfKelch13) kodiert.[19] Bisher wurden 13 Mutationen identifiziert, die mit einer verminderten Parasiten-Clearance verbunden sind. Aus der häufigsten Mutation, einem Einzelnukleotid-Polymorphismus (C580Y), resultiert in einer Fehlfaltung und damit in eine verminderte Bindung der Phosphoinositid-3-Kinasen.[20] Andere, nicht auf C580Y-basierende Resistenzen bei PfKelch13 verbreiten sich auch in Südamerika und Neuguinea aus, in Ruanda die Mutation R561H.[21]
Durch die C580Y-Mutation in PfKelch13 verzögert sich die Entwicklung von P. falciparum, da sie Hämoglobin schlechter aufnehmen können.[21][22] Sie bleiben dadurch länger in einem früheren Entwicklungsstadium, bei dem Artesunat seine Wirkung nicht entfalten kann. Dies verschafft dem Parasiten die nötige Zeit, hohe Spiegel des (kurzlebigen) Antimalariemittels zu überstehen.
Basierend auf einer Überprüfung der Studienlage zur Wirksamkeit sieht die WHO die Anwendung von Tee oder anderen Zubereitungen aus der Artemisia-Pflanze („Hausmittel“) sehr kritisch. Sie erklärte 2019 in einer Stellungnahme, die Verwendung von Artemisia-Pflanzenmaterial zur Prävention oder Behandlung von Malaria weder zu unterstützen noch zu fördern,[6] unter anderem da:[23]
- der Gehalt von Artemisinin in Pflanzen sehr stark variiert;
- er häufig zu niedrig ist, um alle Parasiten zu töten oder ein Wiederauftreten zu verhindern;
- eine weit verbreitete Anwendung mit diesen ungenügenden Wirkkonzentrationen rascher Resistenzen fördert und
- es wirksamere Therapien gegen Malaria gibt.
Geschichte
Die chinesische Wissenschaftlerin Tu Youyou isolierte Artemisinin in den frühen 1970er Jahren und zeigte in den folgenden Jahrzehnten seine Wirksamkeit gegen Malaria auf.[24][25] Ausgangspunkt war die zunehmende Resistenzbildung der damals eingesetzten Therapeutika wie z. B. 1934 eingeführte und ab den 1950er Jahren stark eingesetzte Chloroquin.[14] Dies wirkte sich auch auf den Vietnamkrieg aus: Die damalige nordvietnamesische Regierung forderte Hilfe aus China an, da Malaria die Leistungsfähigkeit ihres Militärs beeinflusste.

1967 startete China daraufhin mit der geheimen Initiative „Projekt 523“,[26] die zum Ziel hatte, neue Medikamente gegen Malaria zu entdecken.[14] Hierbei wurden antike medizinische Texte und Rezepte aus diversen Pflanzen untersucht. Tatsächlich wurde der Einjähriger Beifuß mehrfach erwähnt. Zwar zeigten erste Extrakte eine Wirkung gegen Malaria, die Wirkstärke war jedoch sehr unterschiedlich und nicht reproduzierbar. Bei einem Rezept des chinesischen Alchemisten Ge Hong[27] (341 v. Chr.) wurden mit kaltem Wasser hergestellte Säfte beschrieben – im Gegensatz zu einer klassischen Zubereitung mit heißem Wasser (z. B. als Tee). Youyou erkannte dies und merkte an, dass die Blätter die höchste Wirkung entfalten. Daraufhin wurden Extrakte bei niedriger Temperatur mittels Ether gewonnen, die höchst effektiv gegen Malaria im Tiermodell wirkten. Durch intensive Forschung wurde 1972 schließlich Artemisinin („qinghaosu“) als Antimalaria-spezifische Komponente identifiziert und isoliert.[27] Die Stereochemie des Sesquiterpens wurde 1975 am Institut für Biophysik der Chinesischen Akademie der Wissenschaften mit Sitz in Peking bestimmt und erstmals 1977 veröffentlicht.[27]
Youyou wurde 2011 mit dem Albert Lasker Award for Clinical Medical Research[28] und 2015 mit dem Nobelpreis für Physiologie oder Medizin[29] ausgezeichnet.
Literatur
- Sanjeev Krishna et al.: Artemisinins: their growing importance in medicine. In: Trends in Pharmacological Sciences. Band 29, 2008, S. 520–527, doi:10.1016/j.tips.2008.07.004, PMC 2758403 (freier Volltext).
- Bernd Schäfer: Artemisinin. Teil 1 und Teil 2, In: Chemie in unserer Zeit. Band 48, Heft 2, April 2014, S. 134–145, doi:10.1002/ciuz.201400645 und Band 48, Heft 3, Juni 2014, S. 216–225, doi:10.1002/ciuz.201400652.
Weblinks
- Design und Synthese von Antimalaria Endoperoxiden
- Rolf Bökemeier: Ein Kraut wirkt Wunder. In: Geo. 2006.
- Malaria parasites 'resist drugs'. In: BBC News. 29. Mai 2009 (englisch).
Einzelnachweise
- Datenblatt Artemisinin (PDF) bei Carl Roth, abgerufen am 8. Februar 2013.
- E. Horosanskaia, A. Seidel-Morgenstern, H. Lorenz: Investigation of drug polymorphism: Case of artemisinin. In: Thermochim. Acta. 578, 2014, S. 74–81, doi:10.1016/j.tca.2013.12.019.
- Yan Liu, Huisheng Lü, Fei Pang: Solubility of Artemisinin in Seven Different Pure Solvents from (283.15 to 323.15) K. In: Journal of Chemical & Engineering Data. Band 54, Nr. 3, 2009, S. 762–764, doi:10.1021/je800515w.
- Artemisinin, The International Pharmacopoeia, 10th Edition, 2020. Abgerufen am 1. März 2022.
- WHO Guidelines for malaria. In: WHO. 13. Juli 2021, abgerufen am 18. Oktober 2021 (englisch).
- The use of non-pharmaceutical forms of Artemisia. In: WHO. 10. Oktober 2019, abgerufen am 18. Oktober 2021 (englisch).
- Alexei A. Lapkin et al.: Screening of new solvents for artemisinin extraction process using ab initio methodology. In: Green Chemistry. Band 12, Nr. 2, 1. Januar 2010, S. 241, doi:10.1039/b922001a. und darin zitierte Literatur.
- F. Lévesque, P.H. Seeberger: Continuous-Flow Synthesis of the Anti-Malaria Drug Artemisinin. In: Angewandte Chemie, International Edition. Band 51, Nr. 7, 2012, S. 1706−1709.
- C. J. Paddon, P. J. Westfall u. a.: High-level semi-synthetic production of the potent antimalarial artemisinin. In: Nature. 496, 2013, S. 528–532, doi:10.1038/nature12051.
- Brigitte Osterath: Im Tonnenmaßstab gegen Malaria. In: Nachrichten aus der Chemie. Februar 2014, S. 125–127.
- Synthetic biology’s first malaria drug meets market resistance. In: Nature News & Comment. Abgerufen am 5. April 2016.
- K. I. Chan: Polymorphism of artemisinin from Artemisia annua. In: Phytochem. 46, 1997, S. 1209–1214, doi:10.1016/S0031-9422(97)80013-1.
- Qing Min et al.: [Simultaneous quantitation of artemisinin, arteannuin B, artemisic acid, and scopoletin in mice plasma by HPLC-MS]. In: Zhongguo Zhong Yao Za Zhi = Zhongguo Zhongyao Zazhi = China Journal of Chinese Materia Medica. Band 39, Nr. 17, September 2014, S. 3306–3310, PMID 25522617.
- The use of nonpharmaceutical forms of Artemisia. (PDF) In: WHO. Global Malaria Programme, 2019, abgerufen am 18. Oktober 2021 (englisch).
- Pauline Byakika-Kibwika et al.: Update on the efficacy, effectiveness and safety of artemether-lumefantrine combination therapy for treatment of uncomplicated malaria. In: Therapeutics and Clinical Risk Management. Band 6, 2. Februar 2010, S. 11–20, PMID 20169032, PMC 2817784 (freier Volltext).
- Harald Noedl et al.: Evidence of artemisinin-resistant malaria in western Cambodia. In: The New England Journal of Medicine. Band 359, Nr. 24, 11. Dezember 2008, S. 2619–2620, doi:10.1056/NEJMc0805011, PMID 19064625.
- Arjen M. Dondorp et al.: Artemisinin resistance in Plasmodium falciparum malaria. In: The New England Journal of Medicine. Band 361, Nr. 5, 30. Juli 2009, S. 455–467, doi:10.1056/NEJMoa0808859, PMID 19641202.
- Verena Ilona Carrara et al.: Changes in the treatment responses to artesunate-mefloquine on the northwestern border of Thailand during 13 years of continuous deployment. In: PloS One. Band 4, Nr. 2, 2009, S. e4551, doi:10.1371/journal.pone.0004551, PMID 19234601.
- Romain Coppée et al.: Comparative structural and evolutionary analyses predict functional sites in the artemisinin resistance malaria protein K13. In: Scientific Reports. Band 9, Nr. 1, 23. Juli 2019, S. 10675, doi:10.1038/s41598-019-47034-6.
- Johanna P. Daily: K13-Propeller Mutations and Malaria Resistance. In: New England Journal of Medicine. Band 374, Nr. 25, 23. Juni 2016, S. 2492–2493, doi:10.1056/NEJMe1604520.
- Robin Schumann et al.: Protein abundance and folding rather than the redox state of Kelch13 determine the artemisinin susceptibility of Plasmodium falciparum. In: Redox Biology. Band 48, 1. Dezember 2021, S. 102177, doi:10.1016/j.redox.2021.102177.
- Mechanismus für Unempfindlichkeit gegenüber wichtigem Malariamittel bei neuer Erreger-Variante entdeckt. In: Technische Universität Kaiserslautern. 29. November 2021, abgerufen am 12. Januar 2022.
- Iris Hinneburg: Artemisia-Tee: Ein Heilmittel gegen Malaria? In: Medizin transparent. 4. Oktober 2021, abgerufen am 18. Oktober 2021.
- W. Burns: East meets West: how China almost cured malaria. In: Endeavour. 32, 2008, S. 101–106, doi:10.1016/j.endeavour.2008.07.001.
- Nature News Blog: Protein folding and malaria meds take Laskers.
- Xin-zhuan Su, Louis H. Miller: The discovery of artemisinin and Nobel Prize in Physiology or Medicine. In: Science China. Life sciences. Band 58, Nr. 11, November 2015, S. 1175–1179, doi:10.1007/s11427-015-4948-7, PMID 26481135, PMC 4966551 (freier Volltext).
- Youyou Tu: The discovery of artemisinin (qinghaosu) and gifts from Chinese medicine. In: Nature Medicine. Band 17, Nr. 10, Oktober 2011, S. 1217–1220, doi:10.1038/nm.2471.
- Lasker Foundation: Lasker Clinical Medical Research Award – Tu Youyou.
- nobelprize.org: The Nobel Prize in Physiology or Medicine 2015.