Artesunat
Artesunat ist ein vom Artemisinin abgeleiteter halbsynthetischer Arzneistoff zur Behandlung der durch Plasmodium falciparum verursachten Malaria. Der Wirkstoff Artesunat wurde 2002 von der Weltgesundheitsorganisation (WHO) in die Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation aufgenommen.[4]
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
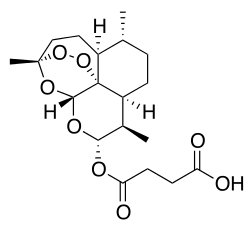 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Artesunat | |||||||||||||||||||||
| Andere Namen |
(3R,5aS,6R,8aS,9R,10S,12R,12aR)-decahydro-3,6,9-trimethyl-3,12-epoxy-12H-pyrano[4,3-j]-1,2-benzodioxepin-10-ol-hydrogensuccinat (IUPAC) | |||||||||||||||||||||
| Summenformel | C19H28O8 | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
P01BE03 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 384,421 g·mol−1 | |||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Pharmakologische Eigenschaften
Artesunat hat eine gegenüber Artemisinin deutlich verbesserte Bioverfügbarkeit. Wie alle Artemisinin-Derivate wirkt es über eine endogene Peroxidgruppe, die in infizierten Erythrozyten vermutlich für die Plasmodien toxische Radikale bildet. Problematisch ist die relativ kurze Halbwertszeit. Artesunat wird in der Leber durch das Enzym Cytochrom P450 3A4 metabolisiert.
Präparate und Verwendung
Der Schwerpunkt für die Anwendung von Artesunat ist die Behandlung der unkomplizierten Malaria tropica, insbesondere bei Plasmodien, die gegen andere Arzneistoffe wie Chloroquin resistent sind. Es wird dazu vorwiegend als Kombinationspräparat mit anderen Malariawirkstoffen eingesetzt. Eine fixe Kombination von Artesunat mit Amodiaquin (ASAQ) wurde in Zusammenarbeit zwischen der Drugs for neglected Diseases Initiative (DNDi) und Sanofi-aventis entwickelt und als Medikament in mehreren afrikanischen Ländern registriert.[5] Im Jahr 2013 hat Sanofi eigenen Angaben zufolge 80 Millionen Packungen dieses Präparates (Coarsucam bzw. ASAQ Winthrop) in Malaria-Endemiegebieten abgesetzt.[6] Eine Kombination von Artesunat mit Mefloquin stellt das Präparat Falcitrim dar.[7] Für die Kombination Artesunat/Pyronaridin (Pyramax) erstellte die Europäische Arzneimittelagentur (EMA) in Zusammenarbeit mit der Weltgesundheitsorganisation (WHO) 2012 ein wissenschaftliches Gutachten, das ausschließlich für Märkte außerhalb der Europäischen Union (EU) bestimmt ist. Staaten außerhalb der EU können sich bei der Genehmigung der Kombination auf das Gutachten stützen, welches auch den Präqualifikationsprozess der WHO erleichtert. Das Gutachten bestätigt eine Wirksamkeit von Artesunat/Pyronaridin, jedoch beschränken mögliche schwere Leberprobleme die Anwendung.[8]
Die Weltgesundheitsorganisation rät von der Monotheraphie der unkomplizierten Malaria mit Artemisinin-Abkömmlingen (wie etwa Artesunat) ab, um die Gefahr der Resistenzbildung zu vermindern.[9]
Bei der komplizierten Malaria (Falciparum Malaria) gilt jedoch die intravenöse Gabe von Artesunat als Mittel der Wahl und soll, falls verfügbar, der intravenösen Gabe von Chinin vorgezogen werden. Es ist in Deutschland nicht im Handel, kann jedoch über Importfirmen bezogen werden.[10] In der Europäischen Union ist Artesunat unter dem Namen Artesunate Amivas (Amivas) seit November 2021 zugelassen zur parenteralen, initialen Behandlung von schwerer Malaria bei Erwachsenen und Kindern,[11] in den USA hatte die Food and Drug Administration (FDA) die Zulassung im Mai 2020 erteilt.[12]
Herstellung
Artesunat wird durch Umsetzung von aus Artemisia annua gewonnenem Dihydroartemisinin mit Bernsteinsäureanhydrid im alkalischen Medium dargestellt. Reines Artesunat ist ein weißes, kristallines Pulver.[1]
Einzelnachweise
- Artesunate, The International Pharmacopoeia, 10th Edition, 2020. Abgerufena am 1. März 2022.
- Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von 4-oxo-4-{[(1R,4S,5R,8S,9R,10S,12R,13R)-1,5,9-trimethyl-11,14,15,16-tetraoxatetracyclo[10.3.1.0^{4,13}.0^{8,13}]hexadecan-10-yl]oxy}butanoic acid im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 17. Dezember 2019.
- Datenblatt Artesunat bei Sigma-Aldrich, abgerufen am 16. Februar 2020 (PDF).
- WHO Model List of Essential Medicines (PDF; 442 kB) abgerufen am 20. September 2012.
- ASAQ to treat malaria. (Memento vom 5. Mai 2012 im Internet Archive) DNDi.org
- Partnering to Promote Access to Healthcare, CSR Brochure 2014–2015, Sanofi, abgerufen am 1. März 2022 (PFD).
- Falcitrim, infarmed.pt.
- European Medicines Agency recommends new anti-malaria treatment for use outside the European Union, Europäische Arzneimittelagentur, 17. Februar 2012.
- WHO Guidelines for malaria. WHO, 18. Februar 2022.
- Leitlinie: Diagnostik und Therapie der Malaria, AWMF-Register-Nr. 042-001, Version Februar 2021 (PDF).
- Übersicht über Artesunat Amivas und warum es in der EU zugelassen ist. Europäische Arzneimittelagentur, 4. Januar 2022. Abgerufen am 1. März 2022.
- Drug Approval Package: ARTESUNATE, FDA. Abgerufen am 1. März 2022.