1-Butanol
1-Butanol (auch n-Butanol oder nach IUPAC Butan-1-ol) ist eine chemische Verbindung aus der Gruppe der Alkanole. Der primäre Alkohol leitet sich vom unverzweigten aliphatischen Kohlenwasserstoff Butan ab.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemeines | |||||||||||||||||||
| Name | 1-Butanol | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C4H10O | ||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit ethanolartigem Geruch[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 74,12 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
0,81 g·cm−3 (20 °C)[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
118 °C[2] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
beliebig mischbar mit organischen Lösungsmitteln, mäßig löslich in Wasser (77 g·l−1 bei 20 °C)[2] | ||||||||||||||||||
| Brechungsindex |
1,3988 (20 °C)[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK | |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Vorkommen
1-Butanol kommt von Natur aus in vielen Nahrungsmitteln vor und entsteht beim mikrobiologischen Abbau von Kohlenhydraten. Es entsteht auch im Zuge des Abbaus von Kohlenhydraten bei der Herstellung alkoholischer Getränke. Nachgewiesen wurde der Alkohol in Pflanzen, bzw. deren Früchten wie Bananen,[7] Cherimoya (Annona cherimola),[8] Noni (Morinda citrifolia),[8] Papaya ( Carica papay),[9] Weißen Maulbeeren (Morus alba),[9] Äpfeln ( Malus domestica)[8] und Melonen sowie verschiedenen Nahrungsmitteln wie Käse, erhitzter Milch und gekochtem Reis sowie bei der Popcornzubereitung, aber auch in der Muttermilch. Ältere quantitative Angaben aus den 1960er-Jahren über den Höchstgehalt von 1-Butanol in Lebensmitteln belaufen sich auf Werte von 12 mg/l in Getränken, 7 mg/kg in Speiseeis und 32 mg/kg in Backwaren.[10]
 Bananen
Bananen Noni-Frucht
Noni-Frucht Apfel
Apfel Käse
Käse Muttermilch
Muttermilch
Gewinnung und Darstellung
1-Butanol lässt sich auf mehreren Wegen herstellen. Industriell bedeutend ist die Hydroformylierung von Propen mit anschließender Hydrierung eines entstehenden Reaktionsproduktes (Butanal)[10]:
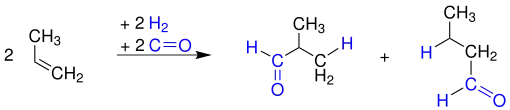
Propen reagiert mit Kohlenstoffmonoxid und Wasserstoff zu Butanal und 2-Methylpropanal.
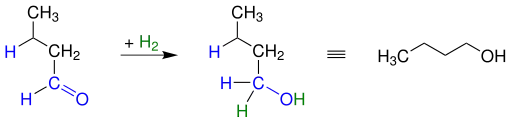
Das entstandene Butanal reagiert mit Wasserstoff weiter zu 1-Butanol.
Eine andere, auf nachwachsenden Rohstoffen basierende Möglichkeit zur Herstellung besteht in der Aceton-Butanol-Ethanol-Gärung von Zucker und Stärke mithilfe von Clostridium acetobutylicum. Solches biologisch hergestelltes 1-Butanol wird auch als Biobutanol bezeichnet.[10]
Eigenschaften
Physikalische Eigenschaften
1-Butanol ist eine farblose Flüssigkeit mit charakteristischem Geruch, der als „weinartig“ beschrieben wird, aber auch als „herb fuselähnlich mit Bananenaroma“ sowie als „süßlich ranzig“.[10] Man kann 1-Butanol mit allen gebräuchlichen Lösungsmitteln, wie zum Beispiel Ether, Glycol, Alkoholen, Ketonen und Aldehyden beliebig mischen. In Wasser ist 1-Butanol jedoch nur begrenzt lösbar.[11] Wasser löst sich in 1-Butanol etwas besser (ca. 20 Gewichts-%).[12]
Chemische Eigenschaften
Mögliche Reaktionen des 1-Butanols sind die Veresterung zu einem Ester, die Dehydrierung zu einem Aldehyd oder die Kondensation zu einem Ether:
Veresterung zu einem Ester:

1-Butanol und Propansäure reagieren unter Säurekatalyse (bspw. mit Schwefelsäure) zu Propionsäure-n-butylester und Wasser.
Dehydrierung zu einem Aldehyd:

1-Butanol reagiert unter Wasserstoffabspaltung zu Butanal.
Kondensation zu einem Ether:
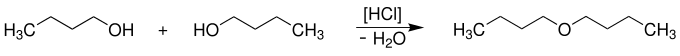
1-Butanol reagiert unter Säurekatalyse (bspw. mit Salzsäure) zu Di-n-butylether und Wasser.
Sicherheitstechnische Kenngrößen
1-Butanol gilt als entzündliche Flüssigkeit. Oberhalb des Flammpunktes können sich entzündliche Dampf-Luft-Gemische bilden. Die Verbindung hat einen Flammpunkt bei 35 °C.[2][13] Der Explosionsbereich liegt zwischen 1,4 Vol.‑% (43 g/m3) als untere Explosionsgrenze (UEG) und 11,3 Vol.‑% (350 g/m3) als obere Explosionsgrenze (OEG).[2][13] Der untere Explosionspunkt liegt bei 34 °C.[2][14] Der maximale Explosionsdruck liegt bei 8,4 bar.[13] Die Grenzspaltweite wurde mit 0,91 mm bestimmt.[2] Es resultiert damit eine Zuordnung in die Explosionsgruppe IIB.[2] Die Zündtemperatur beträgt 325 °C.[2][13] Der Stoff fällt somit in die Temperaturklasse T2.
Verwendung
Man verwendet 1-Butanol als Lösungsmittel bei der Herstellung von Lacken. Es verhindert das Weißanlaufen beim Trocknen der Lacke in feuchter Umgebung. Des Weiteren verwendet man 1-Butanol als Ausgangsstoff bei der Herstellung von Ethern und Estern (wie etwa Butylacetat und Glykolbutylethern und -estern sowie von Phthalaten und Acrylaten), die ihrerseits wieder als Lösungsmittel oder auch als Weichmacher dienen. Als Lösungsmittel für Farbstoffe, Zusatz in Polituren und Reinigungsmitteln, Komponente in Kraftstoffen, Laufmittel für die Dünnschicht- und Papierchromatographie, Extraktionsmittel bei der Gewinnung von Arzneistoffen oder als Ausgangsstoff für die Herstellung von Flotationschemikalien kann 1-Butanol auch verwendet werden.[15] Außerdem wird 1-Butanol zusammen mit den anderen Butanolen als Biokraftstoff der dritten Generation angesehen.[16] 1-Butanol findet darüber hinaus als Referenzmaterial in der Olfaktometrie Anwendung:[17] 123 µg 1-Butanol, wenn dieses in 1 m3 Neutralluft unter Normbedingungen verdampft wird, entsprechen einer Europäischen Geruchseinheit.[18] Außerdem dient 1-Butanol selbst als Lösungsmittel, vor allem in Farben, Lacken, Harzen und Farbentfernern sowie manchen Kosmetika und wird in der Oberflächenveredelung von Kleidung eingesetzt.[10]
Medizinische Verwendung
In den 1960er Jahren wurde 1-Butanol, als Hauptbestandteil des unter dem Handelsnamen „Haemostypiticum Revici“ insbesondere in der Zahnmedizin bekannt gewordenen Arzneimittels, zur Verkürzung der Blutungszeit eingesetzt, beispielsweise bei Nachblutungen nach Zahnentfernungen. Weitere Zusätze waren Citronensäure und Disaccharide. Nach Kuschinsky enthielt das Präparat manchmal Trillium, eine chemisch undefinierte Substanz (Trillium ist eine Gattung von Lilienpflanzen), die auch eine hämostyptische Aktivität haben soll. Emanuel Revici (1896–1997) wurde vor allem durch seine ineffektive Chemotherapie bei Krebserkrankungen bekannt. Mangels wissenschaftlicher Nachweise und der Gefahr, dass im Vertrauen auf die angegebene Wirksamkeit des „Haemostypiticums Revici“ weitere und nützliche Maßnahmen unterlassen werden, verschwand das Mittel in Europa in den 1980er Jahren aus dem Therapiespektrum, nachdem es jahrelang Verwendung gefunden hat. In den USA ist es noch als Revici Injection und Revici-e erhältlich.[19][20]
Sicherheitshinweise
1-Butanol kann beim Einatmen und Verschlucken gesundheitsschädlich wirken: Nieren- und Leberschädigungen, Schwindel, Kopfschmerzen, Benommenheit bis hin zur Bewusstlosigkeit und Hirnfunktionsstörungen können auftreten. Weiterhin kann es Atemwege, Verdauungswege, Augen und Haut reizen. Man sollte 1-Butanol deshalb nicht in die Hände von Kindern gelangen lassen.
Die Metabolisierung von 1-Butanol erfolgt tierexperimentellen und In-vitro-Daten zufolge in erster Linie durch Oxidation mittels Alkoholdehydrogenase (ADH) über Butanal und Butansäure in der Leber, in geringerem Maße auch durch hepatische Cytochrom-P450-Monoxygenasen, deren Aktivität durch Ethanol induzierbar ist. Eine Glucuronidierung oder Sulfatierung von 1-Butanol erfolgt nur in untergeordnetem Maß.[10]
1-Butanol wurde 2017 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Hierbei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von 1-Butanol waren die Besorgnisse bezüglich Verbraucherverwendung, Exposition von Arbeitnehmern, hoher (aggregierter) Tonnage und weit verbreiteter Verwendung sowie der möglichen Gefahr durch reproduktionstoxische Eigenschaften. Die Neubewertung fand ab 2017 statt und wurde von Ungarn durchgeführt. Anschließend wurde ein Abschlussbericht veröffentlicht.[21][22]
Weblinks
Einzelnachweise
- Eintrag zu N-BUTYL ALCOHOL in der CosIng-Datenbank der EU-Kommission, abgerufen am 28. Dezember 2019.
- Eintrag zu 1-Butanol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 97. Auflage. (Internet-Version: 2016), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-78.
- Eintrag zu Butan-1-ol im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte, abgerufen am 28. August 2019.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 97. Auflage. (Internet-Version: 2016), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-7.
- R. Tressl, F. Drawert, W. Heimann, R. Emberger: Notizen: Gasehromatographische Bestandsaufnahme von Bananen-Aromastoffen. In: Zeitschrift für Naturforschung B. 24, 1969, S. 781–783 (online).
- 1-BUTANOL (engl., PDF) In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 20. Juli 2021.
- N-BUTANOL (engl., PDF) In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 20. Juli 2021.
- Umweltbundesamt: Richtwerte für 1-Butanol in der Innenraumluft. In: Bundesgesundheitsblatt - Gesundheitsforschung - Gesundheitsschutz. 57, 2014, S. 733, doi:10.1007/s00103-014-1972-x.
- Datenblatt der BASF
- William Andrew: OSHA regulated hazardous substances: health, toxicity, economic, and technological data. S. 273 (eingeschränkte Vorschau in der Google-Buchsuche).
- E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen. Band 1: Brennbare Flüssigkeiten und Gase. Wirtschaftsverlag NW – Verlag für neue Wissenschaft, Bremerhaven 2003.
- E. Brandes, M. Mitu, D. Pawel: The lower explosion point — A good measure for explosion prevention: Experiment and calculation for pure compounds and some mixtures. In: J. Loss Prev. Proc. Ind. 20, 2007, S. 536–540, doi:10.1016/j.jlp.2007.04.028.
- Eintrag zu Butanole. In: Römpp Online. Georg Thieme Verlag, abgerufen am 12. November 2014.
- Jens Lubbadeh: Sprit aus Stroh: Mit Superhefe Treibstoff brauen. In: Spiegel Online. 18. August 2008.
- A. Ph. van Harreveld, Paul Heeres: Quality control and optimization of dynamic olfactometry using n-Butanol as a standard reference odorant. Staub – Reinhaltung der Luft, Band 55, 2, 1995, S. 45–50.
- DIN EN 13725:2003-07 Luftbeschaffenheit; Bestimmung der Geruchsstoffkonzentration mit dynamischer Olfaktometrie; Deutsche Fassung EN 13725:2003. Beuth Verlag, Berlin, S. 7.
- G. Kuschinsky, M. Lang, U. Wollert: Untersuchungen über die Wirkung von Butanol als Hämostyptikum. In: DMW - Deutsche Medizinische Wochenschrift. 93, 1968, S. 1443, doi:10.1055/s-0028-1110762.
- Verstraete M.Report on a preparation of butyl alcohol: Haemostypticum Revici®. In: Haemostatic Drugs. Springer, Dordrecht, 1977, Abgerufen am 27. August 2019.
- Europäische Chemikalienagentur (ECHA): Substance Evaluation Conclusion and Evaluation Report
- Community rolling action plan (CoRAP) der Europäischen Chemikalienagentur (ECHA): Butan-1-ol, abgerufen am 26. März 2019.


