Scrapie
Scrapie (von englisch scrape ‚kratzen‘, ‚schaben‘) oder Traberkrankheit (Paraplegia enzootica), seltener auch Gnubberkrankheit, Wetzkrankheit oder Rida, ist eine übertragbare, langsam tödlich verlaufende Erkrankung des Gehirns (Enzephalopathie) bei Schafen und in geringerem Ausmaß auch Ziegen. Sie wird höchstwahrscheinlich durch fehlgebildete Proteine (Prionen) hervorgerufen. Scrapie geht mit Hohlraumbildungen (Vakuolisierungen) in den Nervenzellen einher und äußert sich in Verhaltens- und Gangstörungen. Der englische Name rührt daher, dass die erkrankten Schafe infolge starken Juckreizes die Tendenz haben, sich die Wolle abzuscheuern. Sie gehört wie die Creutzfeldt-Jakob-Krankheit und Kuru des Menschen zu den übertragbaren (transmissiblen) spongiformen Enzephalopathien (TSE). Die Traberkrankheit ist wie alle TSE eine anzeigepflichtige Tierseuche. Der Übergang des Erregers auf das Rind wird als Ursache für das Auftreten der BSE angesehen. 2015 gab es in Deutschland elf bestätigte Scrapie-Fälle, die höchste Fallzahl (n=43) seit 1990 wurde 2004 beobachtet.[1]

Ätiologie
Als infektiöses Agens (Scrapie-Agens) wird ein krankhaft verändertes Protein, ein Prion, angesehen. Das normale Prion-Protein (PrPC, „c“ steht für engl. cell = Zelle) besteht beim Schaf aus 256 Aminosäuren (bei den Säugetieren schwankt die Anzahl zwischen 253 und 273 Aminosäuren). Seine C-terminale (jenes Ende, an dem die Carboxygruppe nicht an einer Peptidbindung beteiligt ist) Domäne besteht aus drei α-Helices und enthält zwei antiparallele β-Faltblätter.[2] Es ist Bestandteil nahezu aller Zellen, im Nervensystem vor allem der Nervenkontaktstellen (Synapsen), seine Funktion ist bislang unbekannt. Das PrP-Gen befindet sich auf Chromosom 20.
Das krankhaft veränderte Prion-Protein (PrPRES oder PrPSc, von resistant bzw. scrapie) unterscheidet sich lediglich durch einen höheren Anteil an β-Faltblattstrukturen.[3] Dadurch wird es unlöslich und nicht mehr durch Protein-spaltende Enzyme (Proteasen) abbaubar (Amyloidose). Die Molare Masse des durch Behandlung mit Proteinase K erzeugten Teilstücks von PrPSc beträgt 33 bis 35 Kilodalton. Die krankhaft veränderten Prion-Proteine lagern sich zusammen und bilden 500 bis 1000 nm lange Fibrillen (Scrapie-assoziierte Fibrillen, SAF) innerhalb der Nervenzellen. Dabei existieren verschiedene Unterformen des PrPSc (Erregerstämme), die sich hinsichtlich ihrer Protease-Empfindlichkeit und krankmachenden Wirkung im Mausmodell unterscheiden.[4]
Nach der Prionentheorie rufen einmal veränderte Prion-Proteine auch eine Änderung gesunder PrPC hervor. Der genaue Mechanismus dieses Prozesses ist bislang nicht bekannt und vermutlich spielen auch Wirtsfaktoren[5] und Kupfer-Ionen[6] eine Rolle bei der Entstehung. Das PrPSc von Schafen kann, wie auch das von BSE-infizierten Rindern, eine solche Veränderung beim Menschen hervorrufen, allerdings ist die krankmachende Wirkung des Schaf-PrPSc für den Menschen um ein Vielfaches geringer als jenes der Creutzfeldt-Jakob-Krankheit. Die Infektionsgefahr für den Menschen ist also gering, bislang gibt es keine gesicherten Übertragungen vom Schaf auf den Menschen, aber eine Einstufung als potentiell gefährlich erscheint gerechtfertigt.[7][8]
Das PrPSc ist nicht nur weitgehend unempfindlich gegenüber dem Abbau durch zelluläre Vorgänge, sondern auch gegenüber chemischen und physikalischen Einflüssen. Es ist weitestgehend resistent gegenüber vielen Desinfektionsmitteln, ionisierender und UV-Strahlung. Feuchte Hitze (131 °C) in zur Sterilisation in der Medizin eingesetzten Autoklaven zerstört das PrPSc erst nach zwei Stunden, so dass medizinische Instrumente viermal hintereinander autoklaviert werden müssen. Bei trockener Hitze wird das Prion bei 200 °C erst nach 60 Minuten inaktiviert. Wirksame Desinfektionsmittel sind z. B. Natriumhydroxid, Guanidiniumthiocyanat und Natriumhypochlorit.[9]
Übertragung
Das krankhafte Prion kommt im Zentralnervensystem, Gehirnwasser, in Mandeln, Lymphknoten und in der Milz vor. Es wird über die Nachgeburt und das Fruchtwasser ausgeschieden. Mit dem Scrapie-Agens kontaminierte Oberflächen können über Jahre eine Infektionsquelle sein.
Die natürliche Übertragung erfolgt zumeist durch orale Aufnahme von Nachgeburt und Fruchtwasser oder damit kontaminiertem Wasser oder Futter sowie Belecken des Lammes durch das Mutterschaf. Das Muttertier kann die Erkrankung auf den Fötus übertragen. Offenbar ist auch eine Übertragung durch Kontakt möglich, auch die Übertragung durch Milben (Heumilbe) wird diskutiert. Experimentell wurde auch eine Infektionsübertragung über die Bindehaut und kleinste Verletzungen der Maulschleimhaut sowie über Bluttransfusionen nachgewiesen. Auch kontaminierte Impfstoffe wurden als Auslöser identifiziert. Ebenso wird die Übertragung durch den Verzehr von Milch und Milchprodukten von Kleinwiederkäuern nicht ausgeschlossen[12].
Der Erreger gelangt über das enterische Nervensystem und die Eingeweidenerven in das Rückenmark und von dort aufsteigend in das Gehirn. Beim Schaf spielt auch die Verbreitung über das lymphatische System eine Rolle.
Empfänglichkeit
Prinzipiell sind alle Schafrassen empfänglich. Außer Schafen und (in geringerem Ausmaß) Ziegen sind auch Nerze, Mäuse, Ratten, Hamster, Europäische Mufflons, Affen und der Mensch empfänglich. Der Übergang des Erregers auf das Rind (BSE) wird als eigenständige TSE angesehen.
Die Anfälligkeit bei Schafen variiert in Abhängigkeit von der genetischen Variation in der Aminosäuresequenz des Prion-Proteins. So sind Schafe mit einer homozygoten Erbanlage für Alanin (A) an Position 136, Arginin (R) an Position 154 und Arginin an Position 171 (AA136, RR154, RR171) nahezu resistent. Allerdings sind mittlerweile atypische Scrapie-Fälle auch bei diesem Genotyp bekannt geworden[13] und auch dieser Genotyp ist prinzipiell für das BSE-Agens empfänglich, so dass die Tiere stumme Träger für BSE sein können.[14]
| Genotypklasse | Genotyp * | Gefährdung |
| G1 | AA, RR, RR | extrem niedrig („resistent“) |
| G2 | AA, RH, RQ AA, RR, RH AA, RR, RQ |
geringes Risiko wenn Anpaarung mit G1 oder G2 |
| G3 | AA, HH, QQ AA, HR, QH AA, HR, QQ AA, RR, HH AA, RR, HQ AA, RR, QQ |
erhöhtes Risiko für das Einzeltier, häufigster betroffener Genotyp in Deutschland ist ARQ |
| G4 | AV RR, RQ | hohes Risiko für das Einzeltier und die Hälfte der Nachkommen |
| G5 | AV, HR, QQ AV, RR, HQ AV, RR, QQ VV, RR, QQ |
sehr hohes Risiko |
| *Aminosäure 136, 154 und 171 beider Chromosomensätze; A=Alanin, R=Arginin, V=Valin, H=Histidin, Q=Glutamin; Paare gleicher Buchstaben bedeuten Homozygotie. (Quelle: NSP Genotypes Table der DEFRA) | ||
In der EU sind die Mitgliedsstaaten seit 2003 verpflichtet, Programme zur Züchtung von Schafen auf Resistenz gegen TSE aufzustellen. Bei Ziegen ist diese genetische Abhängigkeit nicht vorhanden, so dass keine Zucht auf Scrapie-resistente Tiere möglich ist.
Klinisches Bild
Nach der Prionentheorie soll die Inkubationszeit mehrere (meist drei bis vier) Jahre betragen. Bei experimenteller Infektion wurden Inkubationszeiten von 180 bis 900 Tagen ermittelt. So lange Zeiten bis zur Ausbildung erster Symptome sind sonst nur bei chronischen Erkrankungen etwa des Immunsystems, chronischen Vergiftungen oder erblich bedingten Erkrankungen bekannt. Die Traberkrankheit zählt zu den sogenannten slow infections („langsame Infektionen“). Die Erkrankung tritt frühestens im Alter von 18 Monaten klinisch in Erscheinung, am häufigsten tritt sie im Alter von drei Jahren auf. Die Traberkrankheit ist eine Erkrankung einzelner Tiere, sie betrifft bis zu 1 % der Tiere eines Bestandes.
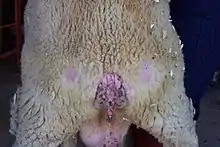
Klinisch zeigt sich die Erkrankung zunächst in Verhaltensveränderungen wie Schreckhaftigkeit, Unruhe, Veränderungen des Lippen- („Gnubbern“) und Ohrenspiels sowie Nick- und Seitwärtsbewegungen des Kopfes. Beim Ergreifen brechen erkrankte Tiere plötzlich zusammen. Auch ein vermehrter Speichelfluss wird häufig beobachtet. Ein weiteres charakteristisches Merkmal sind Störungen der Bewegungsabläufe wie eine Traber-artige Bewegung der Vordergliedmaßen („Traberkrankheit“), ein hahnentrittartiger Gang oder Schwäche der Hintergliedmaßen, Schleifen der Zehen über den Boden, schwankender Gang und Einknicken in den Gliedmaßen. Galopp und Sprünge sind den Tieren nicht mehr möglich. Ein weiteres häufig beobachtetes Merkmal ist Juckreiz, der dazu führt, dass die Tiere mit den Gliedmaßen aufstampfen, sich benagen oder an Gegenständen scheuern (daher der engl. Name Scrapie), was zu Beschädigungen des Vlieses führt. Im Regelfall geht die Erkrankung mit Abmagerung einher.
Nach den ersten Krankheitssymptomen überleben die betroffenen Schafe nur noch einen bis sechs Monate (in Extremfällen zwei Wochen bis sechs Monate), danach tritt unweigerlich der Tod ein.
Pathologie
Mit bloßem Auge (makroskopisch) lassen sich bei verendeten Tieren keine Veränderungen erkennen, abgesehen von eventuellen Haut- und Vliesschäden infolge des Scheuerns.
Das Hirngewebe zeigt histologisch eine Zellvermehrung der Astroglia und anschließend eine Vakuolisierung und Degeneration der Nervenzellen in Hirnstamm und Kleinhirn. Teilweise lassen sich eosinophile Granula und geschrumpfte (pyknotische) Zellkerne in den Nervenzellen nachweisen. Auch in der weißen Substanz kommt es zu einer Vakuolisierung. Elektronenmikroskopisch lassen sich die Scrapie-assoziierten Fibrillen nachweisen, immunhistochemisch auch die krankhaften Prion-Proteine.
Diagnose und Differentialdiagnose
Die Diagnose kann sicher nur anhand von Biopsien der Lymphknoten mit Nachweis des PrPSc durch ELISA oder Western-Blot und nach dem Tod durch eine pathohistologische Untersuchung gestellt werden. In jüngster Zeit wurden auch PrPSc-Nachweisverfahren am lebenden Tier vor dem Auftreten klinischer Erscheinungen entwickelt, die allerdings noch im Experimentalstadium sind.[15][16] Die Diagnose darf nur ein Amtstierarzt stellen. Nach positivem Befund in einer zugelassenen Untersuchungseinrichtung erfolgt eine zweite überprüfende Untersuchung der Probe im Friedrich-Loeffler-Institut. Für die Genotypisierung und damit Risikoabschätzung existieren verschiedene Gentests.
Differentialdiagnostisch müssen andere zentralnervöse Erkrankungen des Schafes wie Bornasche Krankheit, Tollwut, Visna, Listeriose, Coenurose, Enzootische Ataxie und Zerebrokortikalnekrose sowie mit neurologischen Symptomen einhergehende Stoffwechselerkrankungen wie Ketose und Hypokalzämie ausgeschlossen werden (Siehe auch VETAMIN D). Hinsichtlich des Juckreizes ist auch eine Psoroptes-Räude in Betracht zu ziehen.
Bekämpfung
Da die Traberkrankheit nicht behandelbar ist, ist die Bekämpfung auf die Tötung und unschädliche Beseitigung erkrankter Tiere in betroffenen Beständen, die Zucht auf genetisch resistente Schafe und Quarantänemaßnahmen gerichtet. Die konkreten Bekämpfungsmaßnahmen werden international unterschiedlich gehandhabt.
In der Europäischen Union wird die Bekämpfung durch die Verordnung (EG) Nr. 999/2001, zuletzt geändert in der Verordnung (EG) Nr. 339/2006, und das nationale Tierseuchenrecht (in Deutschland: Tierseuchengesetz, Viehverkehrsverordnung, VO über anzeigepflichtige Tierseuchen und die TSE-Überwachungsverordnung;[17] in Österreich: Scrapie-Überwachungsverordnung[18]) geregelt. Alle Todesfälle bei über 18 Monate alten Schafen müssen auf Scrapie untersucht werden, ebenso stichprobenartig alle Schlachttiere ab diesem Alter. Da die Traberkrankheit anzeigepflichtig ist, werden die entsprechenden Maßnahmen durch den Amtstierarzt festgelegt. Dabei ermöglichen die aktuellen Bestimmungen, dass nicht mehr ganze Bestände, sondern nur noch genetische Risikogruppen (Böcke G2–G5, weibliche Schafe G3–G5) in betroffenen Beständen getötet werden. Herden dürfen nach Bestandstötungen nur mit homozygoten ARH-Tieren oder heterozygoten ARH-Kombinationen mit anderen Genotypen außer VRQ aufgefüllt werden. Die Zukäufe sollten nur aus Beständen erfolgen, in denen mindestens 5, besser 8 Jahre keine Scrapie-Fälle mehr auftraten. Sollten keine entsprechenden Tiere verfügbar sein, kann das Veterinäramt Ausnahmeregelungen erlassen. Die Zucht auf „genetisch resistente“ Schafe ist durch die atypischen Scrapie-Fälle in jüngerer Zeit jedoch wieder fraglich geworden.[19] Durch konsequente Hygienemaßnahmen lassen sich auch mit genetisch-empfänglichen Genotypklassen Scrapie-freie Bestände erzeugen.[20]
Geschichte
Der erste publizierte Scrapie-Fall stammt aus dem Jahr 1732 aus Großbritannien. Die Anzahl der jährlich erkrankten Tiere wird allein dort auf ca. 10.000 geschätzt. Auch in Deutschland und im übrigen Europa ist die Erkrankung seit der Mitte des 18. Jahrhunderts aufgetreten. Die Einschleppung erfolgte vermutlich über Importe von Zuchtschafen. Die Traberkrankheit ist heute, mit Ausnahme von Australien und Neuseeland, weltweit verbreitet und tritt am häufigsten in Großbritannien und Zypern auf.
Die Zahl der klinischen Erkrankungen hat in Deutschland ab 1945 deutlich abgenommen, auch durch die Veränderung im Nutzungskonzept (Fleisch- statt Wollerzeugung), da Schafe heute selten älter als fünf Jahre werden.
1947 gab es in den Vereinigten Staaten erste Todesfälle auch bei Nerzen nach Verfütterung von Schafschlachtabfällen, ab 1967 auch in Europa. 1967 wurde erkannt, dass der Erreger aufgrund seiner Resistenz gegenüber Strahlung keine Nukleinsäure enthält und vermutet, dass ein infektiöses Protein beteiligt ist. 1982 wurde von Stanley Prusiner die Hypothese der alleinigen Proteinursache der TSE aufgestellt, er prägte auch den Begriff „Prion“ von proteinaceous infectious particle („eiweißartiger infektiöser Partikel“).
Der Ausbruch der BSE 1985 in Großbritannien wird der Verfütterung von aus Schafen erzeugtem Tierkörpermehl an Rinder zugeschrieben.
Siehe auch
- Sture Böcke (isländischer Film von 2015)
Literatur
- H. Behrens u. a.: Lehrbuch der Schafkrankheiten. 4. Auflage. Paul Parey, 2001, ISBN 3-8263-3186-9.
Weblinks
- Informationen des deutschen Landwirtschaftsministeriums zu Scrapie (Memento vom 27. September 2007 im Internet Archive)
Einzelnachweise
- BMLV: Anzahl der bestätigten Scrapie-Fälle bei Schafen und Ziegen in Deutschland 2015
- R. Riek u. a.: NMR characterization of the full-length recombinant murine prion protein, mPrP(23-231). In: FEBS Lett. 1997 Aug 18;413(2), S. 282–288. PMID 9280298
- K. M. Pan u. a.: Conversion of alpha-helices into beta-sheets features in the formation of the scrapie prion proteins. In: Proc Natl Acad Sci U S A. 1993 Dec 1;90(23), S. 10962–10966. PMID 7902575.
- M. E. Bruce: TSE strain variation. In: Br Med Bull. 2003; 66, S. 99–108. PMID 14522852.
- C. Fasano u. a.: Prions: protein only or something more? Overview of potential prion cofactors. In: J Mol Neurosci. 2006;29(3), S. 195–214. PMID 17085779
- E. Wong u. a.: Copper induces increased beta-sheet content in the scrapie-susceptible ovine prion protein PrPVRQ compared with the resistant allelic variant PrPARR. In: Biochem J. 2004 May 15;380(Pt 1), S. 273–282. PMID 14969585
- H. Cassard, J. M. Torres u. a.: Evidence for zoonotic potential of ovine scrapie prions. In: Nature Communications. Band 5, Dezember 2014, S. 5821, doi:10.1038/ncomms6821, PMID 25510416.
- E. E. Comoy, J. Mikol u. a.: Transmission of scrapie prions to primate after an extended silent incubation period. In: Scientific Reports. Band 5, Juni 2015, S. 11573, doi:10.1038/srep11573, PMID 26123044, PMC 4485159 (freier Volltext).
- P. Brown u. a.: Newer data on the inactivation of scrapie virus or Creutzfeldt-Jakob disease virus in brain tissue. In: J Infect Dis. 1986 Jun;153(6), S. 1145–1148. PMID 3084671
- L. Manuelidis: Transmissible encephalopathies: speculations and realities. In: Viral Immunol. 2003;16(2), S. 123–139. PMID 12828865
- L. Manuelidis: A 25 nm virion is the likely cause of transmissible spongiform encephalopathies. In: Cell Biochem. 2006 Oct 16. PMID 17044041
- EFSA Scientific Opinion: Gutachten des Gremiums für biologische Gefahren (BIOHAZ) über das Risiko für Mensch und Tier im Hinblick auf Transmissible Spongiforme Enzephalopathie. Efsa.europa.eu, 6. November 2008, abgerufen am 24. Mai 2010.
- G. C. Saunders u. a.: PrP genotypes of atypical scrapie cases in Great Britain. In: J Gen Virol. 2006 Nov;87(Pt 11), S. 3141–3149. PMID 17030846
- F. Ronzon u. a.: BSE inoculation to prion diseases-resistant sheep reveals tricky silent carriers. In: Biochem Biophys Res Commun. 2006 Dec 1;350(4), S. 872–877. Epub 2006 Oct 4. PMID 17049491
- P. Saa u. a.: Detection of prions in blood. In: Nat Med. 2005 Sep;11(9), S. 982–985. Epub 2005 Aug 28. PMID 16127436
- R. Jackman u. a.: Evaluation of a preclinical blood test for scrapie in sheep using immunocapillary electrophoresis. In: Journal of AOAC International. 2006;89(3), S. 720–727. PMID 16792071.
- Text der TSE-Überwachungsverordnung
- Scrapie-Überwachungsverordnung Österreich (PDF)
- A. Buschmann, M. H. Groschup: TSE-Bekämpfung bei kleinen Wiederkäuern - quo vadis? In: Berl Munch Tierarztl Wochenschr. 2005 Sep-Oct;118(9-10), S. 365–371. PMID 16206923
- J. Foster u. a.: Derivation of a scrapie-free sheep flock from the progeny of a flock affected by scrapie. In: Vet Rec. 2006 Jul 8;159(2), S. 42–45. PMID 16829598