Isotopenmarkierung
Die Methode der Isotopenmarkierung (auch Methode der isotopisch markierten Verbindungen oder Tracer-Technik) beschreibt das systematische Einfügen definierter Isotope in organische Verbindungen.[1][2][3] Durch den Austausch von Isotopen lassen sich zwei markierte Moleküle oder Atome im Verlauf chemischer Reaktionen unterscheiden.[1][3] Anhand der gewonnenen Informationen können Reaktionsmechanismen aufgeklärt werden.[1][3]
Eigenschaften
In einer chemischen Reaktion sind in der Regel nur die Edukte und die Produkte erkennbar.[1] Mit der Isotopenmarkierung lässt sich die Rolle zweier verschieden gebundener Atome im Reaktionsverlauf untersuchen.[1] Der Vorteil der Isotopenmarkierung ist dabei, dass kein Zusatz störender Substanzen erforderlich ist.[1] Das zur Markierung genutzte Isotop lässt sich im Anschluss an die Reaktion mittels Analyseverfahren, wie der NMR-Technik oder Massenspektrometrie in dem gebildeten Produkt und seiner entsprechenden Bindungssituation nachweisen.[1]

Da es sich bei den markierten Verbindungen meist um kostspielige Stoffe handelt, wird eine markierte Verbindung mit einem Überschuss an unmarkierter Verbindung verdünnt.[1] Beispiele eines Austausch von Isotopen sind der Ersatz von H, durch schweren Wasserstoff wie D (Deuterium) oder T (Tritium), 12C durch 13C, 14C oder 16O durch 17O, 18O.[1][3]
Anwendungen
Melvin Calvin wendete die Isotopenmarkierung bei der Entdeckung des Calvin-Zyklus an.[4] Der Meselson-Stahl-Versuch ist ein weiteres bekanntes Beispiel für die Anwendung der Isotopenmarkierung, durch den Versuch wurde die semikonservative Replikation der DNA nachgewiesen.[5]
Aufklärung von Reaktionsmechanismen
Ein Beispiel zur Anwendung der Isotopenmarkierung als Aufklärungsmethode in der organischen Chemie ergibt sich nach Roberts und Urey mit der Esterbildung.[1] Die Aufklärung des zugehörigen Mechanismus warf zunächst die Frage auf, ob das alkylgebundene hydroxide Sauerstoffatom des Alkohols nach Abschluss der Reaktion im Ester oder im entstandenen Wasser vorliegt.[1] Durch die Verwendung eines mit 18O-markierten Alkohols (nachfolgend blau dargestellt) ließ sich zeigen, dass das 18O-Isotop ausschließlich im Ester nachzuweisen ist, demnach nur der obere Reaktionsweg (A) abläuft (es wird lediglich eine Richtung der Reaktion betrachtet, wobei es sich bei dem gewöhnlich gebundenen Sauerstoff um das 16O-Isotop handelt):[1]

Mittels Isotopenmarkierung ließ sich zudem die Unbeständigkeit der Carbonylgruppe der Carbonsäure im Laufe der Esterbildung feststellen.[1]
Biotechnologische Methode – metabolische Markierung
Gezielt isotopenmarkierte Verbindungen, wie Arzneistoffe, Wirkstoffe in Pflanzenschutzmitteln oder Proteine werden hergestellt, um den Metabolismus dieser Stoffe gezielt untersuchen zu können. Mittels isotopenmarkierter Wirkstoffe kann der Abbau dieser Stoffe im Körper, die Ausscheidung (z. B. über den Urin) und deren Verbleib in der Umwelt studiert werden.[6] Dies wird beispielsweise mit der Methode der metabolischen Markierung erreicht, bei der bestimmte Zellkulturen in speziellen Nährmedien unter anderen mit isotopisch markierten Verbindungen (zum Beispiel 35S) angereichert werden können, um anschließend ihren Verbleib im Metabolismus von Organismen untersuchen zu können.[6]
SILAC-Methode
Das Verfahren der metabolischen Markierung findet beispielsweise im Rahmen der SILAC-Methode (zum Beispiel in Form einer 15N-Markierung) Anwendung.[7]
Anwendung in weiteren Methoden
Eine chemische Variante der Isotopenmarkierung ist die Dimethyl-Markierung (ICAT).[8]
Die Isotopenmarkierung findet zudem Anwendung in Form der Isobarenmarkierung.[9][10]
Mögliche Herstellung einer isotopenmarkierter Verbindungen
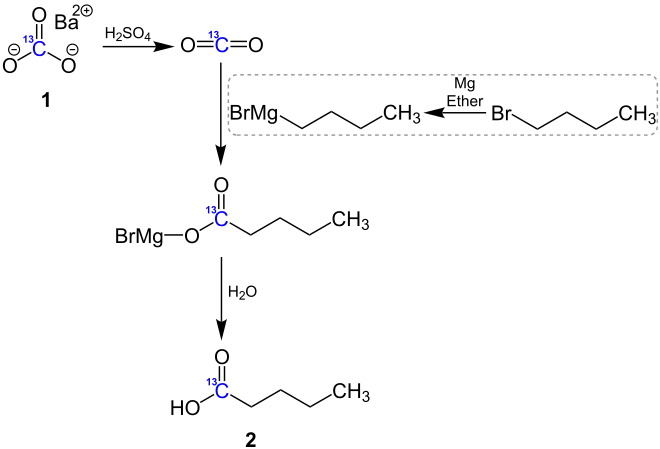
Exemplarisch lässt sich, ausgehend von 13C-markiertem Bariumcarbonat (1), mittels Zusatz von Schwefelsäure 13C-markiertes Kohlenstoffdioxid herstellen.[11][12] Über eine Grignard-Reaktion mit Butylmagnesiumbromid kann das markierte Kohlenstoffdioxid anschließend zur Carbonsäure (2) mit 13C-markierter Carbonylgruppe umgesetzt werden.[13]
Einzelnachweise
- Ivan Ernest: Bindung, Struktur und Reaktionsmechanismen in der organischen Chemie. Springer-Verlag, Wien, 1972, S. 72–74, ISBN 978-3-211-81365-2, doi:10.1007/978-3-7091-8437-0.
- Hans Rudolf Christen, Günther Baars: Chemie. 1. Auflage, Verlag Sauerländer; Aarau und Diesterweg Verlag; Frankfurt am Main, 1997, S. 35, ISBN 3-7941-3768-X (Sauerländer), ISBN 3-425-05393-0 (Diesterweg).
- Jürgen Falbe, Manfred Regitz (Hrsg.): RÖMPP. Lexikon. Chemie H–L. 10. Auflage, Georg Thieme Verlag, Stuttgart, 1997, S. 2015–2016, ISBN 3-13-734810-2.
- Richard E. Dickerson, Harry B. Gray, Marcetta Y. Darensbourg, Donald J. Darensbourg: Prinzipien der Chemie. 2. Auflage, Walter de Gruyter, Berlin, New York, 1988, S. 747, ISBN 3-11-009969-1.
- Matthew Meselson, Franklin W. Stahl: The replication of DNA in Escherichia coli. In: Proceedings of the National Academy of Sciences. Band 44, Nr. 7, 1958, S. 671–682, doi:10.1073/pnas.44.7.671.
- Kurt E. Geckeler, Heiner Eckstein (Hrsg.): Bioanalytische und biochemische Labormethoden. Springer-Verlag, Wiesbaden, 2013, S. 457–458, ISBN 978-3-642-63745-2, doi:10.1007/978-3-642-58820-4.
- Shao-En Ong, Blagoy Blagoev, Irina Kratchmarova, Dan Bach Kristensen, Hanno Steen, Akhilesh Pandey, Matthias Mann: Stable Isotope Labeling by Amino Acids in Cell Culture, SILAC, as a Simple and Accurate Approach to Expression Proteomics. In: Molecular & Cellular Proteomics. Band 1, 2002, S. 376–386, doi:10.1074/mcp.M200025-MCP200.
- Steven P. Gygi, Beate Rist, Scott A. Gerber, Frantisek Turecek, Michael H. Gelb, Rudolf Hans Aebersold|Ruedi Aebersold: Quantitative analysis of complex protein mixtures using isotope-coded affinity tags. In: Nature Biotechnology. Band 17, Nr. 10, 1999, S. 994–999, doi:10.1038/13690.
- Thompson A, Schäfer J, Kuhn K et al.: Tandem mass tags: a novel quantification strategy for comparative analysis of complex protein mixtures by MS/MS. In: Anal. Chem.. 75, Nr. 8, 2003, S. 1895–904. doi:10.1021/ac0262560. PMID 12713048.
- Ross PL, Huang YN, Marchese JN, Williamson B, Parker K, Hattan S, Khainovski N, Pillai S, Dey S, Daniels S, Purkayastha S, Juhasz P, Martin S, Bartlet-Jones M, He F, Jacobson A, Pappin DJ: Multiplexed protein quantitation in Saccharomyces cerevisiae using amine-reactive isobaric tagging reagents. In: Mol. Cell. Proteomics. 3, Nr. 12, 2004, S. 1154–1169. doi:10.1074/mcp.M400129-MCP200. PMID 15385600.
- Barium carbonate-13C als Rohstoff im Katalog von Sigma-Aldrich/Merck. Website des Rohstoffherstellers Sigma-Aldrich/Merck. Abgerufen am 10. November 2017.
- Nils Wiberg, Egon Wiberg, Arnold Frederik Holleman: Anorganische Chemie – Grundlagen und Hauptgruppenelemente. Band 1, 103. Auflage, Walter de Gruyter GmbH, Berlin/Boston, 2016, S. 235–237 & S. 1031, ISBN 978-3-11-026932-1.
- Hauptmann Siegfried: Organische Chemie. 1. Auflage, Verlag Harri Deutsch, Thun, Frankfurt am Main, 1985, S. 400, ISBN 3-87144-902-4.