Duloxetin
Duloxetin ist ein Arzneistoff aus der Gruppe der selektiven Serotonin-Noradrenalin-Wiederaufnahmehemmer (SSNRI) und wird in der Behandlung von Depressionen, generalisierten Angststörungen, diabetischer Polyneuropathie und Harninkontinenz eingesetzt.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
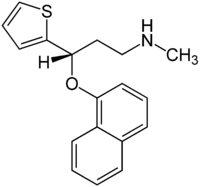 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Duloxetin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel |
| |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
N06AX21 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 297,42 g·mol−1 (Duloxetin) | |||||||||||||||||||||
| Löslichkeit |
Duloxetinhydrochlorid: wenig löslich in Wasser, leicht löslich in Methanol, praktisch unlöslich in Hexan[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
In den Studien wurden neben den psychischen Beschwerden auch begleitende körperliche Symptome (zum Beispiel Schmerzen) gelindert. Der analgetische Effekt bei Schmerzsymptomen in Verbindung mit Depression ist nach einer neueren Metaanalyse vorhanden, allerdings sehr gering ausgeprägt.[4]
Duloxetin wurde von der Firma Eli Lilly entwickelt. Cymbalta gehört zu den „Blockbuster-Medikamenten“ (2013 über 6 Mrd. Dollar Umsatz).
Anwendungsgebiete
Zugelassene Anwendungsgebiete für Duloxetin sind die Behandlung von Frauen mit mittelschwerer bis schwerer Belastungsharninkontinenz (Yentreve) sowie die Behandlung von depressiven Erkrankungen, generalisierten Angststörungen und Schmerzen bei diabetischer Polyneuropathie (Cymbalta, Xeristar, Duloxetine Lilly).
Die Mittel sind peroral anwendbar, es sind verschiedene Wirkstärken verfügbar. Pharmazeutisch wird ausschließlich das Hydrochlorid von Duloxetin eingesetzt.[5]
Entwicklung und Vermarktung
Yentreve
Am 11. August 2004 erteilte die Europäische Kommission dem Unternehmen Eli Lilly Nederland B.V. eine Genehmigung für das Inverkehrbringen von Yentreve in der gesamten Europäischen Union. Entgegen den Erwartungen der Partner (Eli Lilly und Boehringer Ingelheim) verlief der Umsatz von Yentreve enttäuschend, woraufhin sich Boehringer Ingelheim aus der gemeinsamen Kooperation mit Lilly im Bereich Belastungsinkontinenz verabschiedete.[6]
Im Januar 2005 wurde in den USA der Zulassungsantrag für Yentreve hingegen zurückgezogen, da die FDA schwere Sicherheitsbedenken hatte. In den US-Studien kam es zu einer deutlich erhöhten Anzahl von Suizidversuchen, die FDA sprach sogar von einem doppelt so hohen Risiko im Vergleich zur Normalbevölkerung.[7] Bereits zuvor kam es immer wieder zu Suiziden in Duloxetin-Studien, darunter der besonders tragische Fall einer gesunden Probandin, die sich in einem Forschungslabor von Eli Lilly mit einem Schal erhängte. Sie war kurz zuvor von Duloxetin auf Placebo umgestellt worden, als Grund wurde daher ein akutes Entzugssyndrom vermutet.[8] Sowohl Eli Lilly als auch die FDA wurden für ihre damalige Beschwichtigungspolitik heftig kritisiert.[9]
Cymbalta/Xeristar
Im Dezember 2004 bekamen auch Cymbalta und Xeristar eine EU-weite Zulassung, anfangs nur zur Behandlung von depressiven Episoden. Bereits 2005 wurde die Indikation um die Behandlung von Schmerzen bei diabetischer Polyneuropathie bei Erwachsenen erweitert. 2008 kam die Behandlung der generalisierten Angststörung dazu und 2009 schließlich die Erweiterung zur Behandlung depressiver Erkrankungen (Major Depression). Einzig beim Versuch, auch Fibromyalgie den Indikationen hinzuzufügen, scheiterte die Firma 2008. Der Ausschuss für Humanarzneimittel (CHMP) der EMA war der Auffassung, dass die Wirksamkeit von Cymbalta/Xeristar bei der Behandlung der Fibromyalgie nicht hinreichend nachgewiesen worden war.[10]
Vor der Öffnung des Marktes für Generikahersteller kam Lilly 2014 mit der Zulassung Duloxetine Lilly hinzu. Boehringer zog seine 2004 erhaltene Zulassung für Ariclaim (Behandlung von Schmerzen bei diabetischer Polyneuropathie) im Jahr 2018 zurück.
Kosten-Nutzen-Bewertung in Deutschland
2013 lautete der Befund der ersten Kosten-Nutzen-Bewertung des Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) für die Wirkstoffe Venlafaxin, Duloxetin, Bupropion und Mirtazapin, dass Duloxetin im Verhältnis zum Nutzen deutlich höhere Preise als andere Antidepressiva habe.[11]
Seit 2015 sind für den deutschen Markt auch Duloxetin-Generika zugelassen.[12]
Pharmakologie
| Rezeptor | K (nM)i |
|---|---|
| SERT | 0.8 |
| NET | 7.5 |
| DAT | 240 |
| 5-HT6 | 419 |
| 5-HT2A | 504 |
| 5-HT2C | 916 |
| Histamin H1 | 2300 |
| α1 | 8300 |
| α2 | 8600 |
Duloxetin ist chiral und wird als stereochemisch einheitlicher (= reiner). Arzneistoff in der (S)-Konfiguration eingesetzt. Der Wirkstoff ist ein kombinierter Serotonin- und Noradrenalin-Wiederaufnahmehemmer. Er zeigt eine geringe Wiederaufnahmehemmung von Dopamin, hat aber keine signifikante Affinität für Histamin-, Dopamin- und Acetylcholin-Rezeptoren sowie Adrenozeptoren. Die schmerzhemmende Wirkung von Duloxetin dürfte auf eine Verstärkung der absteigenden hemmenden Schmerzbahnen im zentralen Nervensystem zurückzuführen sein. Die antidepressive Wirkung tritt erst mit einer zeitlichen Latenz auf und ist – wie bei allen Antidepressiva – vermutlich auf die höhere Neurotransmitterverfügbarkeit durch Anpassung der Rezeptoren und ähnlicher Strukturen zurückzuführen.
Im Vergleich mit anderen Serotonin-Noradrenalin-Wiederaufnahmehemmer hat Duloxetin eine 10-fach größere Selektivität für Serotonin als für Noradrenalin. Während Milnacipran die Serotonin- und Noradrenalin-Wiederaufnahme ungefähr gleich stark blockiert, hat Venlafaxin eine 30-fach größere Selektivität für Serotonin.[14]
Verstoffwechselung (Pharmakokinetik)
Die absolute orale Bioverfügbarkeit von Duloxetin schwankt stark und kann je nach Patient zwischen 32 % und 80 % liegen. Dies ist auf den starken First-Pass-Effekt zurückzuführen, der großen interindividuellen Unterschieden unterliegt, bedingt durch u. a. Geschlecht, Alter, Raucherstatus (im Vergleich zu Nichtrauchern eine um nahezu 50 % reduzierte Plasmakonzentration), Nahrungsaufnahme und Enzymaktivität des Cytochrom P450 2D6 (CYP2D6). Auch Leber- und Nierenerkrankungen beeinflussen die Pharmakokinetik von Duloxetin. Der Abbau erfolgt gleichzeitig über die Cytochrome P450 1A2 und 2D6 (wobei Duloxetin wohl nur eine moderate Hemmung von 2D6 bewirkt und die anderen Isoenzyme damit nicht gehemmt werden[15]). Eine Hemmung eines dieser Enzyme durch andere Arzneimittel kann zu gefährlichen Überdosierungen führen (siehe Wechselwirkungen). Die entstehenden beiden Hauptmetaboliten 4-Hydroxy-Duloxetin und 5-Hydroxy-6-Methoxy-Duloxetin sind beide inaktiv.[16]
Unerwünschte Wirkungen
Zu den beobachteten Nebenwirkungen gehören:
- Übelkeit, trockener Mund, Halsentzündung und Obstipation (Verstopfung)
- Durchfall, Erbrechen, Appetitverlust oder -abnahme
- Kopfschmerzen, unscharfes Sehen, Schwindel, Schläfrigkeit und Zittern
- Schlafstörungen, Angst und Nervosität
- vermehrtes Schwitzen, Nachtschweiß und Hitzewallungen
- Frieren
- Müdigkeit, häufiges Gähnen
- Sexualstörungen (z. B. Orgasmusunfähigkeit oder Erektionsprobleme)
- Blutdruckerhöhung und Herzbeschwerden
- verzögerte Miktion und Harnverhalt
- Es wurde von Leberschäden berichtet – insbesondere im Zusammenhang mit Alkohol.[17]
Die unerwünschten Effekte treten insbesondere in den ersten Tagen nach dem Beginn der Einnahme auf, können aber auch mehrere Wochen andauern. Im direkten Vergleich ist Duloxetin dem Venlafaxin unterlegen: Mehr Patienten brachen die Therapie wegen Nebenwirkungen ab. Sowohl Duloxetin als auch Venlafaxin schnitten bezüglich dieses Kriteriums schlechter als Serotonin-Wiederaufnahmehemmer ab.[18][19]
Wenn die Einnahme von Duloxetin abrupt beendet wird, können Absetzsymptome auftreten. Es können Schwindel, Hyperhidrose, Übelkeit, Erbrechen, Diarrhoe, Schlafstörungen, Kopfschmerzen, sensorische Störungen, Reizbarkeit und Angst auftreten. Daher wird empfohlen, die Behandlung ausschleichend zu beenden.[20]
Wechselwirkungen und Gegenanzeigen
Bei der Anwendung von Duloxetin zusammen mit anderen Antidepressiva ist Vorsicht geboten. Die gleichzeitige Anwendung von Duloxetin und irreversiblen Monoaminooxidase-Hemmern (MAO-B-Hemmern) wie Selegilin und Tranylcypromin ist kontraindiziert. Ebenfalls kontraindiziert ist die Kombination mit CYP1A2-Inhibitoren, wie Fluvoxamin, Ciprofloxacin oder Enoxacin, da erhöhte Plasmaspiegel von Duloxetin resultieren.[20] Die Kombination von Duloxetin mit reversiblen MAO-Hemmern wie Moclobemid wird nicht empfohlen. Duloxetin sollte nicht zusammen mit Johanniskraut eingenommen werden.[21]
Schwangerschaftsrisiken
Das potenzielle Risiko für den Menschen ist unbekannt. Auch wenn keine Daten über die Anwendung von Duloxetin vorliegen, ist darauf hinzuweisen, dass Entzugssymptome bei Neugeborenen aufgetreten sind, wenn die Mutter kurz vor dem Entbindungstermin andere serotonerge Arzneimittel angewendet hat. Duloxetin sollte während der Schwangerschaft nicht angewendet werden. Die Einnahme von Duloxetin ist jedoch kein Grund für einen Schwangerschaftsabbruch. Frauen, die während der Behandlung schwanger werden oder beabsichtigen, schwanger zu werden, sollten ihren Arzt darüber unterrichten.[20] Im Tierversuch führte Duloxetin zu Schäden bei den Nachkommen trächtiger Tiere, denen es verabreicht wurde (siehe unten). Es ist jedoch unklar, ob dies auf den Menschen übertragen werden kann.
Bei Nachkommen trächtiger Mäuse, die Duloxetin erhielten, wurde eine Wachstumsverzögerung der Jungen beobachtet. Bei den Nachkommen trächtiger Kaninchen konnte in einer Studie eine erhöhte Inzidenz kardiovaskulärer und das Skelett betreffender Missbildungen festgestellt werden, in einer anderen Studie jedoch nicht. Wurde Duloxetin trächtigen Ratten verabreicht, so traten Verhaltensauffälligkeiten bei deren Jungen auf.[22]
Handelsnamen
Cymbalta (EU, CH, USA, J), Yentreve (EU), Xeristar (EU), diverse Generika
Weblinks
- Warnhinweis der FDA zu Duloxetin, FDA ALERT, 7/2006
- Duloxetin (Cymbalta). In: Wirkstoff AKTUELL, 03/2009, Stand: 20. Februar 2009, (PDF 72 kB)
- Europäische öffentliche Beurteilungsberichte (EPAR) zu Duloxetin auf der Seite der Europäischen Arzneimittelagentur
- Kritische Bewertung
Einzelnachweise
- Europäisches Arzneibuch. 8. Ausgabe. Grundwerk 2014, S. 3150.
- Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von N-Methyl-gama-(1-naphthalenyloxy)-2-thiophenepropanamine im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 16. Januar 2020.
- Eintrag zu Duloxetin in der DrugBank der University of Alberta
- Psychother Psychosom. Band 77, Nr. 1, 2008, S. 12–16, doi:10.1159/000110055. PMID 18087203.
- ROTE LISTE 2008. Verlag Rote Liste Service, Frankfurt am Main 2008, ISBN 978-3-939192-20-6.
- Änderung des Abkommens bezüglich Yentreve/Ariclaim Unternehmensbericht 2005 (Memento vom 20. Dezember 2013 im Internet Archive) (PDF; 3,1 MB).
- J Lenzer FDA warns that antidepressants may increase suicidality in adults. In: BMJ. Band 331, 2005, S. 70. PMID 16002878.
- G. Harris: Student, 19, in Trial of New Antidepressant Commits Suicide. In: The New York Times. 12. Februar 2004.
- J. Lenzer: What the FDA isn't telling. In: Slate Magazine. 27. September 2005.
- Öffentlicher Beurteilungsbericht (EPAR) der europäischen Arzneimittelagentur (EMA) zu: Cymbalta
- Kosten-Nutzen-Bewertung von Venlafaxin, Duloxetin, Bupropion und Mirtazapin im Vergleich zu weiteren verordnungsfähigen medikamentösen Behandlungen. (PDF) Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen, 30. Oktober 2013, abgerufen am 1. Januar 2014.
- Fachinformationen entsprechender Präparate, einsehbar z. B. auf Rote Liste online (Memento vom 25. Januar 2019 im Internet Archive) und der Website der europäischen Arzneimittelagentur, abgerufen am 10. März 2019.
- F. P. Bymaster, L. J. Dreshfield-Ahmad, P. G. Threlkeld, J. L. Shaw, L. Thompson: Comparative affinity of duloxetine and venlafaxine for serotonin and norepinephrine transporters in vitro and in vivo, human serotonin receptor subtypes, and other neuronal receptors. In: Neuropsychopharmacology: Official Publication of the American College of Neuropsychopharmacology. Band 25, Nr. 6, Dezember 2001, S. 871–880, doi:10.1016/S0893-133X(01)00298-6, PMID 11750180.
- C. Moret, M. Charveron, J. P. Finberg, J. P. Couzinier, M. Briley: Biochemical profile of midalcipran (F 2207), 1-phenyl-1-diethyl-aminocarbonyl-2-aminomethyl-cyclopropane (Z) hydrochloride, a potential fourth generation antidepressant drug. In: Neuropharmacology. Band 24, Nr. 12, 1985, S. 1211–9, doi:10.1016/0028-3908(85)90157-1, PMID 3005901.
- Torsten Kratz, Albert Diefenbacher: Psychopharmakotherapie im Alter. Vermeidung von Arzneimittelinteraktionen und Polypharmazie. In: Deutsches Ärzteblatt. Band 116, Heft 29 f, 22. Juli 2019, S. 508–517, S. 509.
- Duloxetin (Cymbalta®). (PDF 77 kB) In: Wirkstoff AKTUELL – Ausgabe 03/2009. Kassenärztliche Bundesvereinigung; Arzneimittelkommission der deutschen Ärzteschaft, 20. Februar 2009, abgerufen am 22. Juni 2010 (Kopieren von Inhalt zulässig): „Duloxetin ist kein Mittel der ersten Wahl bei der Akutbehandlung depressiver Erkrankungen“
- arznei-telegramm.de
- Antidepressiva: Nutzen von SNRI belegt. Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen, 18. August 2009, abgerufen am 1. Januar 2014.
- SNRI bei Patienten mit Depressionen, S. 3, Tabelle 2, Abschlussbericht A05-20A, Kurzfassung, Version 1.0, 17. Juni 2009, IQWiG 111 kB, abgerufen am 21. März 2010.
- Fachinformation des Arzneimittel-Kompendium der Schweiz: Cymbalta; Stand: Februar 2008.
- Fachinformation Yentreve, Stand Juli 2004.
- Fachinformationen "Cymbalta"; Stand: April 2009.