Milnacipran
Milnacipran ist ein Arzneistoff, der in einigen Ländern der EU als Antidepressivum zugelassen ist und zu den selektiven Serotonin-Noradrenalin-Wiederaufnahmehemmern (SSNRI) gehört.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
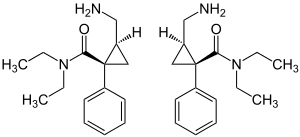 | ||||||||||||||||
| 1:1-Gemisch: (1R,2S)-Isomer (links) und (1S,2R)-Isomer (rechts) | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Milnacipran | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Summenformel |
| |||||||||||||||
| Kurzbeschreibung |
weißes Pulver (Milnacipran·Hydrochlorid) [1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| ATC-Code |
N06AX17 | |||||||||||||||
| Wirkstoffklasse | ||||||||||||||||
| Wirkmechanismus | ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | ||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
Wasser: 19 g·l−1 (HCl)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Indikationen
In Österreich erfolgte die Zulassung als Antidepressivum im Jahr 1998. In Deutschland wurde Milnacipran im Jahr 2016 zugelassen. In der Schweiz hat der Hersteller Pierre Fabre Médicament bisher keine Zulassung beantragt. Als Antidepressivum ist der Wirkstoff in über 40 Ländern zugelassen, darunter Frankreich, Russland, Japan, Finnland.
In den USA ist Milnacipran für die Indikation Fibromyalgie-Syndrom (FMS) seit 2009 zugelassen. In Europa dagegen wurde in die Zulassung hierfür wegen unwesentlicher Wirkung und fehlender Langzeitdaten in einer europäischen Population versagt.[4][5]
2008 wurde in einer Metaanalyse festgestellt, dass in der Wirkung und Verträglichkeit von Milnacipran zu anderen Antidepressiva kein Unterschied nachweisbar ist, wobei festgestellt wurde, dass weniger Patienten aufgrund von Nebenwirkungen die Behandlung abgebrochen haben.[6] Ein Cochrane-Review aus dem Jahr 2009 kommt zu dem Schluss, dass Informationen über klinisch bedeutende Ergebnisse wie Kosteneffektivität und Fähigkeit zur Wiederaufnahme der Arbeit fehlen.[7]
Pharmakologie
Milnacipran hemmt im Zentralnervensystem die Wiederaufnahme (engl.: reuptake) von Serotonin und von Noradrenalin aus dem synaptischen Spalt in die präsynaptischen Vesikel. Die Substanz wird pharmakologisch den selektiven Serotonin-Noradrenalin-Wiederaufnahmehemmern (SSNRI) zugeordnet. Zu dieser Gruppe gehören auch Venlafaxin und Duloxetin. Während Milnacipran die Serotonin- und Noradrenalin-Wiederaufnahme ungefähr gleich stark blockiert, hat Duloxetin eine 10-fach größere Selektivität für Serotonin, Venlafaxin eine 30-fach größere Selektivität für Serotonin.[8] Die Substanz hat keine Affinität zu postsynaptischen Rezeptoren.[9]
Gegenanzeigen (Kontraindikationen)
Milnacipran darf in folgenden Fällen nicht eingesetzt werden:
- bei Verwendung von nichtselektiven MAO-Hemmern sowie selektiven MAO-A-Hemmern: Gefahr eines Serotonin-Syndroms
- selektiven MAO-B-Hemmern, Digitalis, 5-HT1D-Agonisten (z. B. Sumatriptan), parenteralem Adrenalin und Noradrenalin sowie Clonidin und verwandten Stoffen: Gefahr hypertoner Krisen
- bei benigner Prostatahyperplasie und anderen urogenitalen Störungen
- während der Stillperiode.
Die allgemein für SSRI und SNRI ergangene Warnung der Europäischen Arzneimittelagentur bezüglich der Therapie von Kindern und Jugendlichen ist zu beachten.
Wechselwirkungen mit anderen Arzneimitteln
Milnacipran wird nicht über das Cytochrom P450 der Leber abgebaut und hat mit keinem der CYP-Systeme klinisch signifikante Wechselwirkungen. Die Plasmaspiegel gleichzeitig eingenommener Medikamente werden durch Milnacipran nicht verändert. Auch Wechselwirkungen mit Alkohol sind nicht bekannt.[9]
Pharmakokinetik
Milnacipran wird nach oraler Einnahme gut resorbiert. Die Bioverfügbarkeit beträgt circa 85 % und wird durch die Nahrungsaufnahme nicht beeinträchtigt. Die Plasmaspitzenkonzentration wird bei oraler Einnahme etwa nach zwei Stunden erreicht und beträgt ca. 120 ng/ml nach einer einmaligen Gabe von 50 mg. Die Konzentrationen steigen proportional zur Dosis bis zu 200 mg pro Gabe. Die Plasmaproteinbindung ist gering (13 %) und ist nicht sättigbar. Das Verteilungsvolumen von Milnacipran beträgt etwa 5 l/kg mit einer Gesamtclearance von ca. 40 l/h. Renale und nichtrenale Clearance sind äquivalent. Der Metabolismus von Milnacipran beschränkt sich im Wesentlichen auf eine Glucuronsäure-Konjugation. Sehr geringe Konzentrationen aktiver Metaboliten ohne klinische Relevanz wurden nachgewiesen. Die Plasmahalbwertszeit beträgt etwa 8 Stunden. Die Ausscheidung erfolgt im Wesentlichen über die Niere (90 % der verabreichten Dosis) mit einer tubulären Sekretion des unveränderten Produkts. Nach wiederholter Gabe ist Milnacipran zwei bis drei Tage nach Beendigung der Behandlung vollständig ausgeschieden. Eine Leberinsuffizienz verursacht keine signifikante Änderung der pharmakokinetischen Eigenschaften des Wirkstoffes.[10] Milnacipran ist bei Patienten mit Niereninsuffizienz mit Vorsicht einzusetzen – die Dosierung muss gegebenenfalls aufgrund einer verlängerten Eliminationshalbwertszeit verringert werden.[11]
Stereoisomerie

2-(Aminomethyl)-N,N-diethyl-1-phenyl cyclopropancarbamid enthält zwei Stereozentren. Somit existieren die folgenden vier Formen:
- (1R,2S)-Isomer
- (1S,2R)-Isomer
- (1R,2R)-Isomer
- (1S,2S)-Isomer
Der Arzneistoff Milnacipran ist ein Racemat (1:1-Gemisch) aus dem (1R,2S)-Isomer und dem (1S,2R)-Isomer.[3] Das (1R,2R)-Isomer und das (1S,2S)-Isomer besitzen keine praktische Bedeutung.
Handelsnamen
Ixel (A), Savella (USA), Toledomin (Japan), Joncia (Australien), Tivanyl (Mexiko), Dalcipran (Chile), Milna-neurax (D)
Literatur
- Effect of repeated treatment with milnacipran on the central dopaminergic system. In: Pol J Pharmacol. 2000 Mar-Apr;52(2):83-92; PMID 10949109.
- SNRIs: their pharmacology, clinical efficacy, and tolerability in comparison with other classes of antidepressants. In: CNS Spectr. 2005 Sep;10(9):732–747; PMID 16142213.
Einzelnachweise
- Datenblatt Milnacipran hydrochloride bei Sigma-Aldrich, abgerufen am 10. April 2011 (PDF).
- Eintrag zu Milnacipran. In: Römpp Online. Georg Thieme Verlag, abgerufen am 12. November 2014.
- The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage, 2006, S. 1069, ISBN 978-0-911910-00-1.
- Fragen und Antworten zur Empfehlung der Versagung der Genehmigung für das Inverkehrbringen für Milnacipran Pierre Fabre Médicament/Impulsor. (41 kB; PDF) In: Dok.-Ref.: EMA/64535/2010, EMEA/H/C/1034, EMEA/H/C/1122. Ausschuss für Humanarzneimittel (CHMP), 3. Februar 2010, S. 2, abgerufen am 24. August 2010: „Wirkung ... unwesentlich. ... Langzeitwirkungen in einer europäischen Population ... fehlten. ... in Europa zurzeit keine klinischen Prüfungen ... bei Fibromyalgie laufen“.
- REFUSAL ASSESSMENT REPORT FOR Milnacipran Pierre Fabre Medicament. (608 kB; PDF) In: Procedure No. EMEA/H/C/001034. European Medicines Agency, 26. April 2010, abgerufen am 24. August 2010 (englisch, 50 Seiten).
- Nakagawa A, Watanabe N, Omori IM, et al.: Efficacy and tolerability of milnacipran in the treatment of major depression in comparison with other antidepressants: a systematic review and meta-analysis. In: CNS Drugs. 22, Nr. 7, 2008, S. 587–602. PMID 18547127.
- Nakagawa A, Watanabe N, Omori IM, et al.: Milnacipran versus other antidepressive agents for depression. In: Cochrane Database Syst Rev.. 8, Nr. 3, S. CD006529. PMID 19588396.
- Moret C, Charveron M, Finberg JP, Couzinier JP, Briley M: Biochemical profile of midalcipran (F 2207), 1-phenyl-1-diethyl-aminocarbonyl-2-aminomethyl-cyclopropane (Z) hydrochloride, a potential fourth generation antidepressant drug. In: Neuropharmacology. 24, Nr. 12, 1985, S. 1211–9. doi:10.1016/0028-3908(85)90157-1. PMID 3005901.
- Christian Puozzo, Simone Lens, Christian Reh, Karl Michaelis, Dominique Rosillon, Xavier Deroubaix, Dominique Deprez: Lack of Interaction of Milnacipran with the Cytochrome P450 Isoenzymes Frequently Involved in the Metabolism of Antidepressants. In: Clinical Pharmacokinetics. 44, Nr. 9, 2005, S. 977–88. PMID 16122284.
- Puozzo C, Albin H, Vinçon G, Deprez D, Raymond JM, Amouretti M: Pharmacokinetics of milnacipran in liver impairment. In: European Journal of Drug Metabolism and Pharmacokinetics. 23, Nr. 2, 1998, S. 273–9. PMID 9725493.
- Puozzo C, Pozet N, Deprez D, Baille P, Ung HL, Zech P: Pharmacokinetics of milnacipran in renal impairment. In: European Journal of Drug Metabolism and Pharmacokinetics. 23, Nr. 2, 1998, S. 280-6. PMID 9725494.
Weblinks
- Öffentlicher Beurteilungsbericht (EPAR) der europäischen Arzneimittelagentur (EMA) zu: Milnacipran