Borsäuretrimethylester
Borsäuretrimethylester (Trimethylborat) ist eine chemische Verbindung aus der Gruppe der Borsäureester. Es ist der Methylester der Borsäure.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
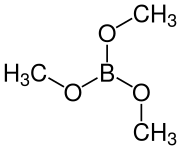 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Borsäuretrimethylester | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C3H9BO3 | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit angenehmem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 103,91 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
0,923 g·cm−3 (20 °C)[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
68,7 °C[2] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
Zersetzung mit Wasser[1] | |||||||||||||||
| Brechungsindex |
1,3568 (20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Darstellung
Borsäuretrimethylester entsteht durch Veresterung von Borsäure mit Methanol in Gegenwart saurer Katalysatoren in einer Gleichgewichtsreaktion:[5]
Zur Verschiebung des Gleichgewichtes auf die rechte Seite ist es jedoch nötig, dem Reaktionsgemisch eines der Produkte zu entziehen (Prinzip von Le Chatelier). Die sich bei Veresterungen häufig anbietende Methode ist die Bindung des Wassers durch wasserentziehende Mittel wie beispielsweise Schwefelsäure, welche gleichzeitig als saurer Katalysator wirkt.
Die Umsetzung von Bortrioxid führt zur Bildung eines Gemisches verschiedener Borsäureester.
Eine dritte Möglichkeit besteht in der Umsetzung von Borhalogeniden mit Methanol in Gegenwart einer Base wie im folgenden Beispiel mit Bortribromid:
Der entstehende Halogenwasserstoff (im Beispiel Bromwasserstoff) wird durch die Base gebunden.
Eigenschaften

Borsäuretrimethylester ist eine farblose, flüchtige Flüssigkeit. In Wasser wird sie zügig in Borsäure und Methanol hydrolysiert. Die Hydrolyse verläuft mit −19,3 kJ·mol−1 exotherm.[6] Sie ist der einfachste Borsäureester. Als Verbindung des Bors brennt sie mit kräftig hellgrün gefärbter Flamme. Weil keine C–C-Bindungen vorliegen, entsteht bei der Verbrennung kein Ruß, der in der Flamme gelb glüht und so die Flammenfärbung überstrahlt (eine große Ethanolflamme hat bereits eine gelbliche Flamme, Alkane brennen mehr oder weniger hell). Bei der Verbrennung entsteht nicht flüchtiges, weißes Bortrioxid, das Säureanhydrid der Borsäure, welches die Flamme rauchen lässt:
Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 4,74371, B = 1476,192 und C = −29,0 im Temperaturbereich von 304 K bis 340,5 K.[7] Die Verbindung bildet entzündbare Dampf-Luft-Gemische. Der Flammpunkt liegt bei −18 °C.[2]
Verwendung
Reiner Borsäuretrimethylester findet technisch wenig Anwendung. Er dient in geringem Maße zur Oberflächenvergütung von Stahl (Bildung einer korrosionshemmenden Fe2B-Schicht) in speziellen Plasmaverfahren. Borsäuretrimethylester findet als Ausgangssubstanz für Borsäure-Edukte der Suzuki-Kupplung Verwendung. Weiterhin wird Borsäuretrimethylester als Flussmittel zum Löten in sogenannten „Gasflux“-Verfahren eingesetzt.
Die durchgehend grüne Flammenfärbung des Esters kann analytisch als Indiz für die Anwesenheit von Borsäure/Boraten bzw. Methanol (die Borsäureester höherer Alkohole liefern nur grüne Flammensäume) dienen, ist jedoch nicht eindeutig. Sie ist jedoch sehr empfindlich und wird schon durch Spuren von Borsäure verursacht (zum Beispiel aus dem häufig in Laboren verwendeten Borosilicatgläsern stammend).
In der Nukleartechnik wird der Borsäuretrimethylester als Absorptionsmittel für Neutronen verwendet.[8]
Weblinks
Einzelnachweise
- Eintrag zu Trimethylborat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. Januar 2017. (JavaScript erforderlich)
- G. Sorbe: Sicherheitstechnische Kenndaten. 100. Ergänzungslieferung 6/2004, ecomed-Verlag, ISBN 3-609-73060-9.
- Datenblatt Borsäuretrimethylester (PDF) bei Merck, abgerufen am 24. Juli 2013.
- Eintrag zu Trimethyl borate im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Grüne Flammen (Bildung von Borsäuremethylester) (PDF; 9 kB).
- Charnley, T.; Skinner, H.A.; Smith, N.B.: Thermochemistry of Organo-boron Compounds. Part I. Esters of Boric Acid, in: J. Chem. Soc., 1952, S. 2288–2291 (doi:10.1039/JR9520002288).
- P. M. Christopher, A. Shilman: Vapor Pressures of Trialkyl Borates, in: J. Chem. Eng. Data, 1967, 12, S. 333–335 (doi:10.1021/je60034a012).
- Herder Lexikon Chemie. Gütersloh 1985, Buch-Nr. 03838 0, S. 43.


