2-Butin-1,4-diol
2-Butin-1,4-diol (nach IUPAC-Nomenklatur: But-2-in-1,4-diol, vereinfacht oft nur als Butindiol bezeichnet) ist eine organisch-chemische Verbindung aus der Stoffgruppe der Alkohole, genauer der Alkinole. Der Stoff kommt als 34%ige wässrige Lösung sowie als kristalline Flocken in den Handel. Es ist ein Zwischenprodukt der chemischen Industrie, welches zu zahlreichen Produkten weiterverarbeitet wird.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
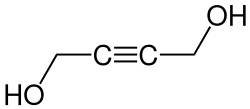 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 2-Butin-1,4-diol | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C4H6O2 | ||||||||||||||||||
| Kurzbeschreibung |
farbloser, kristalliner Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 86,09 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,11 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
238 °C[1] | ||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK | |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Die großtechnische Herstellung von 2-Butin-1,4-diol erfolgt praktisch ausschließlich durch das Reppe-Verfahren (Ethinylierung), welches von Walter Reppe und seinen Mitarbeitern bei der BASF in den 1930er Jahren gefunden und kontinuierlich weiterentwickelt wurde. Danach wird Acetylen mit wässriger, etwa 30–50%iger Formaldehyd-Lösung bei Temperaturen von 80–110 °C und einem Druck von 5–20 bar umgesetzt:[5] Die Umsetzung verläuft mit einer Reaktionswärme von −100,5 kJ·mol−1 exotherm.[6]
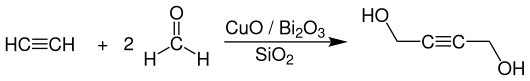
Als Katalysator wird ein System aus Kupfer(II)-oxid (CuO) und Bismut(III)-oxid (Bi2O3), welches auf Kieselgel (SiO2) geträgert ist, eingesetzt. Unter den Reaktionsbedingungen im Reaktor bildet sich durch Komplexierung von Acetylen das katalytisch aktive Kupfer(I)-acetylid (Cu2C2). Bismutoxid wird als Promotor (3–6 %) zugesetzt, um die Bildung von Cuprenen zu unterdrücken. Etabliert ist die Durchführung im Dreiphasensystem in einer Kaskade von drei bis fünf Rieselbettreaktoren, in denen der Katalysator als Festbett angeordnet ist und von der wässrigen Formaldehyd-Lösung überströmt wird. Dabei strömt im Gleich- oder Gegenstrom das Acetylen hinzu. Die Selektivität erreicht etwa 95 %.[6][7]
Eine Großanlage zu dieser Synthesemethode wurde bereits 1941 gebaut.[8]
Eine Weiterentwicklung des klassischen Reppe-Prozesses ist das Linde/Yukong-Verfahren. Danach wird Acetylen schon bei geringen Drücken (Partialdruck von Acetylen: 0,7–1,4 bar) mit Formaldehyd an einem modifizierten Cu-Katalysator auf einem Silikatträger bei Temperaturen von 70–90 °C in einer Kaskade aus vier kontinuierlich betriebenen Suspensionsrührkesseln umgesetzt.[9]
Die europäische Jahresproduktion von 2-Butin-1,4-diol beträgt etwa 200.000 t.[10]
Die wichtigsten Produzenten von 2-Butin-1,4-diol in Westeuropa sind BASF in Ludwigshafen am Rhein und INEOS Solvents (früher GAF, später ISP Marl GmbH) in Marl.
Eigenschaften
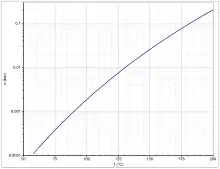
Butindiol ist ein farbloser Feststoff, der bei 58 °C schmilzt. Der Siedepunkt bei Normaldruck liegt bei 238 °C.[11] Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend ln(P) = A−(B/(T+C)) (P in Torr, T in °C) mit A = 9,7532, B = 3603,0 und C = 273,15 im Temperaturbereich von 112 bis 165 °C.[12] Die Schmelze bildet bei erhöhter Temperatur entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt bei 136 °C.[12][1] Die Zündtemperatur beträgt 335 °C.[12][1] Der Stoff fällt somit in die Temperaturklasse T2. Bei thermischer Belastung kann in Gegenwart katalytisch wirkender Verunreinigungen, wie Alkali- und Erdalkalihydroxyde oder -halogenide sowie starken Säuren eine heftige bis explosionsartige Zersetzung erfolgen.[13] Eine langsame thermische Zersetzung wird bei Temperaturen oberhalb von 160 °C beobachtet.[6]
Verwendung
Butindiol ist Ausgangspunkt zur Synthese weiterer Diole. So kann es durch Hydrierung zu 1,4-Butendiol und weiter zu 1,4-Butandiol umgesetzt werden.[9] Weiterhin wird es zur Herstellung von Arzneistoffen, z. B. als Rohmaterial für Vitamin B6, Entlaubungsmitteln, Flammschutzmitteln, Korrosionsschutzmitteln, Weichmachern und Polyurethanen (kettenverlängerndes Mittel) verwendet.[14] Es dient auch als Glanzbildner in Galvanisierungsbädern (bei Nickel und Kupfer) und als Sparbeizenzusatz zur Entfernung von Kesselstein oder Oxidschichten auf Metallen sowie in Abbeizmitteln für Farben.[15]
Sicherheitshinweise
2-Butin-1,4-diol zersetzt sich leicht in der Wärme (ab 160 °C), wobei die Reaktion bei Anwesenheit von Verunreinigungen oder bei höheren Temperaturen sehr heftig ausfallen kann (Flammpunkt 136 °C).[1][10]
Weblinks
- ECHA: Risikoanalyse zu Butindiol (PDF-Datei; 897 kB, englisch)
Einzelnachweise
- Eintrag zu 2-Butin-1,4-diol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- Eintrag zu But-2-in-1,4-diol. In: Römpp Online. Georg Thieme Verlag, abgerufen am 1. Oktober 2019.
- Eintrag zu But-2-yne-1,4-diol im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Oktober 2019. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 110-65-6 bzw. 2-Butin-1,4-diol), abgerufen am 1. Oktober 2019.
- Hans-Jürgen Arpe: Industrielle Organische Chemie – Bedeutende Vor- und Zwischenprodukte. 6. Auflage. WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim 2007, ISBN 978-3-527-31540-6, S. 108.
- Heinz Gräfje, Wolfgang Körnig, Hans-Martin Weitz, Wolfgang Reiß, Guido Steffan, Herbert Diehl, Horst Bosche, Kurt Schneider, Heinz Kieczka, Rolf Pinkos: Butanediols, Butenediol, and Butynediol. In: Ullmann’s Encyclopedia of Industrial Chemistry. Wiley‐VCH Verlag GmbH & Co. KGaA., 23. Juli 2019, doi:10.1002/14356007.a04_455.pub2
- Patent EP2121549B1: Verfahren zur Herstellung von 1,4-Butandiol. Veröffentlicht am 7. Juni 2017, Anmelder: BASF SE, Erfinder: Rolf Pinkos, Rudolf Erich Lorenz, York Alexander Beste.
- Geschichte der BASF (Memento vom 29. September 2007 im Internet Archive).
- Linde/Yukong-Verfahren zur Herstellung von Butandiol über Butindiol (Memento vom 29. September 2007 im Internet Archive) (PDF-Datei; 37 kB)
- Toxikologische Bewertung von Butindiol (PDF) bei der Berufsgenossenschaft Rohstoffe und chemische Industrie (BG RCI), abgerufen am 22. August 2012.
- CRC Handbook of Data on Organic Compounds, 2nd Editon, Weast,R.C and Grasselli, J.G., ed(s)., CRC Press, Inc., Boca Raton, FL, 1989, 1.
- Chemsafe Datenbank für sicherheitstechnische Kenngrößen im Explosionsschutz, PTB Braunschweig/BAM Berlin, abgerufen am 14. Dezember 2021.
- P.G. Urben; M.J. Pitt: Bretherick's Handbook of Reactive Chemical Hazards. 8. Edition, Vol. 1, Butterworth/Heinemann 2017, ISBN 978-0-08-100971-0, S. 339.
- Datenblatt 2-Butyne-1,4-diol (Crystal) (Memento vom 18. März 2014 im Internet Archive) bei BASF, abgerufen am 18. Dezember 2014.
- Datenblatt 2-Butin-1,4-diol bei Gischem, abgerufen am 18. Dezember 2014.


