Thiamin
Thiamin, Vitamin B1 oder Aneurin ist ein wasserlösliches Vitamin aus dem B-Komplex von schwachem, aber charakteristischem Geruch und ist insbesondere für die Funktion des Nervensystems unentbehrlich. Wird das Vitamin B1 für ca. 14 Tage dem Körper nicht mehr zugeführt, sind die Reserven zu 50 % aufgebraucht.
| Strukturformel | |||||||||
|---|---|---|---|---|---|---|---|---|---|
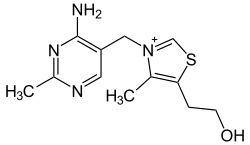 | |||||||||
| Struktur von Thiaminchlorid | |||||||||
| Allgemeines | |||||||||
| Trivialname | Vitamin B1 | ||||||||
| Andere Namen |
| ||||||||
| Summenformel |
| ||||||||
| CAS-Nummer | |||||||||
| ATC-Code |
A11DA01 | ||||||||
| Kurzbeschreibung | farbloses Pulver, charakteristischer Geruch | ||||||||
| Vorkommen | siehe Tabelle im Artikeltext | ||||||||
| Physiologie | |||||||||
| Funktion | Kohlenhydratstoffwechsel, Coenzym bei dehydrierenden Decarboxylierungsreaktionen (z. B. im Pyruvatdehydrogenasekomplex) | ||||||||
| Täglicher Bedarf | 1,0–1,2 mg | ||||||||
| Folgen bei Mangel | Muskelatrophie, Herzinsuffizienz, neurologische Störungen, Beriberi, Wernicke-Enzephalopathie | ||||||||
| Überdosis | nicht bekannt | ||||||||
| Eigenschaften | |||||||||
| Molare Masse | 337,27 g·mol−1 (Hydrochlorid) | ||||||||
| Aggregatzustand | fest | ||||||||
| Schmelzpunkt | |||||||||
| Löslichkeit | sehr gut löslich in Wasser (500 g·l−1[2]) | ||||||||
| Sicherheitshinweise | |||||||||
| |||||||||
| Toxikologische Daten | |||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||
Chemische Struktur
Thiamin besteht aus zwei Ringsystemen, die durch eine Methylenbrücke miteinander verbunden sind: einem Pyrimidin- und einem Thiazolring.
Funktion
Thiamin wird im Darm über den aktiven Thiamintransporter und in hohen Konzentrationen vorliegend auch durch Diffusion aufgenommen. Es existieren seltene erbliche Mangelkrankheiten dieser Proteine. Bei der Thiamin-responsiblen, megaloblastären Anämie (TRMA) kommt es durch Mutationen im SLC19A2-Gen zur Funktionsunfähigkeit des aktiven Thiamintransporters. Hierdurch kann das in der Nahrung in niedrigen Konzentrationen vorliegende Thiamin nicht mehr ausreichend aufgenommen werden. Dies führt zum charakteristischen Krankheitsbild der TRMA mit einem Diabetes mellitus, Schwerhörigkeit und einer megaloblastären Anämie. Unbehandelt führt die TRMA zum Tode. Durch Verabreichung einer hohen Dosis von Thiamin kann ausreichend Thiamin über den Darm durch Diffusion aufgenommen werden.[6]
Thiamin selbst wird im Körper nicht verwendet. Mithilfe des Enzyms Thiaminpyrophosphokinase wird es zunächst zu Thiaminpyrophosphat (TPP, auch Thiamindiphosphat, TDP) umgewandelt. In dieser biologisch aktiven Form ist es Coenzym der Pyruvatdehydrogenase E1, der α-Ketoglutarat-Dehydrogenase, der α-Ketosäure-Dehydrogenase und der Transketolase.
Glucosestoffwechsel und Mitochondrien
Mittels Pyruvatdehydrogenase-Komplex (PDC) wird in den Mitochondrien Pyruvat zu Acetyl-CoA umgebaut. TPP dient diesem Enzymkomplex als Coenzym bei der Abspaltung von CO2[7] und macht damit die aerobe Verwertung von Glucose (und damit auch anderer Kohlenhydrate) erst möglich.[8]
Ist dieser Stoffwechselweg blockiert, wird im Cytosol aus Pyruvat durch Milchsäuregärung Lactat erzeugt, was eine vergleichsweise ineffiziente Form der Energiegewinnung darstellt.[9]
Verluste in Nahrungsmitteln
Thiamin ist hitzeempfindlich, es wird durch Kochen zerstört. Es ist wasserlöslich, dadurch geht beim Kochen in Wasser ein Teil ins Kochwasser verloren. In rohem Fisch und Farnen ist das Enzym Thiaminase enthalten, das Thiamin abbaut und somit vernichtet. Konservierungsstoffe aus der Gruppe der Sulfite (E 220 – E 228)[10] zersetzen ebenfalls Thiamin.
Bei der Herstellung von weißem Mehl (z. B. Typ 405) oder weißem Reis wird der braune Keim der Pflanze vom Rest des Samens (Endosperm) entfernt.[11] Der Keim enthält jedoch das gesamte Vitamin B1 des Samens, welches zur Verbrennung der enthaltenen Kohlenhydrate benötigt wird.
Im Gegensatz dazu bleibt in Vollkornmehl, braunem Reis oder parboiled Reis das Vitamin B1 weitestgehend enthalten.
Anreicherung in Lebensmitteln
Um den Verlust bei der Verarbeitung auszugleichen, wird in vielen Ländern dem Mehl und Reis das Vitamin B1 wieder künstlich zugesetzt. Inzwischen verfahren 71 Länder bei Mehl so, darunter Großbritannien, USA und Kanada, jedoch nicht Deutschland.[12] Thiaminhydrochlorid ist in der EU durch die Verordnung (EG) Nr. 1334/2008 unter der FL-Nummer 16.027 als Aromastoff zugelassen.
Nahrungsergänzungsmittel
In Deutschland und anderen EU-Ländern ist Thiamin in folgender Form in Nahrungsergänzungsmitteln (NEM) erlaubt:
- Thiaminhydrochlorid
- Thiaminmononitrat
- Thiaminmonophosphatchlorid
- Thiaminpyrophosphatchlorid
Wenn mindestens 0,17 mg Thiamin pro Tagesdosis (etwa 15 % des Referenzwertes) in NEMs erhalten ist, darf mit der Aufrechterhaltung normaler Körperfunktionen geworben werden: Energiestoffwechsel, psychischen Funktion, Funktion des Nervensystems und Herzfunktion.[11] Eine Werbung für eine angebliche zusätzliche Leistungssteigerung ist nicht belegt. Auch für eine postulierte Wirksamkeit bei Nervenschmerzen (neuropathische Schmerzen) fehlen Wirksamkeitsnachweise und dürfen nicht beworben werden.[11]
Vorkommen
Pro 100 g der folgenden Lebensmittel sind laut Bundeslebensmittelschlüssel (BLS) bzw. Römpp Lexikon Chemie die angegebenen Mengen Thiamin enthalten:
| Nahrungsmittel | Thiamin mg/100 g |
|---|---|
| Bierhefe, biologisch | 13,0 |
| Weizenkeime | 2,01 |
| Bienenpollen | 0,6 bis 2,2[13][14] |
| Sonnenblumenkerne, frisch | 1,9 |
| Back-/Bierhefe, gepresst | 1,0 |
| Sojabohnen, frisch | 0,44 |
| Sesam, geröstet | 0,4 |
| Kamut (Khorasan-Weizen) | 0,40 |
| Vollkorngetreide (Weizen, Gerste, Mais, Reis – nicht erhitzt) | 0,35–0,46 |
| Teff (äthiopisch-eritreisches Süßgras) | 0,3 |
| Erbsen, grün, frisch | 0,3 |
| Macadamianüsse, frisch | 0,28 |
| Schweinefleisch (mittelfett), frisch | 0,23 |
| Löwenzahn, frisch | 0,19 |
| Austernseitling, frisch | 0,17 |
| Bohnen, weiß, gegart | 0,154 |
| Haferflocken, roh | 0,15 |
| Geflügel, gegart | 0,11 |
| Pellkartoffeln gegart | 0,07 |
Bedarf (Zufuhrempfehlung)
- Säuglinge (bis 12 Monate): 0,2–0,4 mg/Tag[15]
- Kinder (1–15 J.):
- Frauen: 1,0 mg/Tag[15]
- Männer 1,1–1,3 mg/Tag[15]
Der Bedarf korreliert mit dem täglichen Energieverbrauch. Daher benötigen Männer und junge Erwachsene etwas mehr Vitamin B1.[11]
In Südamerika wird häufig Thiamingabe vor Reisen in das Amazonasgebiet als Abwehr gegen Moskitos eingesetzt, da die Mücken den Geruch ablehnen würden. Die Schutzwirkung ist individuell verschieden und wird von zahlreichen Autoren angezweifelt.
Thiamin wird im Blut, in der Leber, der Niere, im Gehirn und in den Muskeln gespeichert, wenngleich die Speicherfähigkeit mit 25–30 mg eher niedrig ist.[11]
Versorgungssituation in Deutschland
Laut der Nationalen Verzehrstudie II von Mitte der 2000 Jahre liegt in allen Altersgruppen der Median der Vitamin-B1-Zufuhr deutlich über der empfohlenen Zufuhr, jedoch erreichen 21 % der Männer und 32 % der Frauen die empfohlene tägliche Zufuhr von Vitamin B1 nicht.[16] Daraus resultiert aber nicht notwendigerweise ein Mangel.[11]
Mangelerscheinungen (Hypovitaminose)
Bereits 1896 stellte Christiaan Eijkman nach seiner Rückkehr von seiner Asienreise nach Europa fest: „Weißer Reis kann giftig sein!“ Zuvor hatte er in Java gehäuft Fälle von Beriberi beobachtet, die durch eine gründlichere Politur des weißen Reises verursacht wurde.[17] Mangelerscheinungen treten insbesondere in Ländern auf, in denen weißer Reis das Grundnahrungsmittel darstellt und noch einseitig gegessen wird.[11]
Symptome:
- Störungen des Kohlenhydratstoffwechsels und Nervensystems (u. a. Polyneuropathie)
- Reizbarkeit und Depressionen
- Müdigkeit, Sehstörungen, Appetitlosigkeit, Konzentrationsschwäche, Muskelatrophie
- Blutarmut (Anämie)
- häufige Kopfschmerzen
- Gedächtnisstörungen (Korsakow-Syndrom), Verwirrungszustände
- Herzversagen, Ödeme, Tachykardie, niedriger Blutdruck, Kurzatmigkeit (Dyspnoe)
- Verringerte Produktion von Antikörpern bei Infektionen
- gestörte Energieproduktion
- schwache Muskulatur (besonders die Wadenmuskulatur)
- Krankheiten:
- Mensch: Beriberi, Wernicke-Enzephalopathie, Strachan-Syndrom
- Tiere: Thiaminmangel-Enzephalopathie der Katze, Zerebrokortikalnekrose, Chastek-Paralyse
In Europa können bestimmte Risikogruppen von einem Mangel betroffen sein, z. B. Alkoholiker, Menschen mit bestimmten Magen-Darm- oder Leberkrankheiten und Frauen mit extremer Schwangerschaftsübelkeit.[11]
Alzheimer
Alzheimer-Patienten zeigen eine verminderte Glucose- und Sauerstoffverwertung im Gehirn, die mit einem Thiaminmangel einhergeht.[18][19] Der Mangel könnte nicht nur die Folge, sondern die Ursache der Krankheit sein.[20] Auch können erniedrigte Thiaminpyrophosphat-Werte in Blut und Gehirn als Diagnosekriterium zur Abgrenzung von Alzheimer zu anderen Formen der Demenz verwendet werden.[21]
Folgen einer Überdosierung (Hypervitaminose)
Thiamin besitzt eine große therapeutische Breite. So zeigen tierexperimentelle Befunde bei Ratten, dass selbst eine 100fach über dem täglichen Bedarf liegende Dosis über drei Generationen ohne Nebenwirkungen vertragen wurde. Nach Verabreichung in den Muskel bzw. in die Vene wurden allerdings in Einzelfällen teils schwerste Überempfindlichkeitsreaktionen bis hin zu Atemnot und Schockzuständen beschrieben. Wegen dieser allergischen Reaktionen sollte Vitamin B1 daher nur in Ausnahmefällen parenteral angewendet werden; orale Therapie der Wahl zur Vitamin-B1-Substitution ist die fettlösliche und dadurch hervorragend gewebegängige Thiamin-Prodrug Benfotiamin.
Da bei Verzehr auch in hohen Mengen keine nachteiligen gesundheitlichen Folgen beobachtet wurden (oral aufgenommenes Thiamin wird über den Urin ausgeschieden),[11] hat das BfR auf eine Festlegung von Höchstmengen verzichtet.[22]
Geschichte
- 1882 erkannte der Japaner Kanehiro Takaki, dass die schon um 2600 v. Chr. in China bekannte Beriberi-Krankheit durch zweckmäßige Ernährung (aus dem Vitamin-B-Bereich) geheilt werden kann.
- 1897 wies der Nobelpreisträger für Medizin/Physiologie (Nobelpreis 1929) Christiaan Eijkman Vitamin-B1-Mangeleffekte durch das Füttern von poliertem Reis nach und zeigte, dass durch die Verfütterung der Silberhäutchen (Kleie) des Reises der Mangel behoben werden kann. Wegen seiner Wirkung auf die Nerven wurde es zunächst anti-polyneuritis factor genannt.
- 1910 entdeckte Umetaro Suzuki das Thiamin, als er untersuchte, warum Reiskleie Beriberi-Kranke heilte. Er nannte es erst aberic acid und später Oryzanin.
- 1912 isolierte Casimir Funk aus Reiskleie Niacin, hielt es aber fälschlicherweise für Thiamin und prägte aufgrund der angeblich entdeckten Aminogruppe den Begriff „Vitamin“.[23][24]
- 1926 wurde das Vitamin erstmals von Barend C.P. Jansen und Willem F. Donath in kristalliner Form aus Reiskleie isoliert und als antineuritisches Vitamin (Aneurin) bezeichnet.[1]
- 1932 erhielt es dann aber von Windaus wegen seines Schwefelgehaltes die Bezeichnung Thiamin, die heute der einzig zulässige Name ist.
- 1936 wurde die Struktur von Vitamin B1 etwa gleichzeitig von Robert R. Williams und Rudolf Grewe aufgeklärt.[1] Die Synthese erfolgte durch Robert R. Williams und von Hans Andersag und Kurt Westphal 1937.
- 1952 entdeckte die japanische Forschergruppe um Fujiwara das fettlösliche Thiamin-Prodrug Benfotiamin, mit dem sich hohe Thiaminspiegel in den Zielorganen erreichen lassen.
Weblinks
- Höchstmengen für Vitamin B1, Vitamin B2 und Pantothensäure in Lebensmitteln inklusive Nahrungsergänzungsmitteln. (PDF) In: Bundesinstitut für Risikobewertung. 2021, abgerufen am 6. Januar 2022.
Einzelnachweise
- Eintrag zu Thiamin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 19. April 2016.
- Eintrag zu Thiamine in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- Datenblatt Thiamine hydrochloride bei Sigma-Aldrich, abgerufen am 25. Juni 2017 (PDF).
- Zhongguo Yaoxue Zazhi. In: Chinese Pharmaceutical Journal. Vol. 30, 1995, S. 407.
- E. T. ANGELAKOS, E. R. LOEW: Histamine toxicity in mice and rats following treatment with histaminase inhibitors. In: Journal of Pharmacology and Experimental Therapeutics. Band 119, Nummer 3, März 1957, S. 444–451, PMID 13417100.
- Thiamin-responsive megaloblastäre Anämie mit Diabetes mellitus und sensorineuraler Schwerhörigkeit. In: Orphanet (Datenbank für seltene Krankheiten).
- Jane B. Reece, Lisa A. Urry, Michael L. Cain, Steven A. Wasserman, Peter V. Minorsky: Campbell Biology. 10. Auflage. Benjamin-Cummings Pub Co, 2014, ISBN 978-0-13-404462-0, S. 894.
- Michael M. Cox, Albert L. Lehninger: Lehninger principles of biochemistry. W.H. Freeman and Company, 2013, ISBN 978-1-4292-3414-6, S. 567–569.
- Lisa A. Urry, Michael L. Cain (Michael Lee), Steven Alexander Wasserman, Peter V. Minorsky, Rob Jackson: Campbell biology. 10. Auflage. ISBN 978-0-321-77565-8, S. 178–179.
- Eintrag zu Schwefeldioxid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 8. Februar 2016.
- Vitamin B1 (Thiamin) für Herz und Nerven? In: Verbraucherzentrale. 22. März 2021, abgerufen am 26. April 2021.
- Vitaminreich: Mehl für die Welt. auf: muehlenchemie.de
- E. W. HERBERT, J. T. VANDERSLICE, MEIS-HSIA HUANG, D. J. HIGGS: LEVELS OF THIAMINE AND ITS ESTERS IN BEE COLLECTED POLLEN USING LIQUID CHROMATOGRAPHY AND ROBOTICS. In: Apidologie. Band 18, Nr. 2, 1987, S. 129–136, doi:10.1051/apido:19870203 (apidologie.org [abgerufen am 9. August 2017]).
- Vanilda Aparecida Soares de Arruda, Aline Aparecida Santos Pereira, Leticia M. Estevinho, Ligia Bicudo de Almeida-Muradian: Presence and stability of B complex vitamins in bee pollen using different storage conditions. In: Food and Chemical Toxicology: An International Journal Published for the British Industrial Biological Research Association. Band 51, Januar 2013, S. 143–148, doi:10.1016/j.fct.2012.09.019, PMID 23022013.
- DGE: Die Referenzwerte für die Nährstoffzufuhr: Thiamin (Vitamin B1)
- Max Rubner-Institut, Bundesforschungsinstitut für Ernährung und Lebensmittel (Hrsg.): Nationale Verzehrstudie II. Ergebnisbericht, Teil 2. Karlsruhe 2008, S. 113 ff. (bund.de [PDF]).
- Christiaan Eijkman: Beriberi and Vitamin B1. (Memento vom 24. Januar 2018 im Internet Archive), abgerufen am 4. Februar 2017.
- Gary E. Gibson, Joseph A. Hirsch, Pasquale Fonzetti, Barry D. Jordan, Rosanna T. Cirio: Vitamin B1 (thiamine) and dementia. In: Annals of the New York Academy of Sciences. Band 1367, Nr. 1, 1. März 2016, S. 21–30, doi:10.1111/nyas.13031, PMID 26971083, PMC 4846521 (freier Volltext).
- Gary E. Gibson, Joseph A. Hirsch, Rosanna T. Cirio, Barry D. Jordan, Pasquale Fonzetti: Abnormal thiamine-dependent processes in Alzheimer's Disease. Lessons from diabetes. In: Molecular and Cellular Neurosciences. Band 55, 1. Juli 2013, S. 17–25, doi:10.1016/j.mcn.2012.09.001, PMID 22982063, PMC 3609887 (freier Volltext).
- Lack of Vitamin B1 May Lead to Alzheimer's. Abgerufen am 6. Februar 2017.
- Xiaoli Pan, Guoqiang Fei, Jingwen Lu, Lirong Jin, Shumei Pan: Measurement of Blood Thiamine Metabolites for Alzheimer's Disease Diagnosis. In: EBioMedicine. Band 3, 1. Januar 2016, S. 155–162, doi:10.1016/j.ebiom.2015.11.039, PMID 26870826, PMC 4739421 (freier Volltext).
- Höchstmengen für Vitamin B1, Vitamin B2 und Pantothensäure in Lebensmitteln inklusive Nahrungsergänzungsmitteln. (PDF) In: Bundesinstitut für Risikobewertung. 2021, abgerufen am 26. April 2021.
- Casimir Funk: The etiology of the deficiency diseases. Beri-beri, polyneuritis in birds, epidemic deopsy, scurvy, experimental scurvy in animals, infantile scurvy, ship beri-beri, pellagra. In: Journal of State Medicine. 20, 1912, S. 341–368.
- Karim Bschir: Wissenschaft und Realität Mohr Siebeck, Tübingen 2012 ISBN 978-3-16-151934-5 S. 14–15