Thiaminpyrophosphat
Thiaminpyrophosphat (TPP), auch Thiamindiphosphat (TDP), ist ein Phosphatester des Thiamins (Vitamin B1). TPP ist die Coenzymform (Cocarboxylase) des Thiamins und dominiert in Zellen von Eukaryoten gegenüber dem Thiamin, da es bald aus diesem durch das Enzym Thiaminpyrophosphokinase synthetisiert wird.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
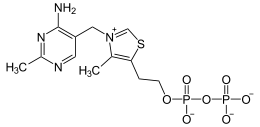 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Thiaminpyrophosphat | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C12H18N4O7P2S | ||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 424,30 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Löslichkeit |
gut in Wasser (220 g·l−1 bei 20 °C)[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Die früher verbreitete Ansicht, dass TPP überhaupt nicht aus der Zelle transportiert wird, ist falsch. Es ist mindestens ein Transportprotein bekannt, das in der Lage ist, in Säugetieren TPP zu transportieren.[3][4]
Eigenschaften
Thiaminpyrophosphat kristallisiert in zwei Hydratformen. Beide Formen, ein Tetrahydrat und ein 4,5-Hydrat bilden trikline Kristallgitter mit der Raumgruppe P1.[5][6]
Funktion
Mehrere TPP-abhängige Enzyme befinden sich an Schaltstellen des Zellstoffwechsels. Allgemein wirkt TPP an Aldehyd-Transferreaktionen mit. TPP ist die prosthetische Gruppe der Transketolase, einem Enzym des Pentosephosphatweges. Deren Aktivität in den roten Blutkörperchen ist ein Kriterium für die Beurteilung des Versorgungszustandes mit Thiamin.
Weitere Enzyme bei denen TPP als Coenzym fungiert:
- Pyruvat-Dehydrogenase (Oxidative Decarboxylierung von Pyruvat)
- α-Ketoglutarat-Dehydrogenase (Citratzyklus)
- Verzweigtketten-α-Ketosäure-Dehydrogenase (Abbau von Aminosäuren mit verzweigten Seitenketten)
- Acetolactat-Synthase (2,3-Butandiolgärung)
- Pyruvatdecarboxylase (Alkoholische Gärung)
- Pyruvatoxidase
- Indolpyruvatdecarboxylase
- Transketolase (Pentosephosphatweg)
Einzelnachweise
- Datenblatt Cocarboxylase chloride (PDF) bei Merck, abgerufen am 25. Januar 2013.
- Datenblatt Thiamine pyrophosphate, ≥95% bei Sigma-Aldrich, abgerufen am 27. Februar 2013 (PDF).
- R. Zhao, F. Gao, Y. Wang, G. A. Diaz, B. D. Gelb, I. D. Goldman: Impact of the reduced folate carrier on the accumulation of active thiamin metabolites in murine leukemia cells. In: J. Biol. Chem. Band 276, Nr. 2, Januar 2001, S. 1114–1118, doi:10.1074/jbc.M007919200, PMID 11038362.
- L. de Jong, Y. Meng, J. Dent, S. Hekimi: Thiamine pyrophosphate biosynthesis and transport in the nematode Caenorhabditis elegans. In: Genetics. Band 168, Nr. 2, Oktober 2004, S. 845–854, doi:10.1534/genetics.104.028605, PMID 15514058, PMC 1448845 (freier Volltext).
- J. Pletcher, M. Wood, G. Blank, W. Shin, M. Sax: Thiamine Pyrophosphate Tetrahydrate: A Structure with the Pyrophosphate Ester in an Extended Conformation. In: Acta Cryst. B 33, 1977, S. 3349–3359.
- J. Pletcher, G. Blank, M. Wood, M. Sax: Thiamin Pyrophosphate*4½H2O: A Second Polymorph of the Neutral Zwitterion. In: Acta Cryst. B 35, 1979, S. 1633–1637.