Dehydrohalogenierung
Eine Dehydrohalogenierung ist in der organischen Chemie eine Eliminierungsreaktion – häufig eine β-Eliminierungsreaktion oder β-Eliminierung – oder eine intramolekulare Substitutionsreaktion. Unter Abspaltung je eines Wasserstoff- und eines Halogenatoms aus derselben Verbindung entsteht ein Alken (bei 1,2-Stellung von Wasserstoff- und Halogenatom), ein Cyclopropanderivat (bei 1,3-Stellung von Wasserstoff- und Halogenatom) oder eine heterocyclische Verbindung. Die Dehydrohalogenierung kann als Dehydrofluorierung (Abspaltung von Fluorwasserstoff), Dehydrochlorierung (Abspaltung von Chlorwasserstoff), Dehydrobromierung (Abspaltung von Bromwasserstoff) etc. durchgeführt werden und läuft durch Einwirkung von Basen auf die entsprechenden Halogenalkane ab. Als Basen benutzt man Alkalilaugen, Amine, Alkylamide oder heterocyclische Stickstoffverbindungen, wie z. B. 1,5-Diazabicyclo[4.3.0]non-5-en (DBN).[1]
| Dehydrohalogenierung (X = Halogen) |
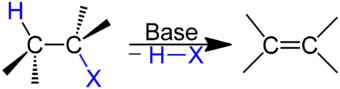 |
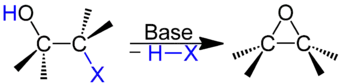 |
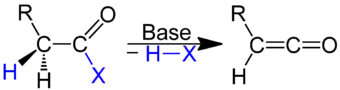 |
Aus 1,2- oder 1,1-Dihalogen-Verbindungen kann man unter Einwirkung von alkoholischer Kalilauge Halogenvinyl-Verbindungen synthetisieren.[2]
Weitere Beispiele für Dehydrohalogenierungen unter Einwirkung einer Base:[3]
- Bildung von Oxiranen aus β-Halogenalkanolen
- Bildung von Oxetanen aus γ-Halogenalkanolen
- Bildung von Aziridinen aus β-Halogenaminen
- Bildung von Azetidinen aus γ-Halogenaminen
- Bildung von Thiiranen aus β-Halogenthioalkanolen
- Bildung von Ketenen aus Carbonsäurehalogeniden mit einem Wasserstoffatom am α-Kohlenstoffatom[4]
Die Bildung des reaktionsfreudigen und instabilen Didehydrobenzols (ein Arin) aus Chlorbenzol ist auch eine Dehydrochlorierung.[5]
Reaktionsmechanismus
Man unterscheidet zwischen der monomolekularen Eliminierung (E1) und der bimolekularen Eliminierung (E2).[6] Daneben gibt es noch den Carbanion- oder E1cB-Mechanismus nach dem derartige β-Eliminierungen ablaufen können.[7]
Einzelnachweise
- Otto-Albrecht Neumüller (Hrsg.): Römpps Chemie-Lexikon. Band 2: Cm–G. 8. neubearbeitete und erweiterte Auflage. Franckh'sche Verlagshandlung, Stuttgart 1981, ISBN 3-440-04512-9, S. 883.
- Siegfried Hauptmann: Organische Chemie, 2. durchgesehene Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1985, S. 258, ISBN 3-342-00280-8.
- Siegfried Hauptmann: Organische Chemie, 2. durchgesehene Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1985, S. 558–563, ISBN 3-342-00280-8.
- Organikum, Wiley-VCH Verlag GmbH, 23. Auflage, 2009, S. 280–281, ISBN 978-3-527-32292-3.
- Ivan Ernest: Bindung, Struktur und Reaktionsmechanismen in der organischen Chemie, Springer-Verlag, 1972, S. 155, ISBN 3-211-81060-9.
- Ivan Ernest: Bindung, Struktur und Reaktionsmechanismen in der organischen Chemie, Springer-Verlag, 1972, S. 136–151, ISBN 3-211-81060-9.
- Siegfried Hauptmann: Organische Chemie, 2. durchgesehene Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1985, S. 229, ISBN 3-342-00280-8.