Salicylaldehyd
Salicylaldehyd ist eine natürlich in einigen Pflanzen und Insekten vorkommende chemische Verbindung, die heute vielfach als Duftstoff und in der pharmazeutischen und chemischen Industrie Verwendung findet. Es leitet sich sowohl vom Benzaldehyd als auch vom Phenol ab. Die Struktur besteht aus einem Benzolring mit angefügter Aldehyd- (–CHO) und Hydroxygruppe (–OH) als Substituenten. Salicylaldehyd gehört zur Gruppe der Hydroxybenzaldehyde.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
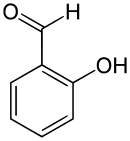 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Salicylaldehyd | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C7H6O2 | ||||||||||||||||||
| Kurzbeschreibung |
farblose bis gelbliche Flüssigkeit mit bittermandelartigem Geruch und brennendem Geschmack[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 122,13 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
197 °C[3] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| pKS-Wert |
6,79[5] | ||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Brechungsindex |
1,5734[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Geschichte
Ungefähr um 1838 gelang es dem Schweizer Apotheker und Pharmazeuten Johann Pagenstecher, aus den Blüten von Mädesüß Salicylaldehyd zu gewinnen.
Vorkommen
Insekten (Blattkäfer) produzieren diese Verbindung in speziellen Drüsen gegen Fraßfeinde aus dem Salicin ihrer Wirtspflanzen. Es kommt weiterhin in der Sumpf-Spierstaude oder Mädesüß (Filipendula ulmaria, früher: Spiraea ulmaria) vor.
Gewinnung und Darstellung
Früher wurde Salicylaldehyd durch die Reimer-Tiemann-Reaktion (1876, frühe Carbenchemie) gewonnen.[6] Dabei werden Chloroform, Kaliumhydroxid und Phenol als Ausgangsstoffe benutzt. Heute wird als Verbesserung eine Phasentransferkatalyse verwendet.
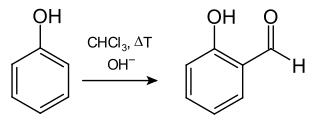
Eigenschaften
Salicylaldehyd besitzt gegenüber dem Phenol (9,99[5]) einen deutlich niedrigeren pKs-Wert von 6,79; die elektronenziehende Aldehydgruppe (−M-Effekt) erhöht die Acidität; die phenolische OH-Bindung wird zunehmend polarisiert.
Verwendung
Salicylaldehyd dient als Zwischenprodukt in der Farbstoff- und Arzneimittelindustrie sowie in 10%iger alkoholischer Lösung zum Nachweis von Ketonen (z. B. Aceton im Harn) und von Fuselölen im Alkohol. Außerdem wird er zur Herstellung von Schiffschen Basen, z. B. dem Komplexbildner N,N′-Bis(salicyliden)ethylendiamin (Abkürzung: salen), dessen Cobalt(II)-komplex (Salcomin) reversibel Sauerstoff binden kann, benutzt. Weiterhin wird es als Duftstoff in Parfüms eingesetzt.
Oxidation mit Wasserstoffperoxid ergibt Brenzcatechin (Dakin-Reaktion).[7]
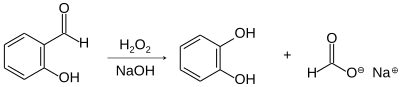
Cumarin wird mit der Perkinschen Synthese aus Salicylaldehyd und Essigsäureanhydrid hergestellt.[8]
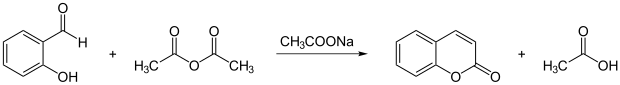
Literatur
- Edwin A. Robinson: The reaction of dichloromethylene with water and with phenoxide ions (Reimer–Tiemann reaction). In: J. Chem. Soc., 1961, S. 1663–1671; doi:10.1039/JR9610001663.
- Karl Winterfeld: Praktikum der organisch-präparativen Pharmazeutischen Chemie. 6. Auflage. Steinkopff.
Siehe auch
Einzelnachweise
- Eintrag zu SALICYLALDEHYDE in der CosIng-Datenbank der EU-Kommission, abgerufen am 19. Januar 2022.
- Eintrag zu Salicylaldehyd. In: Römpp Online. Georg Thieme Verlag, abgerufen am 2. April 2014.
- Eintrag zu Salicylaldehyd in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. Januar 2019. (JavaScript erforderlich)
- Datenblatt Salicylaldehyd (PDF) bei Merck, abgerufen am 22. April 2011.
- CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- P. Rademacher: Organische Chemie IV. (PDF; 203 kB)
- H. D. Dakin: Catechol In: Organic Syntheses. 3, 1923, S. 28, doi:10.15227/orgsyn.003.0028; Coll. Vol. 1, 1941, S. 159 (PDF).
- Erich Koepp, Fritz Vögtle: Perkin-Synthese mit Cäsiumacetat. In: Synthesis. Band 1987, Nr. 2, Januar 1987, doi:10.1055/s-1987-27880.

