Physostigmin
Physostigmin ist ein Indolalkaloid. Es wird in der Medizin bei bestimmten postoperativ auftretenden Störungen und als Gegenmittel bei Vergiftungen mit parasympatholytisch wirkenden Substanzen, die ein anticholinerges Syndrom bedingen, eingesetzt.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
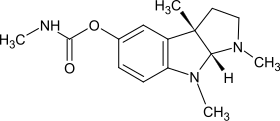 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Physostigmin | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C15H21N3O2 | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code | |||||||||||||||||||
| Wirkstoffklasse | |||||||||||||||||||
| Wirkmechanismus |
Cholinesterasehemmung | ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 275,35 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt |
102–104 °C[1] | ||||||||||||||||||
| pKS-Wert |
6,12; 12,24[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Vorkommen
.jpg.webp)
Die Samen der Kalabarbohne (Physostigma venenosum) und die Früchte des Manchinelbaums (Hippomane mancinella) enthalten Physostigmin.
Klinische Angaben
Physostigmin ist ein indirektes Parasympathomimetikum (Cholinergikum), d. h., es verstärkt die Wirkung des parasympathischen Nervensystems im Körper. Physostigmin verzögert als Acetylcholinesterase-Hemmer den Abbau von Acetylcholin und wirkt durch die Erhöhung der Acetylcholinkonzentration am Rezeptor indirekt parasympathomimetisch.
Am Herzen führt es zu einer Frequenzsenkung, an den Augen zu einer Miosis (Engstellung der Pupille), an den Bronchien zu einer Verengung und am Darm zu einer Anregung der Peristaltik.
Auch an der motorischen Endplatte entfaltet es seine Wirkung. Physostigmin ist ein tertiäres Amin und kann auf Grund seiner Struktur im Gegensatz zu den quartären Aminen wie z. B. Neostigmin die Blut-Hirn-Schranke überwinden und im ZNS seine Wirkung entfalten. Aus diesem Grunde wird es zur Behandlung des zentralen anticholinergen Syndroms (ZAS) eingesetzt, einer postoperativ auftretenden Störung, die durch etliche Anästhetika und in der Anästhesie verwendete Medikamente hervorgerufen werden kann.[5]
Ferner wurde der Einfluss von Physostigmin auf bestimmte Phasen in einem septischen Geschehen untersucht. So konnte gezeigt werden, dass das Immunsystem und das Zentralnervensystem (ZNS) sich gegenseitig beeinflussen können.
Der als „cholinergic antiinflammatory pathway (CAP)“[6] beschrieben efferenter Teil eines inflammatorischen Reflexbogens ist ein Mechanismus der neuronalen Inflammationskontrolle. So können Cholinesteraseinhibitoren durch Aktivierung des „cholinergic antiinflammatory pathway“ über das autonome Nervensystem die Freisetzung proinflammatorischer Zytokine in den Makrophagen hemmen. Über den efferenten Anteil des Nervus vagus, dem Neurotransmitter Acetylcholin und der α7-Subunit des nikotinischen Acetylcholinrezeptors werden also Zellen des Immunsystems erreicht. Sogenannte proinflammatorische Zytokine induzieren eine gesteigerte Freisetzung von Corticotropin-Releasing-Hormon (CRH) oder Arginin-Vasopressin (AVP) im Hypothalamus sowie des adrenocorticotropem Hormons (ACTH) in der Hypophyse. Die hierdurch verursachte gesteigerte Kortisolfreisetzung entfaltet seine antiinflammatorische Wirkung durch Suppression der NF-κB-Aktivierung und durch Aktivierung antiinflammatorischer Zytokine. Im Plexus coeliacus erfolgt wahrscheinlich die Weitergabe der Information an postsynaptische sympathische Nervenfasern, die zur Milz ziehen und dort auf Zellen des Immunsystems einwirken. Cholinesterase-Inhibitoren, wie das Physostigmin, führen in der experimentellen Sepsis zu antiinflammatorischen Effekten, wenn sie frühzeitig verabreicht werden.[7]
Pharmakologische Eigenschaften
Anwendung
Physostigmin wird als Gegenmittel bei Vergiftungen bzw. Überdosierungen durch
- Atropin, Hyoscyamin, Scopolamin (Tropanalkaloide), Strychnin
- Amphetamine,
- Trizyklische Antidepressiva,
- Phenothiazine,
- Benzodiazepine,
- Antihistaminika
- den chemischen Kampfstoff Benzilsäureester
und zur Behandlung von zentralen anticholinergen Syndromen eingesetzt. Weiterhin dient Physostigmin in der Augenheilkunde als Miotikum zur Pupillenverengung nach Verabreichung von Atropin zur Pupillenerweiterung, zur medikamentösen Therapie von Glaukomen sowie zur Senkung des Augeninnendrucks. Andere Acetylcholinesterasehemmstoffe wie z. B. Donepezil, Rivastigmin oder Galantamin werden zur Behandlung der Demenz eingesetzt.
Physostigmin und das ähnliche Carbamat Pyridostigmin werden zur Prophylaxe gegen Vergiftungen mit chemischen Kampfstoffen auf Cholinesteraseinhibitor-Basis eingesetzt.[8][9]
Nebenwirkungen
Als Nebenwirkungen können auftreten:
- Bei Überdosierung:
- Bradykardie
- Hypersalivation
- Erbrechen
- Krampfanfall
- Miosis
Gegenanzeigen
Physostigmin darf bei folgenden Krankheiten nicht verwendet werden:
- Asthma bronchiale,
- schweren peripheren Durchblutungsstörungen
- koronarer Herzerkrankung
- Harnverhalt oder Verstopfung durch eine mechanische Ursache
- Morbus Parkinson
Die gleichzeitige Gabe von anderen Cholinesterasehemmern muss wegen einer gegenseitigen Wirkungsverstärkung unterbleiben.
Literatur
- Ernst Mutschler: Arzneimittelwirkungen: Lehrbuch der Pharmakologie und Toxikologie. 7., völlig neu bearb. und erw. Auflage. Wiss. Verl.-Ges, Stuttgart 1996, ISBN 3-8047-1377-7.
- Rolf Kretschmer: Notfallmedikamente von A – Z: Klinik und Pharmakologie auf einen Blick. 5., aktualisierte Auflage. Wiss. Verl.-Ges., Stuttgart 2005, ISBN 3-8047-2133-8.
Handelsnamen
Anticholium (D, A), enthält Physostigminsalicylat
- ehemalige Kombinationspräparate
Eucard (D)[10]
Weblinks
- Eintrag zu Physostigmin bei Vetpharm, abgerufen am 11. August 2012.
Einzelnachweise
- Datenblatt Eserine bei Sigma-Aldrich, abgerufen am 20. April 2011 (PDF).
- Louis F. Fieser und Mary Fieser: Organische Chemie, 2. Auflage, Verlag Chemie 1982, ISBN 3-527-25075-1.
- Eintrag zu Physostigmine im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag zu Eserin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 23. Juli 2016. (JavaScript erforderlich)
- Peter M. Lauven, H. Stoeckel: Das zentrale anticholinerge Syndrom: Klinik und Therapie. Aktuelle Neuropädiatrie 1986, S. 177–185, doi:10.1007/978-3-642-47569-6_19.
- cholinerg antiinflammatorische Regelpfad
- Katja Weismüller, Michael Bauer, Stefan Hofer, Markus A. Weigand: Die Bedeutung der neuroendokrinen Achse in der Pathophysiologie der Sepsis. Anästhesiol Intensivmed Notfallmed Schmerzther, Georg Thieme Verlag Stuttgart (2010); 45(9): 574–579, doi:10.1055/s-0030-1265750.
- Saskia Eckert: Entwicklung eines dynamischen Modells zum Studium der Schutzeffekte reversibler Acetylcholinesterase-Hemmstoffe vor der irreversiblen Hemmung durch hochtoxische Organophosphate. München 2006, DNB 982657064, S. 1, urn:nbn:de:bvb:19-61966 (Dissertation).
- Szinicz, L. and Baskin, S. I.: Chemische und biologische Kampfstoffe. In: Lehrbuch der Toxikologie. W. V. mbH. Stuttgart: 865-895, 1999.
- Eucard. (Anzeige der Südmedica GmbH, München) In: Münchener Medizinische Wochenschrift. Jahrgang 1953, Nr. 1 (Januar) 1953, S. CXXXV.