Rivastigmin
Rivastigmin wird als Arzneistoff zur symptomatischen Behandlung der leichten bis mittelschweren Alzheimerschen Krankheit eingesetzt. Es ist das einzige Antidementivum, das zusätzlich eine Zulassung für die Behandlung der Parkinsondemenz hat. Rivastigmin kann oral (Hartkapsel, Lösung) und transdermal als Pflaster verabreicht werden.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
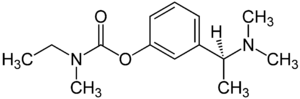 | |||||||||||||
| Allgemeines | |||||||||||||
| Freiname | Rivastigmin | ||||||||||||
| Andere Namen |
(S)-{3-[α-(Dimethylamino)ethyl]phenyl}-N-ethyl-N-methylcarbamat (IUPAC) | ||||||||||||
| Summenformel |
| ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Arzneistoffangaben | |||||||||||||
| ATC-Code |
N06DA03 | ||||||||||||
| Wirkstoffklasse | |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 250,34 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Schmelzpunkt |
123–125 °C [Rivastigmin-Hydrogen-(2R,3R)-tartrat] [1] | ||||||||||||
| Siedepunkt |
viskose Flüssigkeit bei Raumtemperatur [Rivastigmin-Base] [2] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Pharmakotherapeutisch gehört der Wirkstoff in die Gruppe der Cholinesteraseinhibitoren. Rivastigmin hemmt die Acetylcholinesterase und die Butyrylcholinesterase. Sinn dieser Hemmung ist es, den bei Alzheimer-Demenz auftretenden Mangel an Acetylcholin zu reduzieren. Durch die Hemmung der abbauenden Enzyme (Acetyl- und Butyrylcholinesterase) wird eine Verminderung des Abbaus von Acetylcholin erreicht und der Botenstoff steht weiter zur Verfügung. Aus diesem Grund kann Rivastigmin die bei der Alzheimer-Krankheit auftretenden cholinerg vermittelten kognitiven Defizite günstig beeinflussen und eine Verbesserung der Symptomatik erreichen.
In Studien zeigte sich ein geringer, aber signifikanter Effekt von Rivastigmin auf die kognitive Funktion und Lebensqualität.[4] Nebenwirkungen wie Übelkeit, Erbrechen, Durchfall, Anorexie, Kopfschmerzen und Synkopen führen allerdings zu hohen Abbruchraten (9 % höher als bei Placebo) der Behandlung.[5]
Mit der galenischen Zubereitungsform als Pflaster (TTS) wird eine gleichbleibende Abgabe des Wirkstoffes und damit gleichbleibende Wirkspiegel erreicht. Dies ermöglicht eine bessere Verträglichkeit als mit Tabletten oder Lösungen. Die Zulassung der Pflasterform stützt sich auf die IDEAL-Studie (Investigation of transDermal Exelon in ALzheimer’s Disease) mit 195 Patienten. Die Resultate dieser Studie zeigten, dass die tägliche Anwendung eines Pflasters (9,5 mg/Tag) die kognitiven Fähigkeiten und die Alltagskompetenz genauso stark verbesserte wie die höchste zugelassene Kapseldosis (2×6 mg/Tag).[6] Ansonsten häufig beobachtete Nebenwirkungen wie Übelkeit und Erbrechen traten bei der Pflaster-Anwendung dreimal seltener auf als nach Einnahme der Kapseln. Die Häufigkeit der Nebenwirkungen war dabei nicht höher als unter einem Placebo-Präparat (Präparat ohne Wirkstoff). Es gibt aber auch Studien, die eine geringe Wirkung der Acetylcholinesterase-Hemmer zeigen.[7] Rivastigmin wird im Gegensatz zu den anderen Antidementiva Donepezil und Galantamin nicht Cytochrom-P450-abhängig verstoffwechselt, weshalb weniger Arzneimittelwechselwirkungen zu erwarten sind.
Handelsnamen
- Novartis: Exelon (D, A, CH), Prometax (I, E, P u. a.)
- Nimvastid (D, A), weitere Generika
Weblinks
- Alzheimer Demenz: Wie gut helfen Cholinesterasehemmer – Informationen bei Gesundheitsinformation.de (Online-Angebot des Instituts für Qualität und Wirtschaftlichkeit im Gesundheitswesen)
- Kassenärztliche Bundesvereinigung Wirkstoff AKTUELL zu Rivastigmin, Stand Januar 2010
Einzelnachweise
- The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage, 2006, S. 1422–1423, ISBN 978-0-911910-00-1.
- PHARMEUROPA 23.2 The European Pharmacopoeia Forum. 23.2, April 2011, S. 376–379.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Birks J: Cholinesterase inhibitors for Alzheimer's disease. In: Cochrane Database Syst Rev. Nr. 1, 2006, S. CD005593. doi:10.1002/14651858.CD005593. PMID 16437532.
- Lanctôt KL, Herrmann N, Yau KK, et al.: Efficacy and safety of cholinesterase inhibitors in Alzheimer's disease: a meta-analysis. In: CMAJ. 169, Nr. 6, September 2003, S. 557–564. PMID 12975222. PMC 191283 (freier Volltext).
- B. Winblad et al.: A six-month double-blind, randomized, placebo-controlled study of a transdermal patch in Alzheimer's disease – rivastigmine patch versus capsule. Int J Geriatr Psychiatry. 2007, 22(5), 456–467, PMID 17380489.
- Kaduszkiewicz H, Zimmermann T, Beck-Bornholdt HP, Hendrik van den Bussche: Cholinesterase inhibitors for patients with Alzheimer's disease: systematic review of randomised clinical trials. In: BMJ (Clinical Research Ed.). 331, Nr. 7512, August 2005, S. 321–327. PMID 16081444. PMC 1183129 (freier Volltext).