Lackmus
Lackmus ist ein aus Flechten meist der Gattung Roccella gewonnener blauvioletter Farbstoff. Die wässrige Lösung besitzt die Eigenschaft, ihre Farbe zu ändern; abhängig, ob sie mit sauren oder basischen Stoffen zusammengebracht wird (also je nach pH-Wert). Sie dient deshalb als Säure-Base-Indikator in der Chemie. Lackmus ist ein tiefblaues Stoffgemisch mit der CAS-Nummer 1393-92-6.

Name und Geschichte
Das Wort ist seit etwa 1500 bezeugt und stammt aus dem Mittelniederländischen: le(e)cmoes ([1]), von lekken „tröpfeln“, moes vermutlich von „Brei, Mus“ und nicht von der Pflanze (Moos).[2] Bereits im Niederländischen wird le(e)c an lak „Lack“ in der Bedeutung Farbe angeglichen.[3]
Der Name geht auf die historische Herstellung von Lackmus zurück, das aus einem Brei von Flechten und Wasser gewonnen wurde, den man abtropfen ließ.
Lackmus wurde erstmals um 1300 von dem Arzt und Alchemisten Arnaldus de Villanova als chemisches Reagenz verwendet, d. h. als ein Stoff, der zum Nachweis und zur Identifikation eines anderen Stoffes benutzt wird.[4] Seit dem 16. Jahrhundert gewann man den blauen Farbstoff in größerem Maßstab (vorwiegend in den Niederlanden als Lakmoes) aus verschiedenen Flechtenarten. Nachdem das Geheimnis der Herstellung von Lackmus aus Flechten gelüftet war, wurden die grau gefärbten Flechten Lecanora tartarea und Roccella tinctoria unter den Namen Bergmoos und Klippmoos als Exportartikel aus den Niederlanden in andere Industriestaaten ausgeführt.
Natürliches Vorkommen

Lackmus kommt in der Natur wie der mit ihm verwandte Farbstoff Orcein in verschiedenen Flechtenarten vor. Für die Farbstoffgewinnung verwendet wurden früher meist Roccella tinctoria (wächst auf Felsen Makaronesiens (Kap Verde, Kanarische Inseln, Madeira, Azoren) und der Westküste Südamerikas), Roccella fuciformis (Herkunft meist Angola und Madagaskar), Roccella pygmaea (Algerien), Roccella phycopsis, Lecanora tartarea (Norwegen, Schweden), Variolaria dealbata (Pyrenäen und Auvergne), Ochrolechia parella (gesamte Atlantikküste Nordwesteuropas), Parmotrema tinctorum (ebenfalls Kanaren) und verschiedene Parmelia-Arten (weite Verbreitung auf vielen Laubbäumen). Hauptquellen sind heutzutage Roccella montagnei (Mosambik) und Dendrographa leucophoea (Kalifornien).
Herstellung
Es wurde lange Zeit versucht, die Details des Herstellungsprozesses aus wirtschaftlichen Gründen geheim zu halten, um damit ein Monopol zu schaffen. Die gepulverten Flechten werden für mehrere Wochen in einer mit Soda (Natriumcarbonat) oder Pottasche (Kaliumcarbonat) und Ammoniak alkalisch eingestellten Lösung bei gelegentlichem Umrühren stehen gelassen. Da früher Ammoniak nicht als Chemikalie zur Verfügung stand, erhielt man den notwendigen Ammoniakanteil durch Zugabe von Urin. Der im Urin enthaltene Harnstoff wird durch Enzyme als Katalysatoren in Ammoniak umgewandelt. Während die pulverisierten Flechten in der Lösung stehen, ändert sich allmählich ihre Farbe von Rot nach Blau. Die am Ende des Umsetzungsprozesses blaue Mixtur wird getrocknet und zu Pulver zermahlen. In dieser Stufe des Herstellungsprozesses enthält das Pulver teilweise Lackmus- und teilweise Orcein-Farbpigmente. Mit Alkohol wird der auf Orcein entfallende, karminrote Farbanteil herausgelöst, zurück bleibt das tiefblaue Lackmus. Gepresst und teilweise mit Gips und Kreide versetzt, kommt es als leicht krümelnde Pressmasse in den Handel. Aus Lackmus wird auch eine spezielle Farbkomponente – das Azolitmin – hergestellt und als Säure-Base-Indikator mit dem Lackmus ähnlichen Eigenschaften vertrieben.
Heutige technische Herstellung
Im Jahr 1758 patentierten die beiden britischen Chemiker G. Gordon und Cuthbert Gordon die industrielle Herstellung von Cudbear (englische Bezeichnung für Orcein) und Lackmus aus Flechten,[5] es dauerte jedoch bis zum Jahr 1940, ehe die britische Firma Johnsons of Hendon (später Johnsons Photopia Ltd) die Fertigung begann.
Bei der Herstellung werden Flechten zunächst gemahlen, mit Wasser unter Zugabe von Kalk, Pottasche und Ammoniumcarbonat-Lösung ((NH4)2CO3) verrührt und unter Luftzufuhr gären gelassen. Die Lösung verfärbt sich über braun und violett nach etwa drei Wochen zu einem tiefen Blau. Der Brei wird durch ein Sieb gerührt und mit Kreide und Gips versetzt zu kleinen Würfeln geformt. Nach Trocknung können diese direkt weiterverarbeitet werden; sie enthalten große Mengen Orcein und nur etwa 5 bis 8 % der Lackmus-Farbstoffe. Das Orcein kann aufgrund seiner guten Alkohollöslichkeit leicht mit Ethanol abgetrennt werden.[6]
Verwendung und Struktur
Früher und heute
Lackmus fand früher besonders in den Niederlanden zum sogenannten Bläuen von Wäsche und zum Färben von Genussmitteln (Weine, Backwerk, Likör, Käse, Schminke und Zuckerpapier) Verwendung. Durch leichte Blaufärbung wird das Vergilben an der Luft ausgeglichen. Für die Textilfärberei ist Lackmus wegen seiner Farbumschläge in Säuren und Laugen ungeeignet.
Lackmustest
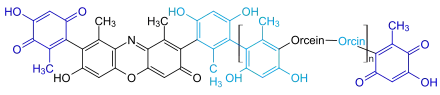
Heute wird Lackmus ausschließlich als Säure-Base-Indikator in der Chemie und Biologie genutzt. Bei pH-Werten kleiner als 4,5 erscheint Lackmus rot, bei Werten größer als 8,3 blau und dazwischen violett. Es wird hauptsächlich in zwei Formen verwendet: in einer wässrigen Lösung als Lackmus-Tinktur und als Lackmus-Papier. Bei letzterem handelt es sich um Papierstreifen, die mit schwach saurer oder alkalischer Lackmus-Tinktur getränkt sind (Reagenzpapier). Der Hauptbestandteil des Lackmus ist polymer (aus mehreren Bausteinen) aus 7-Hydroxy-2-phenoxazin-Chromophoren aufgebaut, was seine Verwandtschaft mit dem karminroten Farbstoff Orcein erklärt.
Lackmusmilch
Mit zwischen 2,5 und 7 % Lackmustinktur versetzte, 10%ige Magermilch oder Magermilchpulver und Wasser in entsprechender Konzentration dient in der Mikrobiologie als Lackmusmilch.[7] Diese wird zur Bestimmung, ob Bakterien Milchzucker (Lactose) verwerten können, verwendet. Dazu wird die Lackmusmilch mit dem Bakterium beimpft. Bei Farbumschlag durch Säurebildung von Blau (alkalisch) nach Rot (sauer) ist erwiesen, dass das Bakterium Lactose vergären kann. Zur besseren Handhabung wird die Milch oft mit Agar geliert.[8]
Strukturermittlung
Der deutsche Chemiker Hans Musso (1925–1988) untersuchte in den Jahren 1955 bis 1965 die Struktur der Flechtenfarbstoffe Orseille, Orcein (im Englischen auch Cudbear) und der Lackmus-Farbstoffe und veröffentlichte darüber etwa 25 Artikel.[9][10] Mit säulenchromatographischen Trennungsmethoden konnte er die meisten der Farbstoffe abtrennen und ihre Struktur ermitteln.[11][12][13]
Erklärung zur Indikatorwirkung von Lackmus
Die Ursache der Farbveränderung des Lackmus von Blau über Violett nach Rot bei Änderung des pH-Wertes ist äußerst komplex und setzt sich aus verschiedenen Faktoren zusammen[14]:
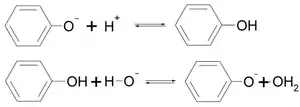
- Hauptursache der Farbveränderung bei Aufnahme oder Abgabe von Protonen (Halochromie) ist die reversible (also umkehrbare) Bildung von roten Phenolen aus blauen Phenolaten.
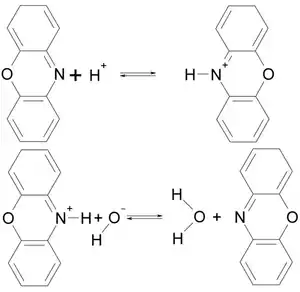
- Weiterhin kann das Oxazinsystem (hier eine cyclische Anordnung mit gegenüberstehendem Sauerstoff- und Stickstoffatom) protoniert bzw. deprotoniert werden, d. h., es können sich Protonen an die Verbindung anlagern oder wieder abspalten.
- Zusätzlich ändert sich auch noch die Tönung der für Lackmus charakteristischen Farben Rot und Blau, wenn man starke oder schwache Säuren bzw. Basen zum Lackmus gibt. Das resultiert aus der schrittweisen Anlagerung bzw. Entfernung weiterer Protonen.
Durch die Größe des Moleküls stehen mehrere Phenolgruppen sowie Oxazin-Stickstoffatome für diese Anlagerung oder Abgabe von Protonen zur Verfügung. Zusätzlich entstehen daher im pH-Bereich 5,6 bis 8 Mischsysteme mit gelb-oranger bis blaugrüner Farbe.
Enthaltene Stoffe
Das Stoffgemisch Lackmus enthält ca. 10-15 verschiedene Substanzen. Erfolgreich extrahiert wurden neben Orcein Erythrolein (auch Erythrolitmin), Azolitmin, Spaniolitmin, Leucoorcein und Leucazolitmin. Azolitmin als Reinsubstanz besitzt annähernd dieselbe Indikatorwirkung wie das Gemisch.[15]
Orceine
Im Lackmusgemisch sind hauptsächlich die beiden Orceine α-Hydroxyorcein C18H17O5N und α-Aminoorcein C18H18O4N2 enthalten.[16] Diese entstehen (neben mehr als 10 anderen Orceinen) aus den Farbstoffen der Flechten durch Behandlung in Ammoniak-haltiger, alkalischer Lösung unter Oxidation. Bei der Lackmusherstellung wird der Großteil des Orceins abgetrennt.
Azolitmin und Leucazolitmin
Azolitmin ist der hauptsächlich für den Farbumschlag verantwortliche Farbstoff mit der Summenformel C18H10O10N. Es entsteht aus Orceinen durch Oxidation. Leucazolitmin ist ein farbloses Derivat des Azolitmins und aus diesem durch Reduktion erhältlich.
Sicherheitshinweise
In englischsprachigen Quellen wird Lackmus als reizend für (Schleim-)Haut und Augen klassifiziert[17] sowie als „wahrscheinlich bei höheren Temperaturen brennbar“. EU- oder deutsche Richtlinien liegen nicht vor.
Siehe auch
Literatur
- Eintrag zu Lackmus. In: Römpp Online. Georg Thieme Verlag, abgerufen am 13. Juni 2014.
Einzelnachweise
- Lackmus bei duden.de, abgerufen am 26. April 2015.
- Kluge/Seebold: Etymologisches Wörterbuch der Deutschen Sprache. De Gruyter: Berlin Boston, 2011, ISBN 978-3-11-022364-4, Artikel: Lackmus.
- Wolfgang Pfeiffer: Etymologisches Wörterbuch des Deutschen. Rhenanina/Lahnstein, Edition Kramer, 2018, ISBN 978-3-941960-03-9, Artikel: Lackmus.
- Wissenschaft-Online-Lexika: Eintrag zu Lackmus im Lexikon der Arzneipflanzen und Drogen, abgerufen am 18. Februar 2013.
- Gordon G. and Gordon C: Manufacture of Dye Colours, British patent 727, 1758
- H.H.J. Hager, F.v. Bruchhausen Hagers Handbuch der pharmazeutischen Praxis, S. 3, Springer-Verlag, ISBN 3-540-62646-8
- Mikrobiologisches Praktikum für Biologie und Lebensmittelchemie, Script SS 2011, TU München
- Wissenschaft-Online-Lexika: Eintrag zu Lackmusmilch im Lexikon der Biologie
- H. Musso: Zur Kenntuis der Orseille-Farbstoffe, Naturwissenschaften, 1955, 42, 513
- H. Musso, C. Rajtjen: Über Orceinfarbstoffe: X. Lichtabsorption und Chromophor des Lackmus, Chemische Berichte, 1959, 92, 751-753
- H. Musso: Die Trennung des Orceins in seine Komponenten (II. Mitteilung über Orceinfarbstoffe), Chemische Berichte, 1956, 89, 1659-1673
- H. Musso: Orcein and litmus pigments: constitutional elucidation and constitutional proof by synthesis, In: Planta Medica, 1960, 8, 431-446
- H. Musso, H. Beecken: Über Orceinfarbstoffe. IV. Craig-Verteilung und Verteilungschromatographie, Chemische Berichte, 1957, 90, 1808-1814
- Was ist eigentlich Lackmus?, Wiechoczek, D. 1999-2009. In: Blume, R. & Wiechoczek, D. "Professor Blumes Bildungsserver für Chemie".
- E.T. Wolf: Vollständige Übersicht der Elementar-analytischen Untersuchungen organischer Substanzen, S. 450–453, veröffentlicht 1846, Verlag E. Anton
- Lichen purple: Orcein structures
- Litmus, Powder auf Sciencelab (Memento des Originals vom 27. September 2007 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. (engl.; abgerufen 29. März 2007)