Edward Calvin Kendall
Edward Calvin Kendall (geboren am 8. März 1886 in South Norwalk, Connecticut; gestorben am 4. Mai 1972 in Princeton, New Jersey) war ein amerikanischer Biochemiker. Kendall gelang die Isolation des Schilddrüsenhormons Thyroxin und die Strukturaufklärung des Glutathion. In den 1940er Jahren isolierte er zudem das Nebennierenhormon Cortison und wurde dafür 1950 gemeinsam mit Tadeus Reichstein und Philip Showalter Hench mit dem Nobelpreis für Physiologie oder Medizin ausgezeichnet.

Leben
Edward Calvin Kendall wurde 1886 in South Norwalk im Bundesstaat Connecticut als drittes Kind von George S. und Eva F. Kendall geboren. Sein Vater war Zahnarzt und aktiv in der kommunalen Politik, das Elternhaus und die Erziehung waren christlich geprägt. Kendall ging auf die Franklin Elementary School und danach für zwei Jahre auf die South Norwalk High School sowie für ein Jahr auf die Stamford High School, wo er sich für das Studium vorbereitete.[1]
Er studierte an der Columbia University in der Stadt New York als einer der ersten Studenten bei Henry Clapp Sherman[2] und erhielt dort 1908 seinen Bachelor of Science sowie 1909 seinen Master of Science im Bereich Chemie. Nach seinem Masterabschluss wurde er der erste Goldschmidt Fellow an der Universität bis 1910, bevor er im Fachbereich Chemie für seine Arbeiten über das Enzym Amylase promoviert wurde. Nach der Promotion ging er am 1. September 1910 für fünf Monate als Forscher zu Parke, Davis and Co., heute ein Tochterunternehmen von Pfizer, in Detroit, Michigan, und arbeitete an der Biochemie der Schilddrüse. Diese Arbeiten führte er von 1911 bis 1914 am St. Luke's Hospital in New York City weiter,[3] wo er anfangs ohne Gehalt das medizinische Labor einrichten durfte.[1] 1915 heiratete er Rebecca Kennedy (1892–1973), mit der Kendall vier Kinder hatte: Hugh, Roy, Norman und Elizabeth.[1][4]
Auf die Empfehlung von Clarence M. Jackson wurde Kendall 1914 Mitarbeiter von William und Charles Horace Mayo an der Mayo Clinic, die ein besonderes Interesse an Schilddrüsenerkrankungen hatten.[1] Hier wurde er später Leiter der Abteilung Biochemie der Graduate School of the Mayo Foundation in Rochester, die mit der University of Minnesota assoziiert war. 1915 wurde er Direktor des Fachbereichs Biochemie der University of Minnesota und Professor für physiologische Chemie.[3] Bis in die späten 1920er Jahre beschäftigte sich Kendall mit der Erforschung des Thyroxin und seiner Wirkung, lag bei der Strukturaufklärung allerdings falsch. Danach beschäftigte er sich mit verschiedenen Aminosäuren, vor allem dem Glutathion. Anfang der 1930er Jahre begann er mit der Erforschung der Nebenniere und den in diesem Organ produzierten Hormonen. Dabei isolierte er u. a. das Cortison, dessen therapeutische Wirkung bei der Behandlung von Rheuma-Erkrankungen er gemeinsam mit Philip S. Hench aufklären konnte. Im Jahr 1950 erhielt er gemeinsam mit diesem und dem Schweizer Tadeus Reichstein, der etwa zeitgleich und unabhängig von Kendall ebenfalls Cortison isolieren konnte, den Nobelpreis für Physiologie oder Medizin.[3]
Kendall blieb an der Universität und wurde am 1. April 1951 emeritiert sowie Visiting Professor des Fachbereichs Biochemie der Princeton University.[3] Ebenfalls 1951 wurde er in die American Academy of Arts and Sciences und die American Philosophical Society[5] gewählt, ein Jahr zuvor war er in die National Academy of Sciences gewählt worden. Im Jahr 1971 veröffentlichte Kendall seine Autobiografie Cortisone: Memoirs of a Hormone Hunter. Er starb am 4. Mai 1972 in Princeton, New Jersey.
Werk
Frühe Arbeiten
Die ersten Forschungsarbeiten publizierte Kendall gemeinsam mit seinem Professor Henry Clapp Sherman im Journal of the American Chemical Society, die sich mit der Identifizierung Reduzierender Zucker mit Hilfe von p-Brombenzohydrazid beschäftigten.[6] Für seine Doktorarbeit mit dem Titel A Quantitative Study of the Action of Pancreatic Amylases[7] arbeitete er an der Pankreas-Amylase, einem in der Bauchspeicheldrüse produzierten Enzym, das für die Verdauung von Kohlenhydraten notwendig ist. Dabei konnte er vor allem die Abhängigkeit der Amylase-Aktivität beim Abbau von Zuckern von der Kochsalz-Konzentration nachweisen.[1][8][9] Sherman arbeitete zu dieser Zeit sehr intensiv an pflanzlichen und tierischen Enzymen und bezog seine Studenten und Doktoranden in dieser Forschungen ein. Allein für seine Serie Studies on amylases veröffentlichte er von 1910 bis 1915 insgesamt zehn Paper mit verschiedenen Studenten.[2]
Schilddrüsenhormone
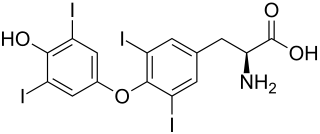
Nach seiner Promotion widmete sich Kendall als Forscher bei Parke, Davis and Co. der Schilddrüse und ihrer Funktion sowie speziell der Aufgabe, das bis dahin nur wenig bekannte Schilddrüsenhormon zu isolieren. Dabei baute er auf Arbeiten des deutschen Chemikers Eugen Baumann, der bis zu seinem Tod 1896 organisch gebundenes Jod der Schilddrüse untersuchte und isolieren konnte. Dieses wurde zur Behandlung von Hypothyreose, der angeborenen oder erworbenen Schilddrüsenunterfunktion, angewendet. Bis 1913 konnte Kendall verglichen mit Baumann etwa die 100-fache Menge der aktiven Substanz gewinnen und ihre Wirkung an Hunden wie auch an Patienten mit einer Hypothyreose nachweisen. Bei seiner späteren Beschäftigung in der Mayo Clinic hatte Kendall erneut die Aufgabe, das Hormon aus operativ entferntem Schilddrüsengewebe zu isolieren. Mit Hilfe von Ethanol als Lösungsmittel gelang es ihm bis Ende 1914 nach der Hydrolyse des Gewebes Jod-Konzentrationen von 47 % zu erreichen. Als Kendall bei einem Versuch am 23. Dezember 1914 einschlief und das gesamte Ethanol der Probe verdampfte, konnte er eine weiße, ethanolunlösliche Inkrustierung feststellen, die 60 % Jod enthielt. Er stellte über Weihnachten größere Mengen des Stoffes her und löste es in Ethanol mit ein wenig Natriumhydroxid und konnte nach Zugabe von ein paar Tropfen Essigsäure eine Kristallbildung beobachten. Die Analysen ergaben, dass es sich bei den Kristallen um eine reine Aminosäure handelte.[10]
Kendall nahm an, dass es sich um ein Oxindol handelt, das er als 'Thyroxin' bezeichnete; in der englischen Sprachform in 'Thyroxine' geändert.[11] Nachdem er in den Folgejahren genug Reinkristalle isolieren konnte, wendete er sie bei klinischen Experimenten an und konnte zeigen, dass dieses Thyroxin bei der Behandlung der Hypothyreose die volle Wirkung des den Patienten fehlenden Schilddrüsenhormons hatte.[1] Kendall konzentrierte sich in den Folgejahren auf die chemischen und physiologischen Eigenschaften sowie auf die Isolierung größerer Mengen des Thyroxins und konnte etwa 33 Gramm des Schilddrüsenhormons aus etwa drei Tonnen Schilddrüsengewebe von Schweinen gewinnen.[11][12] Durch die Vorarbeiten von Kendall konnte der Chemiker Charles Robert Harington 1927 ein synthetisches Thyroxin durch die Kondensation zweier Moleküle Diiodotyrosin herstellen, das die gleichen Eigenschaften wie Thyroxin hatte und so zur korrekten Auflösung der chemischen Struktur des Thyroxin führte.[11]
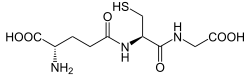
Die Forschung Kendalls konzentrierte sich später auf die Wirkungen und Oxidationsprozesse im menschlichen Körper, die durch das Thyroxin ausgelöst werden. Hierbei fokussierte er seine Arbeit auf das Cystein sowie das Glutathion. Letzteres war zu diesem Zeitpunkt nicht verfügbar und die Mayo Clinic bekam den Auftrag, es zu kristallisieren und für die Synthese bereitzustellen. Glutathion wurde erstmals von Frederick Gowland Hopkins 1921 isoliert und benannt. Kendall arbeitete mit Bernhard F. McKenzie und Harold L. Mason an der Aufgabe und konnte es ebenfalls isolieren sowie außerdem kristallisieren und die Identität als Tripeptid aus den Aminosäuren Glutaminsäure, Cystein und Glycin feststellen.[1]
Cortison
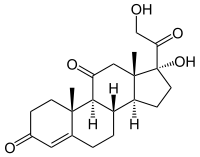
Zu Beginn der 1930er Jahre begann Kendall sich mit der hormonellen Funktion der Nebenniere zu beschäftigen. Zu diesem Zeitpunkt war bekannt, dass die Nebennierenhormone zentrale und lebensnotwendige Funktionen hatten, da Patienten und Versuchstiere nach der Entnahme der Organe starben. Über die genaue physiologischen Zusammenhänge lagen jedoch noch keine Kenntnisse vor. Kendall isolierte 28 Substanzen,[13] von denen sechs physiologische Wirkung zeigten und von ihm als Substanzen A, B, C, D, E und F bezeichnet wurden. Er konzentrierte sich danach vor allem auf die Substanz E, die er Cortison nannte, und konnte nachweisen, dass Versuchstiere ohne Nebenniere nach Einspritzen der Substanz überlebten.[14] Die gleiche Substanz wurde etwa zeitgleich auch von Tadeus Reichstein in Zürich sowie von einer Arbeitsgruppe um Oskar Wintersteiner entdeckt.[15]
Gemeinsam mit seinen Mitarbeitern konnte Kendall die Isolierung aus Gallensäure optimieren[15] und so bis April 1948 400 Gramm des Cortisons herstellen. Er versendete dieses an insgesamt 28 Kliniken zur klinischen und therapeutischen Erprobung, bekam jedoch keine Bestätigung für eine potenzielle Heilwirkung von Cortison. Im September 1948 injizierte der ebenfalls an der Mayo-Klinik aktive Arzt und Professor Philip Showalter Hench das von Kendall erhaltene Cortison einer Frau, die an einer rheumatischen Gelenkentzündung litt, und wiederholte dies in den folgenden Tagen. Nach nur einer Woche war die Patientin schmerzfrei und konnte erste Gehversuche machen, der Erfolg ließ sich auch bei anderen Patienten zeigen.[14] Cortison eröffnete so neue Therapiemöglichkeiten für die Rheumaforschung und -behandlung, auch wenn es keine über die Einnahmedauer hinausgehende Wirkung hat und aufgrund starker Nebenwirkungen nur begrenzt genutzt werden konnte.[16]
1951 fand Robert B. Woodward erstmals einen Weg für die Totalsynthese von Cortison, das damit nicht mehr aus Gewebe isoliert werden musste und entsprechend in größeren Mengen hergestellt und genutzt werden konnte. Ab 1953 stand Cortison in den Vereinigten Staaten bereits in großen Mengen zur Verfügung und wurde zu einem der wichtigsten Arzneimittel.[15] Bis zum Ende der 1960er Jahre wurde es jedoch durch Cortisol bzw. Hydrocortison ersetzt, das die eigentlich wirksame Form des Cortison darstellt.[15] Später eingeführte Präparate wie Prednisolon-Derivate,[15] die neben der höheren Wirksamkeit auch geringere Nebenwirkungen aufweisen, verdrängten Cortison weiter. Insbesondere bei Hormonmangel und allergischen Reaktionen ist Cortison jedoch weiterhin gebräuchlich.[14]
Auszeichnungen
1949 wurde Kendall mit dem Albert Lasker Award for Clinical Medical Research ausgezeichnet. Ein Jahr später erhielt er gemeinsam mit Tadeus Reichstein und Philip S. Hench zu jeweils gleichen Teilen den Nobelpreis für Physiologie oder Medizin für ihre Entdeckungen bei den Hormonen der Nebennierenrinde, ihrer Struktur und ihrer biologischen Wirkungen.[17] 1952 erhielt er die George M. Kober Medal.
Literatur
- Dwight Ingle: Edward C. Kendall 1886–1972. in der Serie Biographical Memoir der National Academy of Sciences. 1975.
- Wouter W. de Herder: Heroes in endocrinology: Nobel Prizes. In: Endocrine Connections. 3 (3), 2014, S. R94–R104. doi:10.1530/EC-14-0070
- Edward Calvin Kendall: Cortisone: Memoirs of a Hormone Hunter. Autobiografie. Macmillan, 1971, ISBN 0-684-31062-7.
- Kendall, Edward Calvin. In: Bernhard Kupfer: Lexikon der Nobelpreisträger. Patmos-Verlag, Düsseldorf 2001, ISBN 3-491-72451-1, S. 237–238.
- Edward C. Kendall, In: Internationales Biographisches Archiv., im Munzinger-Archiv (Artikelanfang frei abrufbar) 30/1972 vom 17. Juli 1972.
Weblinks
- Informationen der Nobelstiftung zur Preisverleihung 1950 an Edward Calvin Kendall (englisch)
- Edward C. Kendall in der Hall of Fame der The Minnesota High Tech Association (MHTA) und dem Science Museum of Minnesota; abgerufen am 2. Februar 2015.
Einzelnachweise
- Dwight Ingle: Edward C. Kendall 1886–1972 in der Serie Biographical Memoir der National Academy of Sciences, 1975.
- Charles Glenn King: Henry Clapp Sherman 1875–1955 in der Serie Biographical Memoir der National Academy of Sciences, 1975.
- Edward C. Kendall - Biographical von Edward Calvin Kendall auf den Seiten der Nobelstiftung zur Preisverleihung 1950 (englisch). Abgerufen auf nobelprize.org am 2. Februar 2015; erschienen in: Nobel Lectures, Physiology or Medicine 1942–1962. Elsevier Publishing Company, Amsterdam 1964.
- Wouter W. de Herder: Heroes in endocrinology: Nobel Prizes. In: Endocrine Connections. 3 (3), 2014, S. R94–R104. doi:10.1530/EC-14-0070
- Member History: Edward C. Kendall. American Philosophical Society, abgerufen am 21. Oktober 2018.
- Edward Calvin Kendall, Henry Clapp Sherman: The detection and identification of certain reducing sugars by condensation with para-brombenzylhydrazide. In: Journal of the American Chemical Society. 30 (9), 1908, S. 1451–1455, doi:10.1021/ja01951a019.
- Edward Calvin Kendall: A Quantitative Study of the Action of Pancreatic Amylases. Wynkoop Hallenbeck Crawford C., New York 1910.
- Edward Calvin Kendall, Henry Clapp Sherman, E. D. Clark: Studies on Amylases. I. An Examination of methods of diastatic power. In: Journal of the American Chemical Society. 32 (9), 1910, S. 1073–1086, doi:10.1021/ja01927a010.
- Edward Calvin Kendall, Henry Clapp Sherman, E. D. Clark: Studies on Amylases. II. A study of the action of pancreatic amylase. In: Journal of the American Chemical Society. 32 (9), 1910, S. 1087–1105, doi:10.1021/ja01927a011.
- Edward Calvin Kendall: The isolation in crystalline form of the compound containing iodine which occurs in the thyroid: Its chemical structure and physiological activity. In: Transactions of the Association of American Physicians. 30, 1915, S. 420–429.
- Asfandyar Khan Niazi, Sanjay Kalra, Awais Irfan, Aliya Islam: Thyroidology over the ages. In: Indian Journal of Endocrinology and Metabolism. 15 (Supplement 2), 2011; S. S121–S126. doi:10.4103/2230-8210.83347
- Edward Calvin Kendall: Isolation of the Iodine Compound Which Occurs in the Thyroid. In: The Journal of Biological Chemistry. 39, 1919, S. 125, (Volltext).
- Edward Calvin Kendall: The Development of Cortisone As a Therapeutic Agent. Nobel Lecture, 11. Dezember 1950, (Volltext).
- Kendall, Edward Calvin In: Bernhard Kupfer: Lexikon der Nobelpreisträger. Patmos-Verlag, Düsseldorf 2001, ISBN 3-491-72451-1, S. 237–238.
- Peter Dilg: Cortison. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner: Enzyklopädie Medizingeschichte. Band 1, De Gruyter, Berlin u. a. 2004, 2011, ISBN 978-3-11-097694-6, S. 275 (abgerufen über De Gruyter Online).
- Renate Wagner: Kendall, Edward Calvin. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner: Enzyklopädie Medizingeschichte. Band 2, De Gruyter, Berlin u. a. 2004, 2011, ISBN 978-3-11-097694-6, S. 731–732 (abgerufen über De Gruyter Online).
- Informationen der Nobelstiftung zur Preisverleihung 1950 an Edward Calvin Kendall (englisch)