ETBE
ETBE (nach IUPAC-Nomenklatur: 2-Ethoxy-2-methylpropan, ausgeschrieben auch Ethyl-tert-butylether) ist eine organisch-chemische Verbindung aus der Stoffgruppe der aliphatischen Ether. Er hat zum einen wegen seiner Verwendung als Antiklopfmittel in Ottokraftstoffen sowie zum anderen als Lösungsmittel in der organischen Chemie eine gewisse großtechnische Bedeutung erlangt.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
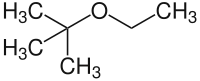 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Ethyl-tert-butylether | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C6H14O | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 102,18 g·mol−1[1] | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
0,74 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
73 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
| |||||||||||||||
| Brechungsindex |
1,375 (20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten |
> 2000 mg/kg (LD50, Kaninchen, transdermal)[1] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
| ETBE | |
|---|---|
| Kurzbeschreibung | Klopfschutzmittel für Ottokraftstoffe |
| Eigenschaften | |
| Aggregatzustand | flüssig |
| Oktanzahl | |
| Flammpunkt |
−19 °C[1] |
| Explosionsgrenze | 1,2–7,7 Vol.-%[1] |
| Sicherheitshinweise | |
| UN-Nummer |
1179 |
| Gefahrnummer |
33 |
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |
Gewinnung und Darstellung
Industrielle Synthese
Ethyl-tert-butylether wird großtechnisch durch säurekatalysierte Veretherung von Isobuten mit Ethanol bei Temperaturen von 30–110 °C und Drücken von 8–13 bar an sauren Ionentauscherharzen hergestellt.[5]

Als Reaktoren eignen sich hierfür vor allem Festbettreaktoren wie Rohrbündel- oder Kreislaufreaktoren, bei denen der Rückstrom optional gekühlt werden kann.[5]
Laborsynthese
Im Labor lässt sich Ethyl-tert-butylether auch durch die säurekatalysierte Veretherung von tert-Butanol mit Ethanol bei 40 °C herstellen. Als Katalysator wird 15%ige wässrige Schwefelsäure verwendet.[6]

Der gewünschte Ethyl-tert-butylether wird dabei mit 95 % Ausbeute erhalten. Dies ist auf die thermodynamische Stabilität des intermediär gebildeten tertiären Carbeniumions zurückzuführen. Aus diesem Grund wird die konkurrierende Kondensationsreaktion zweier Ethanolmoleküle zum Diethylether sehr gering gehalten.[6]
Eigenschaften
Physikalische Eigenschaften
Ethyl-tert-butylether hat eine relative Gasdichte von 3,53 (Dichteverhältnis zu trockener Luft bei gleicher Temperatur) und eine Dichte von 0,74 g·cm−3 bei 20 °C. Außerdem weist ETBE einen Dampfdruck von 173 hPa bei 25 °C auf.[1]
Chemische Eigenschaften
Ethyl-tert-butylether ist eine leicht entzündbare Flüssigkeit aus der Stoffgruppe der Ether. Er ist leichter als Wasser und wenig löslich darin (12 g·l−1 bei 25 °C). Dafür weist er eine sehr gute Löslichkeit in Ethanol und Diethylether auf.[2] Mit Luft kann der leicht flüchtige Ethyl-tert-butylether leicht Peroxide bilden. Daher können explosive Dampf-Luft-Gemische entstehen.[1]
Konstitutionsisomere zu Ethyl-tert-butylether sind n-Butylethylether und sec-Butylethylether.
Verwendung
ETBE wird analog zu Methyl-tert-butylether (MTBE) bzw. tert-Amylethylether (TAEE) zur Verbesserung der Klopffestigkeit dem Ottokraftstoff zugesetzt (maximal 15 Vol.-%). MTBE wird aus fossilen Rohstoffen erzeugt. ETBE dagegen kann z. B. aus fossilem Isobuten und Ethanol aus nachwachsenden Rohstoffen (Bioethanol) erzeugt werden.
In der EU hat gemäß der Erneuerbare-Energien-Richtlinie (EG) bis 2020 der Einsatz von 10 % erneuerbaren Energien im Verkehrssektor zu erfolgen. Ein Großteil dieses Ziels soll durch den Einsatz von Biokraftstoffen erreicht werden. In Deutschland wurde durch das Biokraftstoffquotengesetz (BioKraftQuG) bis 2015 ein Mindestanteil von Biokraftstoffen von 8 % (energetisch) am gesamten Kraftstoffmarkt vorgeschrieben. Dieser wurde durch das Gesetz zur Änderung der Förderung von Biokraftstoffen wieder reduziert, so dass bis zum Jahr 2014 eine Biokraftstoffquote von 6,25 % gilt. Durch den stöchiometrisch berechneten Bioethanol-Anteil in „Bio-ETBE“ kann dieser zu 47 % als Biokraftstoffbeimischung gewertet werden. ETBE ist teurer als Bioethanol. Die Beimischung zu Motorenbenzin erfolgt daher nur, wenn aus technischen Gründen (z. B. fehlende Beimischungstechnik) kein Bioethanol verwendet werden kann oder wenn höherwertige Benzinvarianten produziert werden sollen. Die Oktanzahl von ETBE (117) ist höher als die von Ethanol (104).
Im Rahmen des MTBE-Verbots (siehe MTBE) ist auch die Beimischung von ETBE in Motorenbenzin in etlichen US-Bundesstaaten verboten.[7]
Weblinks
Einzelnachweise
- Eintrag zu Ethyl-tert-butylether in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. März 2017. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 88. Auflage. (Internet-Version: 2008), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-80..
- Datenblatt tert-Butyl ethyl ether bei Sigma-Aldrich, abgerufen am 20. Mai 2015 (PDF).
- François GARIN: FORMULATIONS OF FUELS (Memento vom 15. Oktober 2005 im Internet Archive) (PPT).
- Matthias Grömping, Frank Höper, Jörg Leistner, Franz Nierlich, Udo Peters, Jochen Praefke, Armin Rix, Dirk Röttger, Silvia Santiago Fernandez: Verfahren zur Herstellung von Ethyl-tert.-Butylether aus technischen Mischungen von C4-Kohlenwasserstoffen. In: Google Patents. EVONIK DEGUSSA GMBH, 12. Juli 2007, abgerufen am 21. Februar 2019.
- K. Peter C. Vollhardt, Neil E. Schore: Organische Chemie. Hrsg.: Holger Butenschön. 5. Auflage. WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim / Germany 2011, ISBN 978-3-527-32754-6, S. 390.
- Environmental Protection Agency, USA: Gasoline Composition Regulations Affecting LUST Sites (PDF; 1,1 MB).

