Stereozentrum
Als Stereozentrum (auch Chiralitätszentrum oder stereogenes Zentrum/Atom) bezeichnet man in der Stereochemie einen Punkt in einem Molekül mit einem Satz an Substituenten in einer solchen räumlichen Anordnung, dass sie mit der spiegelbildlichen Anordnung nicht in Deckung gebracht werden kann.[1][2]
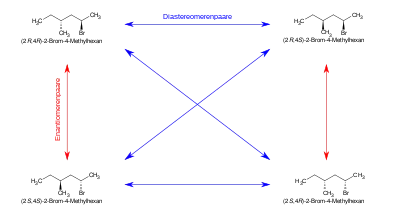 Zwei diastereomere Enantiomerenpaare am Beispiel des 2-Brom-4-methylhexans.[3] Zusätzliche Stereozentren würden zusätzliche Enantiomerenpaare erzeugen.
Zwei diastereomere Enantiomerenpaare am Beispiel des 2-Brom-4-methylhexans.[3] Zusätzliche Stereozentren würden zusätzliche Enantiomerenpaare erzeugen.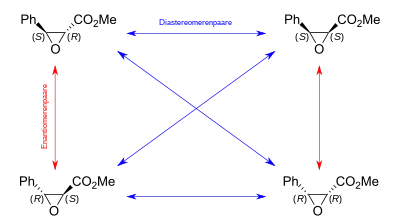 Enantiomere und Diastereomere am Beispiel von Epoxiden: Enantiomere sind Spiegelbilder zueinander, Diastereomere nicht.
Enantiomere und Diastereomere am Beispiel von Epoxiden: Enantiomere sind Spiegelbilder zueinander, Diastereomere nicht.
| Stereozentren |
 Zweidimensionale Präsentation von 3-Methylhexan mit einem Stereozentrum an einem Kohlenstoffatom (mit einem blau markierten Sternchen (✱) gekennzeichnet). |
 Zweidimensionale Präsentation von 2-Brom-4-methylhexan mit zwei Stereozentren an Kohlenstoffatomen (jeweils mit blau markierten Sternchen (✱) gekennzeichnet). |
Das Stereozentrum muss nicht unbedingt mit einem Atom zusammenfallen, sondern kann auch zwischen mehreren Atomen liegen (s. u.: Doppelbindung).
Formen
Eine gängige Form des Stereozentrums ist das asymmetrisch substituierte Kohlenstoffatom, das vier unterschiedliche Substituenten trägt, z. B. ein Wasserstoffatom (H), einen Methylrest (CH3), einen Ethylrest (CH2CH3) und einen Propylrest (CH2CH2CH3). In diesem Zusammenhang wird auch häufig die formal nicht ganz korrekte Bezeichnung des asymmetrischen Kohlenstoffatoms verwendet. Der Begriff ist jedoch historisch geprägt und geht auf Jacobus Henricus van ’t Hoff zurück.[4]
Der Begriff Substituent ist dabei weit zu fassen und beinhaltet auch freie Elektronenpaare. Daher können nicht nur vierbindige, tetraedrisch koordinierte Kohlenstoffatome oder quartäre Ammoniumverbindungen vom Amin-Typ Chiralitätszentren sein, sondern auch pyramidal koordinierte Atome wie z. B. Stickstoffatome in sterisch gehinderten Aminen, Phosphoratome in Phosphanen oder Schwefelatome in Sulfoxiden.
Auch eine Doppelbindung kann ein Stereozentrum darstellen, sie wird dann als stereogene Doppelbindung bezeichnet.[5] Nach der Cahn-Ingold-Prelog-Konvention werden die beiden resultierenden Stereoisomere gekennzeichnet mit (E) (von Entgegen) oder mit (Z) (von Zusammen).[6]
Zur Kennzeichnung eines Stereozentrums in Strukturformeln wird für gewöhnlich ein Stern verwendet. Diese Kennzeichnung wird jedoch seitens der IUPAC nicht empfohlen, sofern die Bedeutung des Sterns nicht eindeutig aus dem gegebenen Kontext hervorgeht.[7] Die Nomenklatur der Konfiguration eines Stereozentrums erfolgt mit Hilfe der Cahn-Ingold-Prelog-Konvention.
Während ein einzelnes Stereozentrum immer ein chirales Molekül bedingt, führt das Vorhandensein mehrerer Stereozentren nicht zwangsläufig zu einer chiralen Struktur. Existieren nämlich mehrere zueinander spiegelbildliche Stereozentren innerhalb des Moleküls, so liegt eine achirale meso-Verbindung vor.
Umgekehrt gibt es auch chirale Verbindungen ohne Chiralitätszentrum, die dann eine axiale, helicale oder planare Chiralität aufweisen.
Von Verbindungen mit Stereozentren existieren Stereoisomere. Sind Stereoisomere spiegelbildlich zueinander, so spricht man von Enantiomeren, andernfalls von Diastereomeren.
Stereozentren können in chemischen Reaktionen entweder gezielt (Stereospezifität) oder bevorzugt (Stereoselektivität) gebildet werden. Reaktionen, bei denen die möglichen Konfigurationen eines Stereozentrums gleich häufig gebildet werden, bezeichnet man als stereounspezifisch.
Anzahl
Die Zahl der maximal möglichen Stereoisomere eines Moleküls lässt sich aus der Zahl seiner Stereozentren berechnen:
- Ein Molekül mit n Stereozentren besitzt 2n Stereoisomere. Die 2n Stereoisomere bilden 2n-1 Enantiomer-Paare, die zueinander diasteromer sind.
Die rechts gezeigte Struktur von 2-Brom-4-methylhexan (n = 2 Stereozentren) besitzt also 22 = 4 verschiedene Stereoisomere. Diese bilden 22-1 = 2 Enantiomer-Paare, die zueinander diastereomer sind.[6]
Die tatsächliche Zahl der Stereozentren kann niedriger sein, beispielsweise durch meso-Verbindungen oder durch Verknüpfungen der Stereozentren untereinander, wie bei Heterocyclen möglich.
Einzelnachweise
- Eintrag zu chirality centre. In: IUPAC (Hrsg.): Compendium of Chemical Terminology. The “Gold Book”. doi:10.1351/goldbook.C01060 – Version: 2.1.5.
- Karl-Heinz Hellwich: Stereochemie: Grundbegriffe. Springer-Verlag, Heidelberg, Berlin 2002, ISBN 3-540-42347-8, S. 21.
- Gerhard Hilt, Peter Rinze: Chemisches Praktikum für Mediziner. Springer, 2012, ISBN 978-3-8348-0667-3 (Seite 153 in der Google-Buchsuche).
- Peter J. Ramberg: Chemical Structure, Spatial Arrangement: The Early History of Stereochemistry, 1874-1914. Ashgate Publishing, Aldershot 2003, ISBN 0-7546-0397-0, S. 57 (eingeschränkte Vorschau in der Google-Buchsuche).
- Ursula Bünzli-Trepp: Systematic Nomenclature of Organic, Organometallic and Coordination Chemistry: Chemical Abstracts Guidelines and Iupac Recommendations and Many Trivial Names. EPFL Press, 2007, ISBN 978-1-4200-4615-1 (Seite 560 in der Google-Buchsuche).
- Paula Yurkanis Bruice: Organische Chemie: Studieren kompakt. Pearson Deutschland GmbH, 2011, ISBN 978-3-86894-103-6 (Seite 131 in der Google-Buchsuche).
- Jonathan Brecher: Graphical representation standards for chemical structure diagrams (IUPAC Recommendations 2008). In: Pure Appl. Chem. Band 80, Nr. 2, 2008, S. 277–410, doi:10.1351/pac200880020277.