Herpes Zoster
Herpes Zoster, auch kurz Zoster,[1][2] deutsch Gürtelrose, umgangssprachlich auch Kopfrose[3] oder Gesichtsrose genannt,[4] ist eine Viruserkrankung, die hauptsächlich durch einen schmerzhaften streifenförmigen Hautausschlag mit Blasen bzw. Hautbläschen auf einer Körperseite in Erscheinung tritt. Der Bläschenausschlag entsteht durch das Übergreifen einer Entzündung von einem Nerv (z. B. eines Ganglions) auf das umliegende Dermatom (Hautgebiet).
| Klassifikation nach ICD-10 | |
|---|---|
| B02 | Herpes Zoster |
| ICD-10 online (WHO-Version 2019) | |
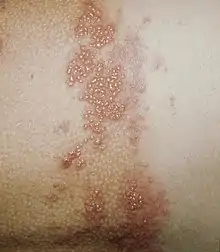
Die Krankheit wird durch das zur Familie der Herpesviridae gehörende Varizella-Zoster-Virus (VZV) ausgelöst. Sie tritt meist bei älteren Menschen oder solchen mit geschwächtem Immunsystem (durch Stress, infolge anderer Erkrankungen wie beispielsweise bei AIDS oder durch eine spezielle immunsuppressive Therapie) auf. Das Virus wird häufig bereits in der Kindheit übertragen und verursacht bei der Primärinfektion die Windpocken.[5] Ein Herpes Zoster ist immer eine endogene, d. h. von innen erzeugte Reaktivierung einer alten VZV-Infektion (Erregerpersistenz).
In Deutschland sind zwei Impfstoffe zugelassen, um einer Erkrankung vorzubeugen. Hierbei empfiehlt die STIKO die Impfung mit einem Totimpfstoff generell für Personen ab 60 Jahren und außerdem bei Personen mit einer erhöhten gesundheitlichen Gefährdung ab 18 Jahren.[6]
Etymologie
Die volkstümliche deutsche Bezeichnung Gürtelrose entstand, weil sich der rötliche Ausschlag bei besonders ausgeprägten Erscheinungsformen von der Wirbelsäule ausgehend halbseitig oder ganz gürtelförmig um den Körper schlingt und dort eine Wundrose hervorruft.[7] Dabei ist Wundrose ein altertümlicher Ausdruck für eine akute, lokal begrenzte Hautentzündung, der oft undifferenziert für verschiedene Krankheitsbilder unterschiedlicher Ursachen verwendet wurde.
Die Bezeichnung Herpes Zoster (früher Herpes zoster) leitet sich ab von altgriechisch ζωστήρ zōstḗr (‚Gürtel‘ in Bezug auf den „gürtelartigen“ Verlauf erstmals bei Plinius dem Älteren[8]). Vergleiche auch altgriechisch ἕρπειν herpein, deutsch ‚kriechen‘.
Auf Englisch wird der Herpes Zoster shingles genannt, was wiederum dem lateinischen cingulum für ‚Gürtel‘ entlehnt ist, auf Französisch zona und zoster.
Alte Bezeichnungen sind unter anderem Fieberflechte[9] sowie „Feuergürtel“ (lateinisch Zona ignea), in Frankreich und England auch Zone bzw. Zona, und der ansonsten für den Ergotismus („Antoniusfeuer“) verwendete Ausdruck Ignis sacer („Heiliges Feuer“).[10] Den Herpes zoster nannte man früher auch Gürtelausschlag und Gürtelflechte[11] sowie Zona serpiginosa.[12]
Häufig werden die verkürzten Fachausdrücke Zoster (für Herpes Zoster, ausgelöst durch das Varizella-Zoster-Virus (VZV)) und Herpes (für Herpes simplex, eine durch Herpes-simplex-Viren hervorgerufene Erkrankung) verwechselt, obwohl es sich um zwei verschiedene Erkrankungen handelt, die sich im Erreger und insbesondere in den Folgeerkrankungen deutlich unterscheiden.
Pathophysiologisch wurde der Herpes zoster auch als Poliomyelitis acuta posterior der Poliomyelitis acuta anterior (Kinderlähmung) gegenübergestellt.[13]
Epidemiologie
In Deutschland erkranken jährlich etwa 350.000 bis 400.000 Menschen an einem Herpes Zoster[14], rund 2/3 davon sind über 50 Jahre, wie eine Studie aus den 2010er Jahren gezeigt hat. Daraus resultiert eine Inzidenz von 9,6 pro 1000 Personen pro Jahr.[15]
Da bis zum vollendeten 40. Lebensjahr rund 98 % der Bevölkerung mit dem Varizella-Zoster-Virus meist entweder klinisch manifest in Form der Windpocken oder in Form einer stillen Feiung Kontakt hatten, sind nahezu alle erwachsenen Menschen gefährdet. Dies beruht auf der Tatsache, dass die Varicella-Zoster-Viren lebenslang inaktiv im Körper verweilen. Rund 25 bis 30 % der Bevölkerung erleiden im Laufe ihres Lebens einen Zoster. Bei den 85-Jährigen hat bereits die Hälfte eine Erkrankung durchlebt. Die Veränderungen, die die Einführung der seit 2004 empfohlenen Impfung im ersten Lebensjahr mit sich bringt, sind bisher nicht bekannt.
Die Wahrscheinlichkeit einer Herpes-Zoster-Infektion steigt mit zunehmendem Alter, Frauen sind häufiger betroffen. Weitere Risikofaktoren sind Erkrankungen, die mit einer Schwächung des Immunsystems einhergehen.[16] Einfluss haben:
- Erkrankungen des Immunsystems erhöhen das Risiko erheblich, so Lymphome (Odds-Ratio OR=3,9), Myelome (OR=2,2), HIV-Infektion (OR=5,1), Stammzelltransplantation (OR = 13,5).
- Immunsuppressive Medikamente: orale Corticoide (OR = 1,5), Januskinase-Inhibitoren (relatives Risiko 2,0–3,2), andere Immunsuppressiva (OR=1,8)
- Erkrankungen mit indirekter Schwächung des Immunsystems: Rheumatoide Arthritis (OR=1,5), entzündliche Darmerkrankungen (OR=1,4), Chronische obstruktive Lungenerkrankung (COPD, OR = 1,3), Asthma, chronische Niereninsuffizienz, Diabetes Typ I
- weitere Risikofaktoren sind eine familiäre Vorbelastung (OR=1,7), vorausgegangene Herpes-Zoster-Erkrankung (OR=1,8), aber auch Schlafstörungen (OR=2,5), Depressionen (OR=3,8) und Stress (OR=2,8).
Erreger
Als Erreger dieser Erkrankung ist das Varizella-Zoster-Virus (VZV) – auch als Humanes Herpes-Virus-3 (HHV-3) bezeichnet – nachgewiesen. Dieses Virus ist ein behülltes, doppelsträngiges DNA-Virus (dsDNA) und gehört zur Familie der Herpesviridae, zur Unterfamilie Alphaherpesvirinae und zur Gattung Varicellovirus. Alle Viren dieser Familie sind mit einem ikosaedrischen Kapsid ausgestattet, das von einer Virushülle umgeben ist. Dazwischen findet sich als Besonderheit das Tegument aus verschiedenen funktionellen Proteinen. Das Varizella-Zoster-Virus ist mit den Herpes-simplex-Viren relativ nahe verwandt, dennoch gibt es keine Kreuzprotektion. Schätzungen zufolge sind rund 90 Prozent der über 14-jährigen Europäer durch Windpocken-Infektionen Träger von Varizella-Zoster-Viren.
Übertragung
Die Erstinfektion eines gesunden Menschen äußert sich üblicherweise in der weitverbreiteten Kinderkrankheit Windpocken. Die hochansteckenden Erregerviren werden per Tröpfcheninfektion, also direktes Einatmen von Ausatmungströpfchen (Exspirationströpfchen) infizierter Personen, oder über Kontaktinfektion beziehungsweise Schmierinfektion mit den Viren der auf Gegenständen oder Körperoberflächen niedergegangenen infektiösen Exspirationströpfchen übertragen, wenn sie anschließend sofort über die Schleimhäute beispielsweise in Mund, Nase oder Augen in den Körper gelangen.[17] Da die Erreger an der Luft nur für etwa zehn Minuten infektiös sind, ist eine Übertragung durch herumliegende Kleidung oder Spielzeug in der Regel nicht zu befürchten. Weiterhin ist durch den virushaltigen Bläscheninhalt des Hautausschlags eine Schmierinfektion möglich. Auch der Speichel und die Tränenflüssigkeit (Konjunktivalflüssigkeit) infizierter Personen sind infektiös. Sehr selten ist die Möglichkeit einer diaplazentaren Übertragung des Varizella-Zoster-Virus durch die Schwangere auf den Fetus. Dabei kann es in etwa ein bis zwei Prozent der Varizellenerkrankungen bei Schwangeren zum fetalen Varizellensyndrom führen.[18]
Auch wenn die Betroffenen normalerweise nach einer Windpocken-Erkrankung ein Leben lang immun gegen die Krankheit sind, verbleibt das Virus nach Abklingen der Symptome im Körper und kann später, beispielsweise ausgelöst durch Stress oder ein altersbedingtes nachlassendes Immunsystem, in seltenen Fällen auch durch Sonneneinwirkung (UV-Licht), reaktiviert werden. Die Viren verbleiben latent in den Nervenwurzeln des Rückenmarks, den Spinalganglien sowie in den Ganglien der Hirnnerven. Der Herpes Zoster kann nicht direkt übertragen werden; es erfolgt immer nur eine Reaktivierung einer bereits stattgefundenen Infektion („Kein Zoster ohne vorherige Windpocken“) oder einer Impfung mit Lebendimpfstoff gegen Varizellen. Herpes Zoster ist demnach keine Infektion im eigentlichen Sinne, sondern die erneute Aktivierung des Varizella-Zoster-Virus nach einer mehr oder weniger langen Latenzzeit. Für Menschen, die in der Kindheit an Windpocken erkrankt waren und über ein voll aktives Immunsystem verfügen (d. h. immunkompetent und nicht immunsupprimiert sind), besteht in der Regel keine Gefahr, sich an einem Herpes-Zoster-Erkrankten anzustecken. Eine Übertragung der Viren erfolgt bei Herpes Zoster nur durch den virushaltigen Bläscheninhalt (Schmierinfektion), nicht aber über die Atemwege als Tröpfcheninfektion. Nur bis zur Verkrustung der Bläschen bleibt der Erkrankte über den Bläscheninhalt ansteckungsfähig. Es können durch Herpes Zoster – ohne eine frühere Windpocken-Erkrankung oder Windpocken-Lebendimpfung – im Infektionsfall dann die Windpocken ausgelöst werden.
Krankheitsverlauf/Symptome

Verlauf
In der Latenzphase der Erkrankung kommt es zu einer Reaktivierung der Varizella-Zoster-Viren, die nach Erstinfektion in den Spinalganglien verbleiben. Diese Phase ist durch eine Entzündung des Nervengewebes ausgezeichnet. Es kommt typischerweise zu starken Schmerzen und weiteren Symptomen wie Brennen in dem Hautbereich, der durch den Nervenstrang versorgt wird. Schmerzen, die vor oder begleitend mit dem dermatomalen Ausschlag auftreten, nennt man zosterassoziierte Schmerzen. Im Gegensatz dazu wird der Schmerz, der nach der Hautsymptomatik auftritt und oftmals von Dauer ist, postzosterische oder postherpetische Neuralgie (PHN) genannt.
In 80 % der Fälle geht der Manifestation des Zoster an der Haut ein Frühstadium (Prodromalstadium) voraus. Dies dauert etwa drei bis fünf Tage. Die Symptome in dieser Phase können sehr variabel sein. In den meisten Fällen wird über Allgemeinsymptome wie leichtes Fieber, Müdigkeit und Abgeschlagenheit (auch B-Symptomatik genannt) berichtet. Seltenere Beschwerden wie Brennen, Parästhesien und Schmerzen mit unterschiedlichem Charakter sind je nach befallenem Dermatom oftmals Anlass für Fehldiagnosen wie Bandscheibenvorfall, Nierenkolik, Herzinfarkt, Blinddarmentzündung, Cholezystitis und Gallenkolik.
Das Nervengewebe entzündet sich bei einer Reaktivierung des latenten Virus. Symptome sind Brennen und teils starke Schmerzen in dem Hautbereich, der durch den betroffenen Nervenstrang versorgt wird, und im Nervenstrang selbst. Auch werden im Frühstadium Allgemeinsymptome wie Abgeschlagenheit und Müdigkeit berichtet. Die Schmerzen treten häufig vor der Bildung der Hauterscheinungen auf, die in der Regel zwei bis drei Tage später folgen. Im befallenen Nervensegment entwickeln sich schubweise einseitig auftretende, schmerzhafte kleine erhabene Stellen mit Rötung der Haut (1). In den folgenden zwölf bis 24 Stunden bilden sich in diesem Erythem oft gruppiert stehende bis zu reiskorngroße prall gespannte Bläschen (2), die eine wasserklare Flüssigkeit enthalten. In der Regel ist dieses Stadium nach zwei bis drei Tagen abgeschlossen. Zu einer Verschmelzung (Konfluenz) dieser Bläschen kommt es nach weiteren zwei bis vier Tagen. Bereits am dritten Tag können die Bläschen eintrüben. Die Bläschen füllen sich anschließend mit Lymphe und brechen auf (3) und können im Normalfall über ca. sieben bis zwölf Tage abtrocknen. Binnen zwei bis sieben Tagen trocknen sie dann aus, dabei bildet sich eine gelb-braune Borke aus (4). Diese Phase kann ein bis vier Wochen dauern, in der Regel heilt der Zoster jedoch binnen zwei bis drei Wochen ab. Abwehrgeschwächte Personen leiden gelegentlich an chronischen Verläufen mit monatelang bestehenden Hautveränderungen und mehrmaligen Bläscheneruptionen.[19][20][21] Häufig bilden sich Narben, insbesondere nach einer Zweitinfektion z. B. durch Bakterien.[22] In sehr seltenen Fällen kann der Ausschlag aber auch ganz ausbleiben.
Als Folge der Gürtelrose können noch lange neurologisch bedingte Schmerzen auftreten.[7] Das Auftreten solch einer (postherpetischen) Neuralgie ist bisher nicht ausreichend geklärt, vermutet werden Schädigungen der Nerven.[23]
Lokalisation
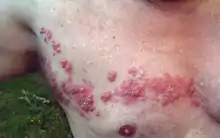
Die Lokalisation der Gürtelrose wird durch das Versorgungsgebiet der befallenen Nerven bestimmt. Überdurchschnittlich häufig (in 50–56 % der Fälle) handelt es sich um einen Befall der Interkostalnerven (im Bereich des Brustkorbes).[24][25][26] Seltener können auch Rücken, Arme oder Beine betroffen sein. Bei tiefgehenden Entzündungen der Haut spricht man vom Zoster gangraenosus.
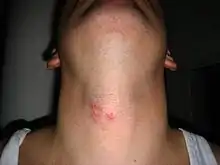
Bei Zoster ophthalmicus sind Gesicht und Augen betroffen (Nervus ophthalmicus aus dem Nervus trigeminus). Sind die Augen betroffen, kann durch Hornhautvernarbung teilweise oder vollständige Erblindung die Folge sein. Bei Befall der Gesichtsnerven (Nervus facialis) kann es zu vorübergehenden Lähmungserscheinungen oder Verlust des Geschmackssinns kommen.
Zoster oticus bezeichnet einen Befall des Gehörgangs und/oder der Ohrmuschel. Mögliche Folgen sind hier neben den Zoster-typischen starken Schmerzen, Schwerhörigkeit (Nervus cochlearis) und Störungen des Gleichgewichtssinnes (Nervus vestibularis). Auch kann im Rahmen eines Zoster oticus eine Neuralgie zusammen mit einer Fazialisparese auftreten (Ramsay-Hunt-Syndrom/Ramsay-Hunt-Neuralgie).[27] Unbehandelt können dauerhafte Hörbeeinträchtigungen oder Taubheit die Folge sein.
Zoster generalisatus bezeichnet einen Befall des gesamten Nervensystems; diese Krankheitsform ist lebensbedrohlich, tritt aber üblicherweise nur bei starker primärer Schwächung des Immunsystems auf (z. B. bei AIDS, Leukämie oder anderen Krebs-Formen).
Zoster genitalis tritt im Genitalbereich auf. Er zieht über das ganze Geschlechtsteil wie Penis, Schamlippen, Klitoris großflächig bis auf die Oberschenkel. Im Lymphabflussgebiet des betroffenen Hautareals lassen sich nicht selten aktivierte Lymphknoten nachweisen.
Zum Zoster disseminatus kommt es bei Streuung der Viren im Blut. Dies ist allerdings nur bei ein bis zwei Prozent der Patienten mit gesundem Immunsystem der Fall. Bei abwehrgeschwächten Patienten wird es häufiger beobachtet.[28][29]
In der Regel ist nur ein Dermatom vom charakteristischen Zosterexanthem betroffen (Zoster segmentalis). Es sind jedoch auch Überlappungen im Befall der Dermatome beschrieben. Zoster duplex, bei dem es zu einer Überschreitung der Mittellinie des Körpers kommt, ist eher selten. In sehr seltenen Fällen werden mehrere Hautsegmente asymmetrisch befallen, insbesondere wenn es zu einer Zweitinfektion z. B. durch Bakterien kommt.[30]
Komplikationen
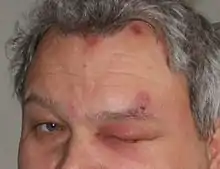
Herpes-Zoster-Komplikationen sind mit über 20 % der Fälle relativ häufig. Insbesondere die postherpetische Neuralgie (PHN), auch als Post-Zoster-Neuralgie (PZN) bezeichnet, ist dabei überaus häufig und führt zu schweren, oft als brennend beschriebenen Schmerzen. Die PZN/PHN kann im schlimmsten Fall sogar lebenslang fortbestehen und ist für die Betroffenen zum Teil unerträglich. Auch die selteneren Zoster-Formen wie Zoster generalisatus, Zoster ophthalmicus (10–15 %, davon mit Augenbeteiligung 30–40 %) und Zoster oticus werden gelegentlich zu den Komplikationen gezählt. Nicht selten heilen auch die Bläschen nur unter Pigmentierungsstörungen und Narbenbildung ab (im Gegensatz zu den Windpocken, sofern diese nicht durch Kratzen zu Vernarbungen geführt haben). Andere Komplikationen sind seltener und betreffen meist nur stark immungeschwächte Menschen. Zu den Komplikationen gehören Zoster-Meningitis (Hirnhautentzündung), Zoster-Enzephalitis (Hirngewebsentzündung) und Zoster-Myelitis (Rückenmarksentzündung).
Ebenso kommt es häufig zu Lähmungen peripherer Nerven, insbesondere des Gesichtsnervs. Die Lähmungserscheinungen bilden sich in der Regel jedoch zurück.[22]
Eine Herpes-Zoster-Infektion ist Indikator für ein leicht erhöhtes Risiko für kardiovaskuläre Erkrankungen wie Schlaganfall und Herzinfarkt.[31] Dies sollte bei der individuellen Planung von Vorsorgeuntersuchungen berücksichtigt werden.
Diagnose und Differenzialdiagnose
Der Herpes Zoster ist vorwiegend eine Diagnose auf der Basis der klinischen Symptome. Spezielle virologische Nachweisverfahren sind nur bei komplizierten Verläufen (Beteiligung des Zentralnervensystems, generalisierter Zoster) oder bei unsicheren klinischen Zeichen notwendig. Führend ist in allen Fällen der direkte Virusnachweis mittels PCR, entweder aus betroffenem Gewebe oder Gewebsflüssigkeit oder aus punktiertem Bläscheninhalt. Da es sich um eine Reaktivierung handelt, sind serologische Methoden zum Nachweis spezifischer Antikörper nur sehr eingeschränkt aussagefähig. Bei Reaktivierungen des VZV kann das Anti-VZV-IgA bei gleichzeitig negativem Anti-VZV-IgM für mehrere Monate nachweisbar sein.
Differentialdiagnostisch ist beim Auftreten von typischen Bläschen auf der Haut auch an eine atypische Lokalisation einer Herpes-simplex-Infektion zu denken. Diese den Zoster nachahmende Form des Herpes simplex bezeichnet man auch als „Zosteriformer Herpes simplex“. Umgekehrt kann ein unregelmäßig lokalisierter Zoster als „Herpetiformer Zoster“ auch eine Herpes-simplex-Infektion nachahmen. Als weitere mögliche Ursache für ständig wieder auftretende Hautbläschen kommt auch ein Morbus Hailey-Hailey in Betracht.
Therapie
Das Varizella-Zoster-Virus kann mit Virostatika behandelt werden. Je früher eine Behandlung einsetzt, desto höher sind die Chancen, mögliche Komplikationen zu reduzieren.
Wichtig ist die frühzeitige medikamentöse Behandlung mit Virostatika bei sehr ausgedehntem Befund, beispielsweise Beteiligung des Auges oder Ohres und insbesondere bei vorbestehender Abwehrschwäche (z. B. Tumorerkrankung, schwerem Diabetes mellitus oder HIV). Üblicherweise erfolgt die Behandlung mit Aciclovir, Brivudin, Famciclovir oder Valaciclovir, meistens in Tablettenform. Medizinische Studien legen nahe, dass der Wirkstoff Brivudin wie auch Valaciclovir und Famciclovir etwas besser als Aciclovir wirkt.[32][33][34] Im Gegensatz zu Aciclovir, Valaciclovir und Famciclovir muss Brivudin nur einmal täglich verabreicht werden.[35] Allerdings sollte Brivudin nicht länger als sieben Tage angewendet werden, da eine Verlängerung der Behandlung über den empfohlenen Zeitraum von sieben Tagen hinaus mit einem erhöhten Risiko für die Entstehung einer Leberentzündung (Hepatitis) verbunden ist.[36] Famciclovir sollte nicht bei Kindern und Jugendlichen angewendet werden.[37]
In komplizierteren Fällen (Beteiligung des Auges, des Ohres, des Rückenmarks) ist eine intravenöse Behandlung mit Aciclovir erforderlich. In der Regel ist die zusätzliche Gabe von starken Schmerzmitteln angezeigt. Bei einigen der betroffenen Patienten können die akuten Schmerzen nicht durch Schmerzmittel beeinflusst werden. Manchmal kommen Lidocainpflaster oder andere Anwendungen mit Lokalanästhetika zum Einsatz.[38]
Vorbeugung/Impfung
Risiken für ungeimpfte Schwangere
An Windpocken oder an Gürtelrose Erkrankte müssen unbedingt den Kontakt mit Schwangeren vermeiden, die nicht entsprechend vorgeimpft bzw. keine oder nicht genügend Antikörper gegen das Virus im Körper entwickelt haben. Eine Windpockeninfektion während der Schwangerschaft kann beim Kind zu Entwicklungsstörungen führen; erleidet die Mutter in den letzten Tagen vor der Geburt einen Windpockenausbruch, besteht für das Kind sogar Lebensgefahr.
Impfungen für Kinder gegen Windpocken (Varizellen)
In Deutschland werden mit Varilrix und Varivax zwei ab dem ersten Lebensjahr zugelassene Varizellenimpfstoffe als Monoimpfstoffe von der Ständigen Impfkommission als Standardimpfstoffe empfohlen.[39] Darüber hinaus ist die Varizelle-Komponente Bestandteil des Mehrfachimpfstoffs MMRV ProQuad und Priorix-Tetra.
Impfungen für Personen ab 50 Jahren
In Deutschland sind zwei Impfstoffe gegen Herpes Zoster für Personen ab 50 Jahren zugelassen und verfügbar: der Lebendimpfstoff Zostavax sowie der Untereinheitenimpfstoff Shingrix, der u. a. ein kombinantes Oberflächenglykoprotein des Varizella-zoster-Virus und einen Wirkverstärker (AS01B) enthält:[6]
- Der Lebendimpfstoff Zostavax wird von der Ständigen Impfkommission (STIKO) derzeit (Stand: 2020) wegen seiner eingeschränkten Wirksamkeit und -dauer nicht als Standardimpfung empfohlen.[6] Zostavax wurde am 25. Mai 2006 in den USA durch die zuständige Behörde FDA zugelassen. Mit einer derartigen Impfung können 51 % der Gürtelrosen-Krankheitsfälle verhindert und auch eine PZN (Post-Zoster-Neuralgie) um 66,5 % vermieden werden. Wenn trotz Impfung dennoch eine Gürtelrose auftritt, verläuft diese in der Regel deutlich milder und mit weniger Komplikationen.[40] Für diesen Lebendimpfstoff ist nur eine Impfdosis erforderlich. Falls Personen aufgrund einer Immunschwäche oder einer immunsuppressiven Therapie ein erhöhtes Risiko haben, an Herpes zoster zu erkranken, ist die Impfung mit Zostavax kontraindiziert.[6]
- Seit Dezember 2018 empfiehlt die Ständige Impfkommission (STIKO) den Totimpfstoff Shingrix für Personen ab 60 Jahren generell als Standardimpfung sowie für Personen ab 50 Jahren bei einer erhöhten gesundheitlichen Gefährdung bzw. bei angeborener oder erworbener Immundefizienz. Dabei ist es meist nicht nötig zu wissen, ob die Person die Windpocken hatte oder nicht.[6] Shingrix wurde Anfang 2018 zugelassen (seit November 2020 auch für Personen über 18 Jahren mit einem erhöhten Risiko für Herpes zoster)[41] und konnte in Studien eine Wirksamkeit von über 90 % für alle Personen ab 50 Jahren belegen. Außerdem kann mit diesem Impfstoff die folgenschwere Komplikation Post-Zoster-Neuralgie (PZN) verhindert werden. Dieser Totimpfstoff wird in zwei Impfdosen im Abstand von zwei bis sechs Monaten verabreicht.[14] Anders als der Lebendimpfstoff zeigt der Totimpfstoff auch im höheren Alter eine gute Wirkung und kann auch nach autologer Stammzelltransplantation gegeben werden. Die Empfehlung, bei schweren Grunderkrankungen ab einem Alter von 50 Jahren zu impfen, folgt aus dem Design der Zulassungsstudien, aber es „gibt keine Evidenz, dass nicht auch jüngere Risikopatienten von der Schutzimpfung profitieren könnten.“[16]
Nebenwirkungen der Impfung
Die beobachteten Nebenwirkungen des Totimpfstoffes sind 1,79 mal häufiger als beim Lebendimpfstoff.[42][43] Da der Impfstoff sehr reaktogen ist, hat man bei 10 % der Geimpften leichte Lokalreaktionen wie Hautrötungen, Schwellungen oder Schmerzen im Bereich der Einstichstelle sowie systemische Reaktionen (Fieber, Müdigkeit, Myalgie und Kopfschmerzen) beobachtet.[6] Nach 1 bis 2 Tagen klingen die Nebenwirkungen wieder ab.
Als schwerere Nebenwirkungen werden vom Hersteller GSK genannt:[14]
- PZN, ein starker stechender und oft sehr lange anhaltender Schmerz,
- Narbenbildung,
- Sehstörungen,
- Lähmungserscheinungen in verschiedenen Körperregionen, vor allem im Gesicht.
Das Paul-Ehrlich-Institut (PEI) hat im April 2020 eine Beobachtungsstudie initiiert, da im engen zeitlichen Zusammenhang mit der Shingrix-Impfung Verdachtsfallmeldungen eines Herpes zosters sowie ausgeprägte, teilweise bläschenförmige Hautreaktionen vorliegen.[44] Ziel ist es herauszufinden, ob der Impfstoff das Varizella-Zoster-Virus reaktivieren kann, was damit eine Nebenwirkung wäre. Da es sich bei Shingrix aber nicht um einen Lebendimpfstoff, sondern um einen Untereinheitenimpfstoff handelt, fehlt momentan eine plausible Erklärung für einen entsprechenden Pathomechanismus; daher kann es sich gemäß Arzneimittelkommission der deutschen Ärzteschaft auch um eine „zufällige zeitliche Assoziation“ handeln.[45] Die Studie wurde am 14. Oktober 2020 beendet.[44]
Meldepflicht
Nach dem sächsischen Recht besteht eine namentliche Meldepflicht bezüglich Erkrankung und Tod an Herpes Zoster.[46]
Literatur
- S2k-Leitlinie Diagnostik und Therapie des Zoster und der Postzosterneuralgie der Dermatologische Gesellschaft. In: AWMF online (Stand 2019)
Weblinks
- Leitlinienvorhaben: Zoster und Zosterschmerzen der Deutschen Dermatologischen Gesellschaft und der Paul-Ehrlich-Gesellschaft für Chemotherapie.'' In: AWMF online (geplant für 12/2018).
- Varizellen (Windpocken), Herpes zoster (Gürtelrose), Zoster – Informationen des Robert Koch-Instituts
- Bilder des Herpes zoster Auf: dermis.net; zuletzt abgerufen am 3. März 2022.
- Peter Wutzler, Wolfgang Meister: Herpes zoster – Symptomatologie, demographische Daten und prognostische Faktoren: Ergebnisse einer prospektiven Studie an ambulanten Zosterpatienten in Deutschland. In: Deutsches Aerzteblatt. 1997, Band 94, Nr. 1, A-1129 / B-963 / C-903. Auf: aerzteblatt.de; zuletzt abgerufen am 3. März 2022.
- Marianne Beutler, Thomas Kappeler: Frühe Therapie verhindert Komplikationen. In: Pharmazeutische Zeitung. 12. Mai 2006.
- Herpes zoster im Gesichtsbereich. In: Zahnärztliche Mitteilungen. vom 1. Dezember 2013, Auf: zm-online.de.
Einzelnachweise
- Pschyrembel Klinisches Wörterbuch. 266., aktualisierte Auflage. De Gruyter, Berlin 2014, ISBN 978-3-11-033997-0, S. 2326.
- Helmut Ruska: Über das Virus der Varicellen und des Zoster. In: Klinische Wochenschrift. Band 22, 1943, S. 703–705.
- Anna Nilsson: Gürtelrose am Kopf. Auf: guertelrose-infektion.de vom 9. September 2013; abgerufen am 24. März 2016.
- Max Höfler: Deutsches Krankheitsnamen-Buch. Piloty & Loehle, München 1899 (reprografischer Nachdruck: Olms, Hildesheim/ New York 1970 und 1979, ISBN 1-174-35859-9), S. 519.
- Was ist Gürtelrose? Abgerufen am 20. Juli 2018.
- Varizellen – Gürtelrose (Herpes zoster): Antworten auf häufig gestellte Fragen zu Erkrankung und Impfung. In: RKI. 24. Januar 2019, abgerufen am 13. Februar 2020.
- Gürtelrose. gesundheit.de; abgerufen am 15. September 2013.
- G. Plinius Secundus: Naturalis historia. Band XXVI, Kapitel 74, § 121.
- A. Müller, R. W. Schlecht, Alexander Früh, H. Still: Der Weg zur Gesundheit: Ein getreuer und unentbehrlicher Ratgeber für Gesunde und Kranke. Band 2, 1929, S. 230: Die Fieberflechte (Gürtelrose, Bläschenflechte).
- Albrecht Scholz: Herpes zoster. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin/ New York 2005, ISBN 3-11-015714-4, S. 579.
- Friedrich Copei, Ad Quest: Der biochemische Ratgeber. 5. Auflage. Weichert, Lage in Lippe 1922, S. 92.
- Günter Thiele (Hrsg.): Handlexikon der Medizin. Band 4: S–Z. Urban & Schwarzenberg, München/ Wien/ Baltimore ohne Jahr, S. 2739.
- Fr. Hiller: Organische Nervenkrankheiten. In: Lehrbuch der inneren Medizin. Band 2. 4. Auflage. Springer-Verlag, Berlin 1939, S. 590.
- Flyer des Pharma-Herstellers GSK im Zusammenhang mit der Schutzimpfung; Stand vom Sommer 2021.
- B. Ultsch et al.: Herpes zoster in Germany: Quantifying the burden of disease. In: BioMed Central (BMC): Infectious Diseases. 2011, Nr. 11, S. 173, doi:10.1186/1471-2334-11-173.
- Florian Prechter, Matthias Pletz, Ulf Müller-Ladner, Andreas Stallmach: Therapie mit Wermutstropfen: Reaktivierung von Herpes zoster Deutsches Ärzteblatt 2019, Jahrgang 116, Heft 35–36 vom 2. September 2019, Seiten A-1541–A-1542.
- Dietmar Busch: Varizella-Zoster-Virus: Windpocken und Herpes Zoster – Eine szientometrische Analyse. Dissertation, Institut für Arbeitsmedizin der Medizinischen Fakultät Charité – Universitätsmedizin Berlin, Berlin 2011, S. 3: 1.3.1 Primärinfektion. Volltext (PDF).
- Windpocken, Herpes zoster (Gürtelrose). Abschnitt: Infektionsweg. RKI-Ratgeber für Ärzte, Stand: 30. März 2016; abgerufen am 11. Januar 2017.
- J. J. Rusthoven, P. Ahlgren, T. Elhakim et al.: Varizella zoster infection in adult cancer patients: a population study. In: Archives of internal medicine. Band 148, Nr. 7, Juli 1988, S. 1561–1566, PMID 3382302.
- W. B. Hoppenjans, M. R. Bibler, R. L. Orne et al.: Prolonged cutaneous herpes zoster in acquired immunodeficiency syndrome. In: Archives of Dermatology. Band 126, Nr. 8, August 1990, S. 1048–1050, PMID 2166483.
- R. G. Kost, S. E. Straus: Postherpetic neuralgia – pathogenesis, treatment and prevention. In: The New England Journal of Medicine. Band 335, Nr. 4, Juli 1996, S. 23–42, PMID 8637540.
- Ingrid Moll (Hrsg.): Dermatologie. 6., komplett überarbeitete und erweiterte Auflage. Thieme, Stuttgart/ New York 2005, ISBN 978-3-13-126686-6, S. 215 f.
- Lea Schnurbus, M. Foerster: Herpes Zoster. Auf: www.guertelrose-infektion.de, aktualisiert am 26. Mai 2013, abgerufen am 15. September 2013.
- R. Edgar Hope-Simpson: The Nature of Herpes Zoster: A Long-term Study and a New Hypothesis. In: Proceedings of the Royal Society of Medicine. Januar 1965, Band 58, Nr. 1, S. 9–20, PMC 1898279 (freier Volltext), PMID 14267505.
- M. W. Ragozzino, L. J. Melton et al.: Risk of cancer after herpes zoster: a population-based study. In: The New England Journal of Medicine. 12. August 1982, Band 307, Nr. 7, S. 393–397, PMID 6979711, doi:10.1056/NEJM198208123070701.
- W. Meister, A. Neiss, G. Gross et al.: Demography, symptomatology, and course of disease in ambulatory zoster patients: a physician-based survey in Germany. In: Intervirology. 1998, Band 41, Nr. 6, S. 272–277.
- C. Sweeney, D. Gilden: Ramsay Hunt syndrome. In: Journal of Neurology, Neurosurgery, and Psychiatry. August 2001, Band 71, Nummer 2, S. 149–154, doi:10.1136/jnnp.71.2.149.
- J. L. Meier, S. E. Straus: Comparative biology of latent varicella-zoster virus and herpes simplex virus infections. In: The Journal of infectious diseases. Nr. 166, Supplement 1, August 1992, S. 13–23, PMID 1320646.
- P. R. Cohen, V. P. Beltrani, M. E. Grossman: Disseminated herpes zoster in patients with human immunodeficiency virus infection. In: The American journal of medicine. Band 84, Nr. 6, Juni 1988, S. 1076–1080, PMID 3376978.
- G. Bloss, M. A. Ebisch u. a.: Bilateral asymmetric herpes zoster in adolescence. In: Der Hautarzt; Zeitschrift für Dermatologie, Venerologie, und verwandte Gebiete. Band 52, Nr. 4, April 2001, S. 335–338, ISSN 0017-8470, PMID 11382126.
- Judith Breuer, Maud Pacou, Aline Gauthier, Martin M. Brown: Herpes zoster as a risk factor for stroke and TIA: A retrospective cohort study in the UK. In: Neurology. Online-Veröffentlichung vor Druck am 2. Januar 2014, doi:10.1212/WNL.0000000000000038.
- S. W. Wassilew, P. Wutzler u. a.: Oral brivudin in comparison with acyclovir for improved therapy of herpes zoster in immunocompetent patients: results of a randomized, double-blind, multicentered study. In: Antiviral research. Juni 2003, Band 59, Nr. 1, S. 49–56, PMID 12834860.
- S. W. Wassilew, P. Wutzler u. a.: Oral brivudin in comparison with acyclovir for herpes zoster: a survey study on postherpetic neuralgia. In: Antiviral research. Juni 2003, Band 59, Nr. 1, S. 57–60, PMID 12834861.
- S. Wassilew, Collaborative Brivudin PHN Study Group: Brivudin compared with famciclovir in the treatment of herpes zoster: effects in acute disease and chronic pain in immunocompetent patients. A randomized, double-blind, multinational study. In: Journal of the European Academy of Dermatology and Venereology. (JEADV) Januar 2005, Band 19, Nr. 1, S. 47–55, PMID 15649191, doi:10.1111/j.1468-3083.2004.01119.x.
- X. Rabasseda: Brivudine: a herpes virostatic with rapid antiviral activity and once-daily dosing. In: Drugs of today (Barcelona, Spain: 1998.) Mai 2003, Band 39, Nr. 5, S. 359–371, PMID 12861349.
- Zostex. Beipackzettel, abgerufen am 16. Juli 2017.
- Peter Wutzler et al.: Antivirale Therapie des Herpes Zoster. In: Konsensuskonferenz der Paul Ehrlich Gesellschaft, Erfurt, 8. Februar 2002.
- R. W. Johnson, A. S. Rice: Clinical practice. Postherpetic neuralgia. In: The New England Journal of Medicine. 16. Oktober 2014, Band 371, Nr. 16, S. 1526–1533, doi:10.1056/NEJMcp1403062.
- Varizellen-Impfstoffe (Windpocken). In: Paul-Ehrlich-Institut. 15. Juli 2021, abgerufen am 20. Juli 2021.
- M. N. Oxman, M. J. Levin, G. R. Johnson et al.: A Vaccine to Prevent Herpes Zoster and Postherpetic Neuralgia in Older Adults. In: New England Journal of Medicine. 2. Juni 2005, Nr. 352, S. 2271–2284, doi:10.1056/NEJMoa051016 („Shingles prevention study“).
- STIKO zur Änderung der Fachinformation von Shingrix. In: RKI. 30. November 2020, abgerufen am 20. Juli 2021.
- A. C. Tricco, W. Zarin, R. Cardoso, A. A. Veroniki et al.: Efficacy, effectiveness, and safety of herpes zoster vaccines in adults aged 50 and older: systematic review and network meta-analysis. In: BMJ. Band 363, Oktober 2018, S. k4029, doi:10.1136/bmj.k4029, PMID 30361202, PMC 6201212 (freier Volltext).
- P. O. Lang, R. Aspinall: Vaccination for quality of life: herpes-zoster vaccines. In: Aging clinical and experimental research. Band 33, Nummer 4, April 2021, S. 1113–1122, doi:10.1007/s40520-019-01374-5, PMID 31643072 (Review).
- Studie zu Shingrix. In: Paul-Ehrlich-Institut. 16. Oktober 2020, abgerufen am 20. Juli 2021.
- Daniela Hüttemann: Fallberichte: Zoster-artige Läsionen nach Shingrix-Impfung. In: Pharmazeutische Zeitung. 26. Juni 2020, abgerufen am 1. September 2020.
- Staatsministerin für Soziales: Verordnung des Sächsischen Staatsministeriums für Soziales und Verbraucherschutz über die Erweiterung der Meldepflicht für übertragbare Krankheiten und Krankheitserreger nach dem Infektionsschutzgesetz. Vollzitat: Verordnung des Sächsischen Staatsministeriums für Soziales und Verbraucherschutz über die Erweiterung der Meldepflicht für übertragbare Krankheiten und Krankheitserreger nach dem Infektionsschutzgesetz vom 3. Juni 2002 (SächsGVBl. S. 187), die zuletzt durch die Verordnung vom 9. November 2012 (SächsGVBl. S. 698) geändert worden ist. In: revosax.sachsen.de. Abgerufen am 16. November 2020 (Fassung gültig ab: 16. Dezember 2012).