Bortrichlorid
Bortrichlorid ist eine gasförmige chemische Verbindung aus der Gruppe der Bor-Halogen-Verbindungen bzw. anorganischen Chlorverbindungen.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
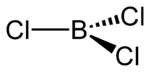 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Bortrichlorid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | BCl3 | ||||||||||||||||||
| Kurzbeschreibung |
farbloses Gas[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 117,17 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
gasförmig | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
12,5 °C[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
Zersetzung in Wasser[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
−403,8 kJ/mol[3] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Bortrichlorid wird industriell durch direkte Chlorierung von Bortrioxid und Kohlenstoff bei 500 °C gewonnen.[4]
Diese Synthese ist analog zum Kroll-Prozess.
Alternativ ist auch die Synthese direkt aus Borsäure über den Zwischenschritt von Triphenylborat möglich.[4]
Ebenfalls möglich ist eine Direktsynthese aus den Elementen Bor und Chlor.
Zur Darstellung kleiner Mengen sehr reinen Bortrichlorides im Labor wird die gasförmige Verbindung Bortrifluorid mit wasserfreiem Aluminiumchlorid umgesetzt[5]
Alternativ kann ein Gemisch von Kaliumtetrafluoroborat mit Aluminiumchlorid über mehrere Stunden erhitzt werden, um die gasförmige Verbindung zu erzeugen. Diese sollte im Anschluss allerdings zur Aufreinigung einer fraktionierten Destillation unterworfen werden[5]
Eigenschaften
Bortrichlorid ist ein unbrennbares, farbloses, an feuchter Luft durch Bildung von Chlorwasserstoff-Nebel stark rauchendes Gas.
Bei Kontakt mit Wasser reagiert es heftig unter Bildung von Salzsäure und Borsäure:
Der kritische Punkt liegt bei 178,8 °C, 38,7 bar und 0,790 kg/l; der Tripelpunkt bei −107 °C und 0,373 mbar.[1] Bortrichlorid ist eine Lewis-Säure und reagiert leicht mit tertiären Aminen, Phosphinen, Ethern, Thioethern und Halogenid-Ionen.[6] Es besitzt eine spezifische Verdampfungsenthalpie von 203 kJ/kg, spezifische Wärmekapazität von 0,5345 kJ/(kg·K) und eine Wärmeleitfähigkeit von 110·10−4 W/(m·K) (als Gas bei 25 °C und 1 bar Druck).[7]
Verwendung
Bortrichlorid wird als Katalysator, zur Synthese anderer chemischer Verbindungen (z. B. Borazin), für Chlorierungen, zur Beseitigung von Nitriden, Carbiden und Oxiden aus Schmelzen von Aluminium-, Magnesium-, Zinn- und Kupferlegierungen sowie zur Dotierung von Halbleitern verwendet.[1]
Einzelnachweise
- Eintrag zu Bortrichlorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- Eintrag zu Boron trichloride im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-5.
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3.
- E. Lee Gamble: Boron chloride and bromide. In: Ludwig F. Audrieth (Hrsg.): Inorganic Syntheses. Band 3. McGraw-Hill, Inc., 1950, S. 27–30 (englisch).
- W. Gerrard, M. F. Lappert: Reactions Of Boron richloride With Organic Compounds. In: Chemical Reviews. Bd. 58, Nr. 6, 1958, S. 1081–1111, doi:10.1021/cr50024a003.
- Datenblatt (Messer) (Seite nicht mehr abrufbar, Suche in Webarchiven) Info: Der Link wurde automatisch als defekt markiert. Bitte prüfe den Link gemäß Anleitung und entferne dann diesen Hinweis. (PDF; 254 kB).


