Tris(hydroxymethyl)nitromethan
Tris(hydroxymethyl)-nitromethan ist das Produkt der vollständigen Umsetzung von Nitromethan mit Formaldehyd und ähnelt strukturell dem Formaldehydabspalter Bronopol, dessen Bromatom im THNM durch eine Hydroxymethylgruppe ersetzt ist. Die Verbindung wird als Biozid zur Konservierung flüssiger technischer Produkte und als Ausgangsstoff für chemische Synthesen eingesetzt.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
nitromethan_Struktur.svg.png.webp) | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Tris(hydroxymethyl)-nitromethan | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C4H9NO5 | ||||||||||||||||||
| Kurzbeschreibung | |||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 151,12 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
sehr gut wasserlöslich (220 g·l−1 bei 20 °C), gut löslich in Ethanol, sehr wenig löslich in Benzol[2] | ||||||||||||||||||
| Brechungsindex |
1,4183 (25 °C, 589 nm)[4] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Vorkommen und Darstellung
Der belgische Chemiker Louis Henry beschrieb bereits 1895 die später als Henry-Reaktion bezeichnete Nitroaldol-Reaktion von Nitromethan mit überschüssigem Formaldehyd in Gegenwart eines basischen Katalysators, wie z. B. Natriumhydroxid.[6][7]
nitromethan_Synthese.svg.png.webp)
Die Reaktion verläuft exotherm und liefert auch bei Einsatz stöchiometrischer Massen Formaldehyd meist ein Gemisch aus Mono-, Di- und Triadditionsprodukt. Bei überstöchiometrischem Formaldehydeinsatz entstehen Verfärbungen durch (teerartige) Polymere, und das am Feststoff anhaftende überschüssige Formaldehyd muss bei der Aufarbeitung umständlich entfernt werden.
Daher wurden kontinuierliche Verfahren vorgeschlagen, die im Wesentlichen darauf abzielen, bei leicht überstöchiometrischen Formaldehydeinsatz die Verweildauer bei erhöhter Temperatur im Reaktor zu reduzieren.[8] Unter kontrollierten Bedingungen können im kontinuierlichen Betrieb Ausbeuten von > 97 % erzielt werden.[9]
Eigenschaften
Tris(hydroxymethyl)-nitromethan ist als Reinprodukt ein weißes geruchloses Kristallpulver, das sich sehr gut in Wasser und in polaren Alkoholen, wie z. B. Ethanol löst. Aus höheren Alkoholen, wie z. B. Amylalkohol kann das Rohprodukt umkristallisiert werden. In Wasser gelöst (0,1 mol·l−1)[3] stellt sich ein pH-Wert von 4,5 ein, bei dem Trimethylolnitromethan stabil, d. h. in der Anwendung als Biozid unwirksam ist. Bei pH-Werten >7,5 spaltet THNM langsam Formaldehyd ab, wodurch die bakterizide Wirkung einsetzt.
Anwendungen
Das funktionelle Amin 2-Amino-1,3-propandiol (Serinol), ein Strukturelement des Antibiotikums Chloramphenicol und Vorstufe für Sphingosine, Fungizide und Arzneistoffe, ist aus Trimethylnitromethan nach Ketalbildung mit Aceton, Abspaltung der noch freien Hydroxymethylgruppe, Hydrierung zur Aminogruppe und Abspaltung der Ketal-Schutzgruppe zugänglich.[10]

Die strukturelle Ähnlichkeit von Tris(hydroxymethyl)-nitromethan mit Glycerin legt die Verwendung als Ausgangssubstanz für Sprengstoffe nahe. Der resultierende Trinitratester ist ein Sekundärsprengstoff.
Die Puffersubstanz TRIS wird bei der katalytischen Hydrierung von Tris(hydroxymethyl)-nitromethan in Methanol mit Raney-Nickel in bis zu 90 %iger Ausbeute erhalten.[11]

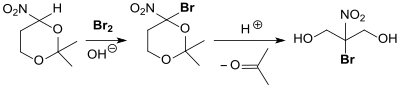
Der Syntheseweg des Biozids Bronopol verläuft ebenfalls über die Serinol-Zwischenstufe 2,2-Dimethyl-5-nitro-1,3-dioxan, das im Alkalischen bromiert wird. Anschließend wird die Schutzgruppe im Sauren abgespalten. Die Gesamtausbeute, ausgehend von THNM, beträgt ca. 73 %.[12]
Hauptanwendung von Tris(hydroxymethyl)-nitromethan ist als Formaldehydabspalter (engl. formaldehyde releaser oder formaldehyde donor) zur bioziden Ausrüstung von wässrigen Systemen wie z. B. Klebstoffen und Leimen, Kühlschmiermitteln in der Metallbearbeitung, Bohrschlämmen und Fracking-Fluiden in der Öl- und Gasindustrie, als Topf-Konservierungsmittel für Latexfarben, Polymeremulsionen, sowie als Desinfektionsmittel, Schleimbekämpfungsmittel und Desodorierungsmittel für zirkulierende industrielle Wassersysteme, z. B. in der Zellstoff- und Papierindustrie.[13] Typische Konzentrationen in Zubereitungen liegen zwischen 50 bis 1,000 ppm.[13] Zur Erhöhung der bioziden Wirkung werden oft Gemische mit Isothiazolinonen oder Glutaraldehyd[14] eingesetzt. Daneben sind Anwendungen von THNM zur Viskositätskontrolle in kosmetischen Zubereitungen, als Crosslinker in Polyurethanen und bei der Herstellung von Sprengstoffformulierungen[15] beschrieben.
Sicherheitshinweise
Tris(hydroxymethyl)-nitromethan wird – im Gegensatz zu vielen anderen Formaldehydabspaltern – praktisch nur technischen Produkten zur Konservierung zugesetzt.[16] Die Werte für die akute und subchronische orale und dermale Toxizität von Tri(hydroxymethyl)-nitromethan sind toxikologisch nicht signifikant und Ames-Tests auf Mutagenität waren negativ.[17]
Vereinzelte Befunde zur Sensibilisierung durch Trimethylolnitromethan zeigen mit 0 bis 0,6 % sehr niedrige Prävalenz.[16]
Gemäß den von der BAuA erarbeiteten Technische Regeln für Gefahrstoffe (TRGS) in der Ausgabe TRGS 611[18] darf 2-Hydroxymethyl-2-nitro-1,3-propandiol als „nitrosierendes Agens“ wegen der Gefahr der Bildung karzinogener Nitrosamine (seit 1993) in Deutschland in Kühlschmierstoffen nicht verwendet werden.
Einzelnachweise
- Eintrag zu TRIS-HYDROXYMETHYLNITROMETHANE in der CosIng-Datenbank der EU-Kommission, abgerufen am 30. Dezember 2021.
- Eintrag zu 2-(Hydroxymethyl)-2-nitro-1,3-propanediol bei TCI Europe, abgerufen am 4. April 2020.
- Eintrag zu Tris(hydroxymethyl)nitromethan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 4. April 2020. (JavaScript erforderlich)
- Carl L. Yaws: Thermophysical Properties of Chemicals and Hydrocarbons, 2nd Edition. Elsevier Inc., Amsterdam, NL 2015, ISBN 978-0-12-800834-8, S. 57.
- Datenblatt Tris(hydroxymethyl)nitromethane bei Sigma-Aldrich, abgerufen am 4. April 2020 (PDF).
- Louis Henry: Formation synthétique d’alcools nitrés. In: Comptes rendus. Band 120, S. 1265–1268 (bnf.fr).
- L. Henry: A propos des alcools nitrés. In: Recueil des Travaux Chimiques des Pays-Bas. Band 16, Nr. 8, 1897, S. 250–252, doi:10.1002/recl.18970160803.
- Patent DE1910458: Verfahren zur Herstellung von Tris-(hydroxymethyl)-nitromethan. Angemeldet am 1. März 1969, veröffentlicht am 6. November 1969, Anmelder: Commercial Solvents Corp., Erfinder: H.S. Vierk, W.A. den Adel.
- Patent US2301259: Method of producing nitrohydroxy compounds. Angemeldet am 25. Oktober 1939, veröffentlicht am 10. November 1942, Anmelder: Hercules Powder Co., Erfinder: R.F.B. Cox.
- Patent EP0348223A2: Novel process for the preparation of serinol. Angemeldet am 23. Juni 1989, veröffentlicht am 27. Dezember 1989, Anmelder: W.R. Grace & Co.-Conn., Erfinder: J.M. Quirk, S.G. Harsy, C.L. Hakansson.
- Patent US4233245: Preparation of tris(hydroxymethyl)aminomethane. Angemeldet am 25. Januar 1979, veröffentlicht am 11. November 1980, Anmelder: Societé Chimique de La Grande Paroisse, Azote et Produits Chimiques, Erfinder: J. Bourguignon, M.-X. Sion, M. Moreau.
- Patent US4851588: Novel process for the preparation of bronopol. Angemeldet am 23. Juli 1988, veröffentlicht am 25. Juli 1989, Anmelder: W.R. Grace & Co.-Conn., Erfinder: R.J. Kupper, F. Jachimowicz, J.M. Quirk, C.L. Hakansson.
- Tris(hydroxymethyl)nitromethane. In: Product Safety Assessment. The Dow Chemical Company, 12. November 2014, abgerufen am 6. April 2020.
- Patent EP2700313B1: Biocidal compositions comprising glutaraldehyde and tris(hydroxymethyl)nitromethane and methods of use. Angemeldet am 26. Februar 2014, veröffentlicht am 23. Dezember 2015, Anmelder: Dow Global Technologies LLC, Erfinder: B. Yin.
- Li, J.; Brill, T.B.: Nanostructured Energetic Composites of CL-20 and Binders Synthesized by Sol Gel Methods in Propellants Explosives Pyrotechnics 31 (2006) 61–69, doi:10.1002/prep.200600010.
- A. de Groot, J. Geier, M.-A. Flyvholm, G. Lensen, P.-J. Coenraads: Formaldehyde-releasers: relationship to formaldehyde contact allergy. Metalworking fluids and remainder. Part 1. In: Contact Dermatitis. Band 63, Nr. 3, 2010, S. 117–128, doi:10.1111/j.1600-0536.2010.01714.x.
- Tris Nitro®. In: Technical Bulletin. Angus Chemical Company, 1998, abgerufen am 7. April 2020.
- Verwendungsbeschränkungen für wassermischbare bzw. wassergemischte Kühlschmierstoffe, bei deren Einsatz N-Nitrosamine auftreten können. In: TRGS 611. BAuA, Mai 2007, abgerufen am 7. April 2020.
