Rubidiumcarbonat
Rubidiumcarbonat ist eine chemische Verbindung aus der Gruppe der Rubidiumverbindungen und Carbonate.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
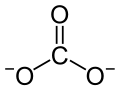 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Rubidiumcarbonat | |||||||||||||||
| Summenformel | Rb2CO3 | |||||||||||||||
| Kurzbeschreibung |
weißer geruchloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 230,95 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
3,55 g·cm−3[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−1136,0 kJ/mol[4] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Rubidiumcarbonat kann durch Reaktion von Ammoniumcarbonat mit Rubidiumhydroxid gewonnen werden.[5]
Eine andere Methode ist die Oxidation von Rubidiumoxalat.
Bei der Verarbeitung des Minerals Lepidolith erhält man ein Gemisch aus Kaliumcarbonat, Rubidiumcarbonat und Caesiumcarbonat.
Eigenschaften
Physikalische Eigenschaften
Rubidiumcarbonat ist ein weißer, geruchloser, feuchtigkeitsempfindlicher, luftempfindlicher, hygroskopischer Feststoff. Er kommt in drei Kristallmodifikationen vor, wobei bei Raumtemperatur nur die alpha-Form vorliegt. Die Raumgruppen für die Modifikationen sind P21/c (Nr. 14) mit den Gitterparametern a = 734,4 pm, b = 1011,6 pm, c = 587,26 pm, sowie vier Formeleinheiten pro Elementarzelle,[2] Pnma (Nr. 62) und P63/mmc (Nr. 194). Sie entsprechen damit denen von Kalium- und Caesiumcarbonat.[6]
In 100 g absolutem Ethanol lösen sich 0,74 g Rubidiumcarbonat.[7]
Die Standardbildungsenthalpie von Rubidiumcarbonat beträgt −1150 kJ·mol−1.[8]
Chemische Eigenschaften
Rubidiumcarbonat dissoziiert oberhalb von 900 °C.[9]
Beim Einleiten von Kohlendioxid in die wässrige Lösung bildet sich Rubidiumhydrogencarbonat.[10]
Beim Erhitzen mit Magnesium im Wasserstoffstrom bildet sich Rubidiumhydrid.[11]
Verwendung
Rubidiumcarbonat wird zur Herstellung von Spezialgläsern[12] und als Katalysator zur Herstellung von kurzkettigen Alkoholen aus Erdgas und zur Herstellung anderer Rubidiumverbindungen verwendet.[13]
Rubidiumcarbonat kann zur analytischen Trennung von Rubidium und Caesium verwendet werden, da es in Ethanol kaum löslich ist, Caesiumcarbonat jedoch gut löslich ist.[3]
Einzelnachweise
- Eintrag zu Rubidiumcarbonat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- Jean D’Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. 3. Elemente, anorganische Verbindungen und Materialien, Minerale. Band 3. 4. Auflage. Springer, 1997, ISBN 978-3-540-60035-0, S. 684 (eingeschränkte Vorschau in der Google-Buchsuche).
- K. A. Hofmann: Lehrbuch der anorganischen Chemie. 2. Auflage 1919. Verlag F. Vieweg & Sohn, S. 439 (Textarchiv – Internet Archive).
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-20.
- Rubidium. In: Encyclopædia Britannica. 11. Auflage. Band 23: Refectory – Sainte-Beuve. London 1911, S. 808 (englisch, Volltext [Wikisource]).
- Sascha Vensky: Konformationsaufklärung anorganischer Oxoanionen des Kohlenstoffs und Festkörpersynthesen durch Elektrokristallisation von Ag3O4 und Na3BiO4. Stuttgart 2004, DNB 97181533X, urn:nbn:de:bsz:93-opus-19129 (Dissertation, Universität Stuttgart).
- Aterton Seidell: Solubilities Of Organic Compounds Vol – I. S. 1432 (Textarchiv – Internet Archive).
- Fania Moriseevna Perelman: Rubidium and Caesium. Verlag Pergamon Press, 1965, S. 46, doi:10.1002/ange.19660780727 (eingeschränkte Vorschau in der Google-Buchsuche).
- Dale L. Perry, Sidney L. Phillips: Handbook of inorganic compounds. CRC Press, 1995, ISBN 978-0-8493-8671-8, S. 333 (eingeschränkte Vorschau in der Google-Buchsuche).
- R. Abegg, F. Auerbach: Handbuch der anorganischen Chemie. Band 2. Verlag S. Hirzel, 1908, S. 435 (Textarchiv – Internet Archive).
- J. W. Mellor: A comprehensive treatise on inorganic and theoretical chemistry. Band 2. Verlag Wiley, 1962, S. 2186 (eingeschränkte Vorschau in der Google-Buchsuche).
- Winfried Lenk, Horst Prinz, Anja Steinmetz: Rubidium and Rubidium Compounds. In: Ullmann’s Encyclopedia of Industrial Chemistry. Wiley-VCH Verlag, 2000, ISBN 978-3-527-30673-2, doi:10.1002/14356007.a23_473.pub2.
- micronmetals: Rubidium carbonate (Memento vom 6. Oktober 2010 im Internet Archive)
