Rosiglitazon
Rosiglitazon ist ein Antidiabetikum aus der Gruppe der Insulin-Sensitizer zur Behandlung des Diabetes mellitus Typ 2. Das Wirkprinzip ist eine Erhöhung der Empfindlichkeit des Gewebes auf Insulin. Das körpereigene Insulin ist folglich wieder effektiver in der Lage, erhöhte Blutzuckerspiegel zu senken.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
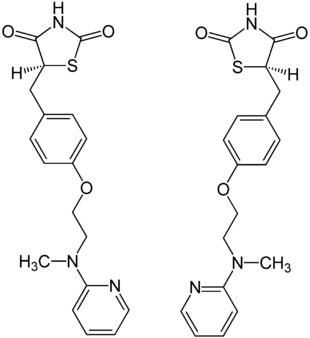 | ||||||||||||||||||||||
| 1:1-Gemisch aus (S)-Rosiglitazon (links) und (R)-Rosiglitazon (rechts) | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Rosiglitazon | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel |
| |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
A10BG02 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus |
orales Antidiabetikum | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | ||||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Seit November 2010 ruht auf Anordnung des Bundesinstituts für Arzneimittel und Medizinprodukte (BfArM) in Deutschland die Verkehrsfähigkeit für Arzneimittel mit dem Wirkstoff Rosiglitazon. Ihr Nutzen-Risiko-Verhältnis war seitens des Ausschusses für Humanarzneimittel (CHMP) bei der Europäischen Arzneimittelagentur als insgesamt ungünstig eingestuft worden (kardiovaskuläre Risiken, gehäufte Herzinfarkte).[3][4] Neuere Studien zeigen jedoch, dass die ursprünglichen Bedenken möglicherweise unbegründet sind, laut einer Überprüfung erhöht Rosiglitazon (Handelsname Avandia) das Herzinfarktrisiko nicht. Die Rohdaten seien in der Originalstudie, die zusätzlich nicht verblindet war, mehr oder weniger bewusst manipuliert worden. Das wirtschaftliche Interesse an der neuerlichen Vermarktung des Medikaments ist aktuell jedoch gering, da das Patent bereits ausgelaufen ist.[5]
Rosiglitazon scheint den herkömmlichen Antidiabetika bei höheren Kosten nicht überlegen zu sein.[6]
Pharmakologische Angaben
Wirkungen
Dem Wirkmechanismus der Insulin-Sensitizer entsprechend aktiviert Rosiglitazon nach oraler Aufnahme im Zellkern den PPAR-Rezeptor (peroxisome proliferator-activated receptors) vom Typ γ. Dieser Rezeptor ist an der Regulation verschiedener Mechanismen im Kohlenhydrat- und Fettstoffwechsel beteiligt. Die Aktivierung erhöht die Empfindlichkeit der Zellen von Leber, Muskulatur und Fettgewebe für Insulin (Senkung der Insulinresistenz). Auch die Wirkung von zugeführtem Insulin wird verstärkt. Fettsäuren und Glukose werden dadurch vermehrt in die Zellen aufgenommen und im Stoffwechsel umgesetzt. In der Leber verringert sich zusätzlich die Neubildung von Glukose.[7][6]
Rosiglitazon hat neben den Wirkungen im Stoffwechsel zusätzlich entzündungshemmende Eigenschaften. Es senkt die Konzentration von NF-κB (Nukleärer Faktor κB) und erhöht die Konzentration von IκB (inhibitorisches kappa-B) in Entzündungszellen.[8] Aufgrund tierexperimenteller Untersuchungen wurde auch eine therapeutische Wirkung bei der Alzheimer-Erkrankung und der Alzheimer-Demenz diskutiert.[9]
Pharmakokinetik
Der maximale Spiegel im Blut wird aufgrund der schnellen Resorption aus dem Darm nach etwa einer Stunde erreicht. Die Bioverfügbarkeit beträgt dabei 99 %. Die Plasmaproteinbindung beträgt nahezu 100 %. Der Abbau erfolgt über das Cytochrom P450-System der Leber, die Metaboliten sind nicht wirkaktiv. Deren Ausscheidung geschieht zu 70 % über die Niere (renal), zu 30 % über den Stuhlgang. Die Plasmahalbwertszeit liegt bei drei bis vier Stunden, bei Lebererkrankungen kann sie verlängert sein. Eine Dosisanpassung bei Niereninsuffizienz ist nicht notwendig.[6][7]
Klinische Angaben
Anwendungsgebiete
Rosiglitazon ist angezeigt zur Behandlung des Diabetes mellitus vom Typ 2. Rosiglitazon wird entweder allein oder in Kombination mit anderen Arzneistoffen verwendet.[7]
- Monotherapie
- Die Monotherapie mit Rosiglitazon ist angezeigt bei Erwachsenen, deren Blutzucker durch Diät und Bewegung nicht hinreichend einstellbar ist und für die Metformin ungeeignet ist.
- Zweifach-Kombinationstherapie
- Die gleichzeitige Gabe zusammen mit entweder Metformin oder einem Arzneistoff aus der Gruppe der Sulfonylharnstoffe ist angezeigt, wenn eine alleinige Verabreichung dieser Wirkstoffe unzureichend wirksam ist.
- Dreifach-Kombinationstherapie
- Die gleichzeitige Gabe zusammen mit Metformin und einem Sulfonylharnstoff ist angezeigt bei Erwachsenen, bei denen der Blutzucker mit einer Zweifach-Kombinationstherapie nur unzureichend einstellbar ist.
Nebenwirkungen
Die häufigsten unerwünschten Wirkungen sind Ödeme, Blutarmut (Anämie), Gewichtszunahme und Erhöhung der Cholesterinwerte im Blut (Hypercholesterinämie). Diese treten in Kombination mit Insulin deutlich häufiger auf als unter Einzelmedikation mit Rosiglitazon. In Kombination mit Insulin oder einem Sulfonylharnstoff treten zudem sehr häufig dosisabhängig Unterzuckerungen (Hypoglykämie) auf. Weiter kann es zu erhöhtem Appetit und Körpergewicht, Verstopfung (Obstipation) sowie Leberschädigungen mit Erhöhung der Transaminasen, jedoch nur sehr selten mit manifester Leberentzündung (Hepatitis), kommen. Nur selten kommt es zu einer Entzündung des Pankreas (Pankreatitis), anaphylaktischen Reaktionen, zu Angioödem, Urtikaria, Ausschlag und Juckreiz der Haut oder einem Makulaödem des Auges.[7] Insbesondere in Kombination mit Insulin kann es zu einem Sauerstoffmangel des Herzmuskels kommen.[7]
Im Mai 2005 veröffentlichte das BfArM, dass in Studien ein erhöhtes Risiko für Knochenbrüche bei Frauen gefunden wurde; die Produktinformationen wurden ergänzt und die Ärzteschaft per Rote-Hand-Brief informiert.[10]
Bei einer Auswertung von 42 Studien, die im Juni 2007 im New England Journal of Medicine veröffentlicht wurde, wurde ein um 43 % erhöhtes Herzinfarktrisiko beobachtet.[11] Der Hersteller des Medikamentes sowie die Europäische Arzneimittelagentur zweifelten die Aussagekraft der Metastudie an.[12] Eine unabhängige Kontrolle der Studiendaten bestätigt nun den Zweifel, Rosiglitazon stelle doch kein erhöhtes Risiko für Herzinfarkte dar.[13] Die FDA hat deswegen auch schon die Auflagen zur Verschreibung von Rosiglitazon gelockert.
Aufgrund des angeblich erhöhten Risikos kardiovaskulärer Erkrankungen bei Einnahme von Rosiglitazon-Präparaten empfahl die Europäische Arzneimittelagentur (EMA) schließlich im September 2010 die Aufhebung der Zulassung in Europa.[14] Das deutsche Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) kam dieser Empfehlung nach, sodass Rosiglitazon seit November 2010 in Deutschland nicht mehr erhältlich ist.
Nach Aussage eines ehemaligen Mitarbeiters der Food and Drug Administration (FDA) hat der Avandia-Hersteller GlaxoSmithKline PLC Datenmaterial über das Risiko zurückgehalten.[15] Eine Expertenrunde derselben Behörde hat mehrheitlich Bedenken gegen "Avandia" bekundet, ebenfalls eine Mehrheit derselben aber sich dafür ausgesprochen, das Medikament unter bestimmten Bedingungen auf dem Markt zu behalten.[16]
Interaktionen
Rosiglitazon wird hauptsächlich durch die Cytochrom P450-Isoenzyme CYP2C8 und CYP2C9 metabolisiert. Deshalb kann es bei gleichzeitiger Einnahme von Medikamenten mit Beeinflussung von CYP2C8 wie Rifampicin, Trimethoprim oder Gemfibrozil zu Schwankungen des Wirkstoffspiegels kommen. Wechselwirkungen mit Phenytoin, Carbamazepin, Phenobarbital und Johanniskraut können nicht ausgeschlossen werden. Die Pharmakokinetik der Cumarinderivate Warfarin und Acenocumarol, die ebenfalls über CYP2C9 abgebaut werden, ist hingegen unbeeinflusst. Weiter ist eine Verstärkung der Wirkung von Methotrexat möglich. Ein mäßiger Alkoholkonsum während der Einnahme hat keinen Einfluss auf die Wirkung.[7]
Gegenanzeigen
Rosiglitazon ist kontraindiziert bei bekannter Überempfindlichkeit gegen Rosiglitazon, bei Herzinsuffizienz sowie Leberfunktionsstörungen. Auch die Kombination mit Insulin ist aufgrund der stark erhöhten Nebenwirkungsraten nicht angezeigt.
Für die Anwendung im Alter unter zehn Jahren liegen keine Daten vor. Eine Anwendung wird nicht empfohlen. Rosiglitazon ist plazentagängig, während Schwangerschaft und Stillzeit darf die Anwendung deshalb nicht erfolgen, wenn auch keine Daten über die Toxizität beim Menschen vorliegen.[7]
Chemische und pharmazeutische Angaben
Rosiglitazon ist chiral. Die Handelspräparate enthalten den Arzneistoff als Racemat (1:1-Gemisch der Enantiomere).
Rosiglitazon ist oral anwendbar und als Filmtablette formuliert. Die Filmtabletten enthalten den Arzneistoff als Salz der Maleinsäure (Rosiglitazonmaleat). Rosiglitazon ist verschreibungspflichtig.
Siehe auch
Einzelnachweise
- The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage. 2006, ISBN 0-911910-00-X, S. 1427.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- DAZ online, Arzneimittelkommission: BfArM ordnet Vertriebseinstellung an (Memento des Originals vom 28. September 2010 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis., 23. September 2010.
- Aussetzung der Vermarktung von Arzneimitteln, die Rosiglitazon enthalten (Avandia®, Avandamet® und Avaglim®) in der europäischen Union (PDF; 243 kB), Rote-Hand-Brief vom 23. September 2010.
- Avandia: FDA soll Anwendungseinschränkungen lockern
- T. Koch, U. P. Masche: Rosiglitazon. In: pharma-kritik. Jahrgang 21, Nr. 9, 2000.
- Avandia: Produktinformationstexte (PDF; 3,1 MB), Stand Juli 2010.
- P. Mohanty, A. Aljada, H. Ghanim, D. Hofmeyer, D. Tripathy, T. Syed, W. Al-Haddad, S. Dhindsa, P. Dandona: Evidence for a potent antiinflammatory effect of rosiglitazone. In: J Clin Endocrinol Metab. 89(6), Jun 2004, S. 2728–2735. PMID 15181049.
- G. Landreth: PPARgamma agonists as new therapeutic agents for the treatment of Alzheimer's disease. In: Neurol. 199(2), Jun 2006, S. 245–248. PMID 16733054.
- Glitazone (Rosiglitazon, Pioglitazon): Erhöhtes Risiko für Frakturen bei Frauen. auf der Webseite des Bundesinstituts für Arzneimittel und Medizinprodukte
- Steven E. Nissen, Kathy Wolski: Effect of Rosiglitazone on the Risk of Myocardial Infarction and Death from Cardiovascular Causes. In: N Engl J Med. Vol. 356, No. 24, 14. Juni 2007. PMID 17517853.
- Stefan Schmitt: Herzinfarkt-Risiko - Studie sorgt für Streit um Blockbuster-Medikament. In: Spiegel online. 25. Mai 2007.
- FDA requires removal of some prescribing and dispensing restrictions for rosiglitazone-containing diabetes medicines.
- European Medicines Agency recommends suspension of Avandia, Avandamet and Avaglim. Presseveröffentlichung der Europäischen Arzneimittelagentur, 23. September 2010.
- Alicia Mundy: Grassley Says Glaxo Withheld Drug Data. In: The Wallstreet Journal. 12. Juli 2010.
- The Avandia Saga Continues. Editorial. In: The New York Times. 14. Juli 2010.
Handelsnamen
Alle Handelsnamen befinden sich Markenrechtlich im Besitz des britischen Pharmaunternehmens GlaxoSmithKline:
Avandia
- mit Glimepirid: Avaglim, Avandaryl
- mit Metformin: Avandamet