Restless-Legs-Syndrom
Beim Restless-Legs-Syndrom (kurz RLS), auch bekannt als Willis-Ekbom-Disease (kurz WED), handelt es sich um eine sensomotorische Störung, die sich durch einen unbändigen Bewegungsdrang und quälende Missempfindungen insbesondere in den Beinen äußert. Die Beschwerden treten dabei vornehmlich in Ruhe auf, bessern sich jedoch bei Bewegung. Typischerweise folgt die Erkrankung zirkadianen Rhythmen, d. h. die Beschwerden verstärken sich deutlich zum Abend bzw. zur Nacht hin, weshalb das RLS zu massiven Schlafstörungen führen kann.
Risikofaktoren für die Entwicklung eines sekundären RLS sind u. a. Eisenmangel bzw. Eisenmangelanämie, Vitamin-B12-Mangel, Folsäuremangel, Nierenfunktionsstörungen, Parkinson, Diabetes mellitus und Rheumatoide Arthritis. Darüber hinaus kann es auch als Nebenwirkung diverser Medikamente auftreten, insbesondere bei Antidepressiva und Neuroleptika. Bei Behandlung bzw. Behebung der zugrundeliegenden Ursachen kann ein sekundäres RLS wieder vollständig verschwinden. Die primäre oder idiopathische Form des RLS ist bislang hingegen weder heil- noch kausal behandelbar, insofern sich seine Ursache nach gegenwärtigem Stand der Medizin nicht feststellen lässt. Unabhängig davon, ob es sich um ein primäres oder sekundäres RLS handelt, hat sich die Gabe von Levodopa oder Dopaminagonisten als wirksames Mittel zur Linderung der Beschwerden bewährt.[1]
Das RLS wird den Schlafbezogenen Bewegungsstörungen zugerechnet und seit Veröffentlichung des ICD-11 als Schlaf-Wach-Störung kategorisiert. Zuvor war es unter dem ICD-10 der Gruppe Sonstiger näher bezeichneter extrapyramidaler Krankheiten und Bewegungsstörungen zugeordnet.[2]
Entdeckung
Thomas Willis hat die Störung zum ersten Mal als eine Akathisie (Ruhelosigkeit mit Bewegungsdrang) beschrieben.[3] 1945 hat dann Karl-Axel Ekbom das Syndrom als eine neurologische Störung identifiziert.[4] Daher wird gelegentlich auch vom Willis-Ekbom Syndrom gesprochen.
Symptomatik
Das RLS äußert sich in Form oft quälender Missempfindungen, mit denen stets ein unbändiger Bewegungsdrang einhergeht. Die Symptome treten dabei hauptsächlich in Phasen körperlicher Inaktivität auf, insbesondere bei längerem Sitzen oder Liegen und beschränken sich überwiegend auf die Beine. Sie können jedoch auch Arme und andere Körperpartien betreffen, in seltenen Fällen auch nur die Arme.[5] Charakteristisch ist die sofortige Linderung der Beschwerden, sobald dem Bewegungsdrang nachgegeben wird, sowie ihre baldige Rückkehr in der nächsten Ruhephase.
Die Stärke der notwendigen Bewegung hängt dabei von der Stärke der Symptome ab. So kann bei leichtem RLS ein Wippen mit den Füßen ausreichend sein, während schwerere Ausprägungen beispielsweise ein dauerhaftes Umhergehen oder sportliche Aktivität erzwingen. Im Allgemeinen verstärken sich die Beschwerden immer weiter, bis dem Bewegungsdrang nachgegeben wird, weshalb ihm – wenn überhaupt – nur kurzfristig widerstanden werden kann. Der Bewegungsdrang an sich verursacht jedoch keine unwillkürlichen Bewegungen wie Tics oder Tremores, d. h. die Betroffenen behalten dabei die volle Kontrolle über ihren Körper. Als häufige Begleiterscheinung bekannt sind allerdings periodisch oder aperiodisch auftretende Myoklonien, die sowohl im Schlaf- als auch im Wachzustand auftreten können. Beim RLS werden diese meist als Periodic Limb Movements (PLM) bezeichnet, sind jedoch nicht zu verwechseln mit der Periodic Limb Movement Disorder (PLMD), bei der es sich um eine eigenständige Erkrankung handelt. Nur im Schlaf auftretende Myoklonien sind den Patienten jedoch meist nicht bewusst.
Die auftretenden Missempfindungen selbst werden von Betroffenen auf unterschiedlichste Weise beschrieben, etwa als Ziehen, Spannen, Kribbeln, Ameisenlaufen, Druck-, Kälte- oder Wärmegefühl, aber auch als diffuse Schmerzen, Krämpfe oder eine Art Pulsieren.[6] Die genaue Lokalisation der Beschwerden in den betroffenen Körperpartien ist dabei überaus variabel. Oft beschränken sie sich auf die Unterschenkel bzw. -arme, können aber auch bis in die Oberschenkel bzw. Schultern ausstrahlen. Häufig werden die Empfindungen als tief in der Muskulatur, teilweise auch als in den Knochen sitzend beschrieben oder, was die Symptome in den Beinen betrifft, vom Knöchel über das untere Schienbein ins Knie aufsteigend. Die Beschwerden können beidseitig symmetrisch auftreten, aber auch nur einseitig oder alternierend.[7]
Charakteristisch ist die Verstärkung der Symptome zum Abend hin. Je nach Schweregrad können sie sich auch auf die Abend- und Nachtzeit beschränken, während der Rest des Tages weitgehend beschwerdefrei bleibt. Zudem kann sich die Erkrankung auch nur in tage- bis monatelangen Schüben manifestieren, auf die ebenso lange beschwerdefreie Phasen folgen. Leichte Formen treten mitunter auch nur unregelmäßig an einzelnen Tagen auf.[8]
Auswirkungen
Da sich der quälende Bewegungsdrang typischerweise zum Abend hin verstärkt und auch während des Schlafes persistiert, kann das RLS zu massiven Ein- und Durchschlafstörungen führen, insbesondere bei zugleich auftretenden PLMs. Betroffenen müssen sich dieser Schlafstörungen dabei nicht zwingend bewusst sein, v. a. wenn die Symptome nur zu gehäuften, aber unbewussten Arousals führen, jedoch nicht im Wachzustand präsent sind.
Das Ausmaß des Schlafmangels kann bei RLS-Patienten enorm sein und alle dafür typischen Konsequenzen nach sich ziehen, so etwa chronische Tagesschläfrigkeit, Antriebslosigkeit, chronische Erschöpfung, Konzentrationsstörungen, Gereiztheit, Vergesslichkeit, Schwindel, Migräne oder sogar Depressionen. Insbesondere bei schweren Ausprägungen, welche eine normale Nachtruhe praktisch vollkommen unmöglich machen, sind auch Zirkadiane Rhythmusstörungen zu beobachten. Aus einem schmerzhaften RLS kann sich zudem wie bei allen längerandauernden Schmerzzuständen ein chronisches Schmerzsyndrom entwickeln. Unbehandelt kann ein längerfristig bestehendes RLS einen massiven Leistungsabfall und soziale Isolation zur Folge haben und die Lebensqualität Betroffener somit massiv beeinträchtigen.
Symptomverstärkende Faktoren
Potentiell symptomverstärkende Faktoren sind beim RLS so individuell ausgeprägt wie die Erscheinungsformen der Krankheit selbst und hängen stark von deren Form (primär oder sekundär) sowie eventuell bestehenden Begleiterkrankungen ab. Eine allgemeingültige Aussage über symptomverstärkende Faktoren ist daher nur bedingt zu treffen.
Ein temporär deutlich negativer Einfluss auf die Symptome ist von Koffein bekannt,[9] insbesondere wenn es am Nachmittag zu sich genommen wird. Nicht als pathologisches RLS gilt jedoch aus zu hoher Koffeinzufuhr resultierende temporäre Unruhe oder Nervosität bei nicht von der Erkrankung betroffenen Personen.
Weiterhin wird häufig von einer deutlichen Verschlimmerung der Symptome infolge intensiver oder ungewohnter Bewegung am Tage berichtet, ebenso wie nach zu wenig Bewegung.[10][11][12] Moderate Bewegung am Tage kann die abendlichen Symptome hingegen lindern. Aussagekräftige Studien liegen zu diesen Zusammenhängen bislang jedoch nicht vor.
Eine längerfristige Behandlung mit L-Dopa kann zudem zu einer Aggravation der Symptomatik führen.
Diagnose
Die Diagnose des RLS erweist sich häufig als schwierig, da sich bei dieser Erkrankung einerseits keinerlei Biomarker feststellen lassen und andererseits die Vielfalt und Diffusität der Symptome leicht zu Fehldiagnosen führt. So können zwar bestimmte Krankheitsbilder, insbesondere ein Eisenmangel bzw. eine Eisenmangelanämie, als bekannte Ursachen eines sekundären RLS einen Hinweis auf die Diagnose geben, da neurologische und bildgebende Untersuchungen beim RLS jedoch in aller Regel unauffällig verlaufen,[13] kann die Diagnose letztlich nur anhand der Symptome gestellt werden. Hierzu werden folgende Kriterien herangezogen (nach Allen et al., 2014):[14]
Hauptkriterien (müssen alle erfüllt sein)
- Ein Drang, die Beine und/oder andere Körperteile zu bewegen, der meistens, aber nicht immer, begleitet wird von unangenehmen Empfindungen in den betroffenen Körperpartien oder der als von diesen verursacht wahrgenommen wird.
- Der Bewegungsdrang und die unangenehmen Empfindungen beginnen oder verschlimmern sich während Phasen der Ruhe oder Inaktivität, wie Liegen oder Sitzen.
- Der Bewegungsdrang und die unangenehmen Empfindungen werden durch Bewegung teilweise oder vollständig gelindert, wie etwa durch Gehen oder Dehnen, zumindest, solange die Aktivität anhält.
- Der Bewegungsdrang und alle begleitenden unangenehmen Empfindungen während Ruhe oder Inaktivität treten ausschließlich oder stärker am Abend oder in der Nacht auf als am Tag.
- Das Auftreten der obengenannten Kennzeichen lässt sich nicht ausschließlich als Symptome eines anderen medizinischen oder verhaltensbezogenen Zustandes erklären (z. B. Myalgie, venöse Stase, Beinödeme, Arthritis, Beinkrämpfe, positionsbedingte Beschwerden oder habituelles Fußklopfen).
Nebenkriterien (müssen nicht zwingend erfüllt sein)
- Vorhandensein periodischer Beinbewegungen im Schlaf (PLMS) oder im ruhenden Wachzustand (PLMW) jenseits der für das Alter oder den medizinischen bzw. medikamentösen Status erwarteten Häufigkeit und/oder Intensität
- zumindest anfängliches Ansprechen auf eine dopaminerge Behandlung
- positive Familienanamnese des RLS bei Verwandten ersten Grades
- Fehlen einer ausgeprägten Tagesmüdigkeit.
Die Anamneseerhebung kann sich beim RLS besonders schwierig gestalten, da Betroffene die Symptome häufig nur schwer beschreiben können oder teilweise nicht als solche erkennen. So wird der charakteristische Bewegungsdrang oft nicht als eigenständiges Symptom, sondern nur als Folge der Missempfindungen wahrgenommen. Gerade auch schmerzhafte Ausprägungen können die Diagnosefindung erschweren, wenn die Schmerzen vom Patienten als Hauptproblem wahrgenommen werden und dadurch andere Symptome verschleiern. Tritt ein RLS nur während des Schlafes auf und sind sich die Betroffenen infolgedessen der eigentlichen Symptome nicht bewusst, sondern nur deren vielfältigen Auswirkungen, kann die Diagnose teils auch nur im Schlaflabor gestellt werden.[15]
Differenzialdiagnosen
Differentialdiagnostisch muss das RLS vor allem gegen Polyneuropathie, Funikuläre Myelose, Vitamin-B12-Mangel, Radikulopathie, Akathisie, Venenleiden, Wadenkrämpfe (Crampi nocturni), arterielle Verschlusskrankheit („Schaufensterkrankheit“), Pruritus und Einschlafmyoklonien abgegrenzt werden. Die vielfältigen Begleiterscheinungen des RLS machen Betroffene jedoch anfällig für Fehldiagnosen. So führt die schwierige Diagnostik immer wieder zu regelrechten Ärztemarathons der Patienten, denen aufgrund der fehlenden Biomarker besonders häufig Hypochondrie, somatoforme Störungen, Depressionen oder andere psychische Leiden unterstellt werden. Infolgedessen wird die richtige Diagnose teils erst durch Psychiater gestellt.
Formen
Man unterscheidet zwischen einer sekundären (symptomatischen) und einer primären (idiopathischen) Form des RLS:
Sekundäre Form
Die sekundäre Form des RLS tritt meist als Folge eines anderen (Mangel-)zustandes oder einer anderen Erkrankung auf. Als häufige auslösende Faktoren bekannt sind[16]Eisenmangel und Eisenmangelanämie,[17] Folsäuremangel, Vitamin-B12-Mangel, perniziöse Anämie, Urämie, Niereninsuffizienz mit Dialyse,[18] Arthritis, Diabetes mellitus, Hypothyreose, Hyperthyreose, Fibromyalgie,[19] Polyneuropathie, Radikulopathie, Morbus Parkinson und andere neurologische Erkrankungen. Auch während einer Schwangerschaft ist ein RLS häufig zu beobachten. Ebenso kann es als Nebenwirkung von diversen Medikamenten auftreten, insbesondere bei Antidepressiva, Neuroleptika und Dopaminagonisten.[20] Auch nach schweren operativen Eingriffen, wie etwa einer Total-Endoprothese des Knies, kann es zum erstmaligen Auftreten eines RLS kommen.[21] Seltenere Auslöser können Bluthochdruck, Herzinfarkt und Schlaganfall sein.[22]
Lässt sich die Ursache des sekundären RLS beheben, kann dieses wieder vollständig verschwinden.
Idiopathische Form
Bei der idiopatischen Form des RLS liegen keine klinisch feststellbaren körperlichen Ursachen vor. Bekannt ist jedoch eine erbliche Prädisposition für die Erkrankung. Diese scheint bei einem Early-onset-RLS (Erstauftreten vor dem 45. Lebensjahr) stärker ausgeprägt zu sein als bei einem Late-onset der Erkrankung (nach dem 45. Lebensjahr).[23]
Ein idiopathisches RLS kann sich prinzipiell in jedem Alter erstmals manifestieren, besonders häufig jedoch in den Zwanzigern und Vierzigern.[24] Insbesondere in der Anfangszeit sowie bei leichteren Ausprägungen der Erkrankung können Form, Häufigkeit und Stärke der Beschwerden individuell erheblich variieren. Ein idiopathisches RLS ist dabei nach gegenwärtigen Kenntnisstand nicht degenerativ, es besteht jedoch eine Tendenz zur schleichenden Verschlimmerung der Symptomatik mit fortschreitendem Lebensalter, v. a. wenn die Symptome sich im jungen Alter erstmals zeigen. Bei einem erstmaligen Auftreten in höherem Alter, bleiben die Symptome eher langfristig stabil.[24] Ob sich ein idiopathisches RLS aus einem sekundären heraus entwickeln kann, ist bislang nicht geklärt.
Aufgrund der unbekannten Ursache ist das idiopathische RLS bisher nicht heilbar. Symptomatisch unterscheiden sich beide Formen RLS nicht, die idiopatische Form ist jedoch nur im Ausschlussverfahren zu diagnostizieren, wenn alle potentiellen Auslöser der sekundären Form als Ursachen definitiv ausgeschlossen werden können. Möglich ist indes auch eine zufällige, nicht kausale Komorbidität eines idiopathischen RLS mit einer der genannten Ursachen der sekundären Form, was jedoch nur schwer zu diagnostizieren ist. Eine Spontanheilung des idiopathischen RLS gilt als ungewöhnlich.
Epidemiologie
Die Prävalenz der Störung wird auf 5–10 % der kaukasischen Bevölkerung (Europa und Nordamerika) geschätzt. In Asien wird die Erkrankung seltener diagnostiziert. Frauen sind doppelt so häufig betroffen. Die Störung tritt selten auch schon im Kindesalter auf.[25]
Pathophysiologie
Für das pathophysiologische Verständnis der Störung werden verschiedene Erklärungspfade in Anschlag gebracht. Aufgrund der rein klinischen Definition der Erkrankung muss diese zunächst in Erinnerung gebracht werden. Das RLS ist eine sensomotorische Störung mit zirkadianer Ausprägung, wobei die Beschwerden durch Dopaminagonisten gemildert werden. Damit rücken drei Erklärungen ins Blickfeld:
- handelt es sich aufgrund der zirkadianen Symptomatik um eine Schlafstörung;[26][27]
- welche Beziehung besteht aufgrund der Wirksamkeit von Dopaminagonisten zum Parkinsonsyndrom;[28]
- was ist der – hypothetische – Ort der Läsion einer Dopamin-responsiven sensomotorischen Störung.[29]
- RLS und Schlafstörungen
Trotz der auffälligen tageszeitlichen Ausprägung der Störung sind die Beziehungen zu Schlafstörungen unklar. Das RLS ist nicht – wie viele andere Schlafstörungen – mit mitochondrialen Erkrankungen assoziiert.[30] Es gibt Übereinstimmungen genetischer Marker für RLS und Schlafstörungen, insbesondere im Falle des BTBD9-Markers.[31] Dieser Marker wird mit dem PLM-Syndrom ebenso in Verbindung gebracht wir mit dem RLS.[32][33] Eine BTBD9 Knockout-Mutante ("Wanderlust") ist bei der Fruchtfliege mit fragmentiertem Schlaf assoziiert.[34] In der Summe ist aber der kombinierte genetische Effekt der bisher identifizierten Marker mit 3 % nur gering.[35]
- RLS und Parkinsonsyndrom
Für die Beobachtung der Komorbidität von RLS und Parkinsonerkrankung (PD) können folgende Fragenkomplexe diskutiert werden:[36]
- das RLS könnte entweder eine Art Vorbote oder eine Folge der Parkinsonerkrankung sein
- beide Störungen verbindet eine "dopaminerge Brücke"
Die Komorbidität von RLS und PD ist intensiv untersucht worden.[37] Zahlreiche über Jahrzehnte durchgeführte Studien fanden dabei heraus, dass das Auftreten eines RLS bei Patienten mit PD zwischen 0 % und 52 % schwankt.[38] Auch ganz spezifische Studiendesigns zeigten uneinheitliche Ergebnisse. Wenn man neu an PD erkrankte und unbehandelte Probanden mit solchen vergleicht, deren PD behandelt wurde findet man unterschiedliche Prävalenzen für RLS in verschiedenen Ländern. Während sich in Europa die beiden og. Gruppen nicht unterscheiden, sieht man deutliche unterschiede bei koreanischen Patienten.[39] Die zum Teil völlig inkohärenten Befunde werden von manchen Forschern mit unzureichender Sorgfalt bei der Untersuchung der Probanden erklärt, in dem Sinne, dass Parkinsonsymptome für RLS-Symptome gehalten werden. Zur Differenzierung der pseudo-RLS-Symptomatik (mimicking RLS symptoms) beim Parkinson wird daher der "suggested immobilization Test" empfohlen.[40] Die oben genannte Alternative "Vorbote oder Folge" ist also anhand der Studienlage nicht entscheidbar. Demgegenüber kann mit Sicherheit gesagt werden, dass das Phänomen der Augmentation (Wirkungsverlust der Dopaminagonisten) bei PD mit PD sehr selten auftritt. Dies wird damit begründet, dass die dopaminergen Regelkreise der Störungen unterschiedlich sind: beim RLS eine Dopamin-Dysfunktion, beim PD ein Dopamin-Mangel. Das Stichwort der "dopaminergen Brücke" verliert damit seinen heuristischen Wert. Stattdessen wird man der Frage nachgehen, was der Ort der Läsion ist: welche dopaminergen Regelkreise sind möglicherweise beim RLS gestört?
Genetik
Es gibt eine genetische Veranlagung für die Entwicklung des primären (idiopathischen) Restless-Legs-Syndroms. Die Prävalenz der idiopathischen Form des RLS ist unter Angehörigen ersten Grades von RLS-Patienten drei- bis fünfmal so hoch wie bei Personen ohne RLS. Mehr als 50 % der Patienten mit einem idiopathischen RLS haben eine „positive Familienanamese“.[41] Die Veranlagung scheint zumindest teilweise autosomal-dominant vererbt zu werden. Durch Genomweite Assoziationsstudien konnten mittlerweile (Stand 2021) 23 Genvarianten bei hauptsächlich europäisch-stämmigen Patienten identifiziert werden, die mit einem höheren Risiko für ein idiopathisches RLS einhergehen. Für nicht-europäischstämmige Patienten liegen kaum Daten vor. Von den 23 bislang bekannten Genen wurden drei näher untersucht: MEIS1, PTPRD und BTBD9. MEIS1 und PTPRD spielen in der Entwicklung des Nervengewebes eine Rolle. Vom Tiermodell ist bekannt, dass eine gestörte Funktion von PTPRD und BTBD9 zu Schlafstörungen und Bewegungsauffälligkeiten führt.[42]
Behandlung
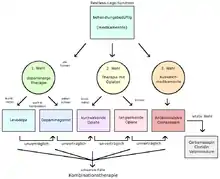
Die Behandlung muss an dem subjektiven Leidensdruck der Patienten ausgerichtet werden. Primär steht meist eine Verbesserung der Schlafqualität im Vordergrund. Eine bedarfsorientierte oder dauernde medikamentöse Therapie dürfte für die Mehrheit der Betroffenen mit ausgeprägter Symptomatik unausweichlich sein.
Bei der sekundären Form des RLS muss nach Möglichkeit die zugrundeliegende Ursache beseitigt werden; so sollten etwa kontra-indizierte Medikamente vermieden und erhöhte Nierenwerte notfalls durch Dialyse abgesenkt werden. Die Behandlung des RLS bei einer Schwangerschaft kann sehr schwierig sein.
In Fällen, in denen sich die Behandlung mit nur einer bestimmten Wirkstoffgruppe (Monotherapie) als nicht erfolgreich oder nach längerer Anwendung als zunehmend ineffizient erweist, kann der Arzt auch auf die Möglichkeit einer Kombinationstherapie (z. B. Dopaminagonist + L-Dopa) zurückgreifen.
Aggravation
Aggravation ist eine ernst zu nehmende Nebenwirkung vor allem bei der lang andauernden Behandlung mit Levodopa und Dopaminagonisten. Es ist zu unterscheiden von therapieunabhängigen („spontanen“) und von nach Absetzen der Medikamente erfolgenden („Rebound“) Verschlechterungen der RLS-Symptome. Das Kernsymptom der Aggravation ist ein früheres Eintreten der Symptome im Tagesverlauf (mindestens 4 Stunden im Vergleich zu Beginn der aktuellen Therapie). Aggravation zeigt sich ferner, indem die Zeit der Ruhe bis zum Eintreten der Beschwerden kürzer wird: Traten RLS-Beschwerden beispielsweise vorher erst nach Stunden auf, sind sie nun schon nach wenigen Minuten da. Das dritte Symptom von Aggravation ist die Ausbreitung der Beschwerden von den Beinen auf andere Körperteile, insbesondere die Arme.[43] Die derzeit für RLS geltende Leitlinie empfiehlt in solchen Fällen, auf Opiate, Gabapentin oder Pregabalin umzustellen, auch wenn diese Wirkstoffe derzeit für diese Indikation nicht zugelassen seien.
Levodopa (L-Dopa)
Als Therapie bei leichten und nur gelegentlich auftretenden Beschwerden gilt vor allem die Verabreichung von Levodopa (z. B. Restex, Madopar), einer Vorstufe von Dopamin. Es führt zu fast sofortiger Linderung der Beschwerden. Die dauerhafte Gabe führt allerdings bei einigen Patienten nach längerer Anwendung zur Aggravation (s. o.): Sie ist die häufigste und wichtigste der Nebenwirkungen von Levodopa. In einigen Fällen kann die Aggravation mit einer geringeren täglichen Dosis oder Verteilung der Dosis auf mehrere kleine Dosen rückgängig gemacht werden.[44] Außerdem stellen Toleranzentwicklung sowie schnelles Abklingen der Wirkung im Laufe der Nacht ein häufiges Problem dar.
Dopaminagonisten
Bei der Behandlung schwerer bzw. täglicher Beschwerden gelten dopaminähnlich wirkende Substanzen (Dopaminagonisten) inzwischen als Mittel der Wahl. Diese Substanzen stimulieren Dopamin-Rezeptoren.
- Von Mutterkornalkaloiden abgeleitete Dopaminagonisten (auch „ergoline Dopaminagonisten“ oder „Ergot-Derivate“ genannt) wie die auch bei der Therapie des Morbus Parkinson eingesetzten Cabergolin (Cabaseril®) und Pergolid (Parkotil®) sind hochwirksame, wenngleich nicht unumstrittene und nebenwirkungsreiche Wirkstoffe beim RLS. Sie können aber, sofern sie vertragen werden, zeitlich unbegrenzt eingenommen werden und steigern die Lebensqualität der Betroffenen erheblich (ca. 50 % der Anwender sind länger als ein Jahr beschwerdefrei). Weitere eingesetzte Substanzen dieser Wirkstoffgruppe sind Bromocriptin und Lisurid. Die deutschen Krankenkassen bezahlen die kostenintensive RLS-Therapie mit diesen Substanzen (Off-Label-Use) inzwischen in der Regel nicht mehr.
- Die nicht von Mutterkornalkaloiden abgeleiteten (nonergolinen) Dopaminagonisten Ropinirol (Adartrel® bzw. Requip®) und Pramipexol (Sifrol® bzw. Mirapexin®), welche beide Anfang 2006 für die Behandlung von RLS zugelassen wurden, können die Symptome des RLS ebenfalls lindern.[45] Bei lang andauernder Behandlung beispielsweise mit Pramipexol kommt es nicht derart häufig zur Augmentation wie unter L-Dopa. Die Medikamente stellen daher aktuell neben der Behandlung mit L-Dopa-Präparaten den Goldstandard in der Behandlung des RLS dar.
- Studien zu Dopaminagonisten in transdermaler Applikation (Pflaster) mit dem Wirkstoff Rotigotin (Neupro®-Pflaster, Leganto®-Pflaster) haben Wirksamkeit und Verträglichkeit dieses Wirkstoffs und der Darreichungsform gezeigt.[46] Als besonderes Merkmal scheint bei der transdermalen Rotigotin-Therapie das Risiko einer Augmentation besonders gering.[47] Inzwischen wird sie erfolgreich bei Morbus Parkinson und beim RLS eingesetzt. Ein weiterer Kandidat für diese Anwendungsform ist Lisurid.[48]
Opioide
Opioide wie Tilidin (z. B. Valoron N), Oxycodon (z. B. Targin) oder Codein stehen in schweren und schwersten, vor allem schmerzhaften Fällen bzw. bei Versagen anderer Therapieversuche als (stärkstes) Mittel zur Behandlung zur Verfügung. Außerdem können sie ebenso wie Levodopa ergänzend zu einer Basistherapie eingesetzt werden.[49][50][51] Nachdem für die Fixkombination aus retardiertem Oxycodon mit Naloxon (Targin®) eine Wirksamkeit bei vorbehandelten Patienten mit RLS nachgewiesen wurde,[51] erfolgte im Mai 2014 die Zulassung dieses Präparates für das RLS.[52]
Bei dieser Stoffgruppe steht für die Behandlung des RLS weniger die sonst häufig gewünschte analgetische Wirkung im Vordergrund. Vielmehr wird die dopaminerge Komponente dieser Stoffgruppe ausgenutzt, die über eine Aktivierung zentraler μ-Rezeptoren Einfluss auf extrapyramidal-motorische Mechanismen nimmt.[53] Zunehmende Toleranzentwicklung und Ceiling-Effekt stellen hier ein Problem dar, so dass der Einsatz dieser Stoffgruppe solange wie möglich hinausgezögert wird. Eine Therapie mit Methadon kann in Einzelfällen notwendig werden, um bei schwersten RLS-Fällen das therapeutische Ziel der Erhaltung einer minimalen Lebensqualität zu gewährleisten.
Gabe von Eisen
Zu den diskutierten Ursachen des RLS gehört auch eine Störung des Eisenstoffwechsels mit der Folge eines Sauerstoffmangels in der Muskulatur. Sonografische, laborchemische und einzelne neuropathologische Untersuchungen sind auch mit einem verminderten Eisenspeicher im Gehirn von RLS-Patienten vereinbar. Die dortige Eisensättigung steht in engem Zusammenhang mit derjenigen im Blut.[41] Einer der Kenngrößen für das im Blut verfügbare Eisen ist Ferritin. Tatsächlich leiden Patienten mit einem tief-normalen Ferritin (< 50 ng/ml) an einer eher schweren RLS-Symptomatik.[54] Daher werden Laboruntersuchungen mit Bestimmung des Ferritins im Serum durchgeführt, wenn ein RLS diagnostiziert wurde. Pragmatisch wird allgemein ein Richtwert von < 50 µg/l als Grenzwert für eine etwaige Eisengabe benannt. Allerdings ist Ferritin ein akute-Phase-Protein, es steigt also bei Entzündungen an, selbst wenn der Eisenbestand niedrig ist. Daher wird von einigen Autoren die Transferrinsättigung als aussagekräftigerer Parameter für den Eisenbestand vorgeschlagen. Zwar ist grundsätzlich ein deutlich erniedrigter Eisenbestand des Körpers nachteilig und sollte daher korrigiert werden. Bezüglich des RLS allerdings zeigte 2012 eine Meta-Analyse zahlreicher Studien, dass weder die intravenöse noch die orale Gabe von Eisen zu einer signifikanten Verbesserung der RLS-Symptome führt.[55] Das Anstreben des o. a. Ferritin-Richtwerts ist daher laut Leitlinie der Deutschen Gesellschaft für Neurologie[41] keine evidenzbasierte Maßnahme bei RLS.
Ausweichmedikationen
Verschiedene Antikonvulsiva – so etwa Gabapentin (Gabax/Neurontin) oder das vor allem gegenwärtig wieder stark in das Forschungsinteresse gerückte Pregabalin (Lyrica) – haben eine gewisse Wirksamkeit beim RLS gezeigt.[56] In einer 2014 durchgeführten großen Vergleichsstudie war Pregabalin bei RLS ähnlich gut wirksam wie Pramipexol, die Augmentationsrate war damit aber fünffach geringer. Ein limitierender Faktor sind jedoch Nebenwirkungen wie Benommenheit und Somnolenz.[57] Pregabalin gilt außerdem bei bestimmten Patienten als missbrauchs- und abhängigkeitserzeugend.[58]
Als Ausweichmedikamente oder bei bestimmten Indikationen stehen u. a. auch Clonazepam, Carbamazepin, Clonidin und Valproinsäure zur Verfügung. Über die Wirksamkeit von Tetrahydrocannabinol liegen keine Studien vor, doch zeigen zumindest einzelne Patienten bei der Verabreichung von Dronabinol signifikante Verbesserungen der RLS-Symptomatik.[59]
Über die Wirksamkeit von Magnesiumpräparaten wird gestritten. In einer wissenschaftlichen Studie der Universitätsklinik Freiburg konnten keine signifikanten Verbesserungen von Magnesiumpräparaten gegenüber Placebo festgestellt werden, die Autorin der Studie weist aber auf mögliche Schwachpunkte im Studiendesign und dem Bedarf nach weiteren Untersuchungen hin und will deshalb die Wirksamkeit von Magnesiumpräparaten nicht ausschließen.[60]
Nicht-medikamentöse Maßnahmen
RLS-Patienten haben eine gegenüber Kontrollpersonen verminderte Hautdurchblutung. Die Anwendung von Vibrationen auf den gesamten Körper 1 Woche lang täglich etwa 1/4 Stunde führte nicht nur zu einer Normalisierung der Hautdurchblutung, sondern auch zur Verbesserung von RLS-typischen Beschwerden. Eine weitere Woche täglicher Vibrations-Anwendungen führte nicht zu einer zusätzlichen Verbesserung.[61] Dagegen bisher nicht belegt ist, ob und ggf. unter welchen Bedingungen und in welchem Ausmaß Erfahrungen einzelner Patienten auch auf andere Patienten übertragbar sind, wonach weitere nicht-medikamentöse Maßnahmen RLS-Beschwerden lindern wie etwa die Verbesserung der Schlafhygiene, leichter Sport, gymnastizierende Übungen (wie Dehngymnastik), Pilates, Yoga, Taijiquan, Qigong, Massagen, der Verzicht auf Koffein, das Abduschen mit kaltem oder heißen Wasser, Nahrungsaufnahme und ein Bürsten der Füße und Waden mit einer trockenen Wurzelbürste.
Nachteilige oder unwirksame Maßnahmen
Von Nachteil und daher kontraindiziert ist die Einnahme von Schlafmitteln, Antidepressiva, Neuroleptika und Betablockern, da hierunter die neuromuskulären Störungen des RLS zunehmen. RLS-Betroffene berichten über Besserung der Beschwerden, wenn und solange sie sich körperlich bewegen. Dagegen führt körperliche Ruhe, auch die Immobilisation im Rahmen eines Tests,[62] zur Zunahme der Symptome, besonders wenn dies am späten Abend und in der Nacht erfolgt.[63] Psychotherapeutische Maßnahmen können zwar das RLS selbst nicht beseitigen, aber bei der Alltagsbewältigung der Symptome und Folgen des RLS helfen.
Sonstiges
Eine 2006 veröffentlichte Untersuchung zeigte, dass die durch erhöhte Medienpräsenz erzeugte Aufmerksamkeit um das Restless-Legs-Syndrom – vor allem auch im Rahmen der engagierten Vermarktung von Medikamenten – als ein paradigmatisches Beispiel für Disease Mongering gelten kann.[64] Dabei wird nicht grundsätzlich die Existenz oder der individuelle Schweregrad der Erkrankung bei Betroffenen in Frage gestellt, sondern die Folgen der durch die Medien (gegebenenfalls durch Lobbygruppen gezielt lanciert) erzeugten awareness, die wiederum Folgen bei der Wahrscheinlichkeit einer bestimmten Auswahl von Diagnosen und Krankheitswertzuschreibung von Symptomen durch Ärzte und Patienten hat. Obwohl RLS als schwerwiegende Erkrankung auftreten kann, ist die überwiegende Zahl der Betroffenen nicht oder noch nicht dringend behandlungsbedürftig. Die mediale Präsenz der Krankheit und die Bewerbung von Medikamenten führt allerdings zu einem Druck auf Arzt und Patient: Der „informierte Patient“ übt Einfluss auf die Diagnosestellung seines Behandlers aus, Ärzte wiederum sind oftmals in Beziehungen mit Pharmaunternehmen verstrickt, zumal auch sie nicht immun gegen Werbung sind. Nach Ansicht der Autoren können alle diese Faktoren die Wahrscheinlichkeit für die Diagnose „RLS“ und damit für den Beginn einer (möglicherweise zu frühen oder bei unsorgfältiger Diagnose sogar unnötigen) medikamentösen Behandlung auf Kosten von Patient und Gesundheitswesen erhöhen.[65]
Diese Untersuchung basiert jedoch lediglich auf der Auswertung einer Sammlung von Pressemitteilungen und Artikeln. In welchem Maße diese Informationen tatsächlich zu einer verstärkten Diagnose und Behandlung des RLS beitragen und welcher Anteil davon gerechtfertigt (etwa infolge eines tatsächlich beseitigten Informationsdefizits) bzw. wirklich unnötig ist, stellt die Untersuchung nicht dar.
Verwendete Literatur
Klinik
- Lisa Klingelhoefer et al: Restless legs syndrome, in: Clin Med. (London 2016): pg. 379-82. PMID 27481386
- Abeera Mansur et al: Restless Legs Syndrome, StatPearls Publishing. (2021 e-Book) PMID 28613628
- Shiyi Guo et al: Restless Legs Syndrome: From Pathophysiology to Clinical Diagnosis and Management, in: Front Aging Neurosci. 171 (2017) pg. 1-14. PMID 28626420
- Joannes Hallegraeff et al: Criteria in diagnosing nocturnal leg cramps: a systematic review, in: BMC Fam Pract. (2017) Feb 28;18(1):29. PMID 28241802
- Mauro Manconi et al: Restless legs syndrome, in: Nat Rev Dis Primers. 2021 Nov 3;7(1):80. PMID 34732752
Verlauf
- Giuseppe Didato et al: Restless Legs Syndrome across the Lifespan: Symptoms, Pathophysiology, Management and Daily Life Impact of the Different Patterns of Disease Presentation, in: Int J Environ Res Public Health. (2020) May 22;17(10):3658. PMID 32456058
- Pädiatrie
- Pamela Hamilton Stubbs et al: Tools for the Assessment of Pediatric Restless Legs Syndrome, in: Front Psychiatry. (2020) May 5;11:356. PMID 32431628
- Lourdes M DelRosso et al: Restless sleep in children: A systematic review, in: Sleep Med Rev. (2021) Apr;56:101406. PMID 33341437
- Geriatrie
- Prathusha Tatineny et al: Sleep in the Elderly, in: Mo Med. Sep-Oct 2020;117(5):490-495. PMID 33311760
- Keisuke Suzuki et al: Sleep disorders in the elderly: Diagnosis and management, in: J Gen Fam Med. (2017) Mar 30;18(2):61-71. PMID 29263993
Geschlechtsdifferenzen
- Mary V Seeman: Why Are Women Prone to Restless Legs Syndrome?, in: Int J Environ Res Public Health. (2020) Jan 6;17(1):368. PMID 31935805
- Evi Holzknecht et al: Gender differences in clinical, laboratory and polysomnographic features of restless legs syndrome., in: J Sleep Res. 2020 Jun;29(3):e12875. PMID 31162763
Komorbidität
- Claudia Trenkwalder at al: Restless legs syndrome associated with major diseases: A systematic review and new concept, in: Neurology. (2016) Apr 5;86(14):1336-1343. PMID 26944272
RLS und PD
- Luigi Ferini-Strambi et al: Restless Legs Syndrome and Parkinson Disease: A Causal Relationship Between the Two Disorders?, in: Front Neurol. (2018) Jul 24;9:551. PMID 30087647
- Claudia Trenkwalder et al: Comorbidities, treatment, and pathophysiology in restless legs syndrome, in: Lancet Neurol. 2018 Nov;17(11):994-1005. PMID 30244828
- Ambra Stefani et al: Sleep in Parkinson's disease, in: Neuropsychopharmacology. 2020 Jan;45(1):121-128. PMID 31234200
- Lama M Chahine et al: A systematic review of the literature on disorders of sleep and wakefulness in Parkinson's disease from 2005 to 2015., in: Sleep Med Rev. 2017 Oct;35:33-50. PMID 27863901
- Hortensia Alonso-Navarro et al: Association between restless legs syndrome and other movement disorders., in: Neurology. 2019 May 14;92(20):948-964. PMID 31004074
- Jens Carsten Möller et al: Restless Legs Syndrome (RLS) and Parkinson's disease (PD)-related disorders or different entities?, in: J Neurol Sci. 2010 Feb 15;289(1-2):135-7. PMID 19755200
- Birgit Högl und Ambra Stefani: Restless legs syndrome and periodic leg movements in patients with movement disorders: Specific considerations., in: Mov Disord. 2017 May;32(5):669-681. PMID 28186669 (nicht signierter Beitrag von Andreas Werle (Diskussion | Beiträge) 19:45, 12. Dez. 2021 (CET))
Pathophysiologie und Genetik
- Richard P Allen: Restless Leg Syndrome/Willis-Ekbom Disease Pathophysiology, in: Sleep Med Clin. (2015) Sep;10(3):207-14, xi. PMID 26329430
- Barbara Schormair et al: Identification of novel risk loci for restless legs syndrome in genome-wide association studies in individuals of European ancestry: a meta-analysis, in: Lancet Neurol. (2017) Nov;16(11):898-907. PMID 29029846
- Olivia J Veatch et al: Pleiotropic genetic effects influencing sleep and neurological disorders, in: Lancet Neurol. 2017 Feb;16(2):158-170. PMID 28102151
- Faezeh Sarayloo et al: MEIS1 and Restless Legs Syndrome: A Comprehensive Review, in: Front Neurol. (2019) Aug 28;10:935. PMID 31551905
- Valerio Brunetti et al: Sleep Disorders in Mitochondrial Diseases, in: Curr Neurol Neurosci Rep. 2021 May 5;21(7):30. PMID 33948737
- Claudia Trenkwalder at al: Restless legs syndrome: pathophysiology, clinical presentation and management, in: Nat Rev Neurol. 2010 Jun;6(6):337-46. PMID 20531433
Behandlung
- Qing Lv et al: Pharmacologic Treatment of Restless Legs Syndrome, in: Curr Neuropharmacol. (2021);19(3):372-382. PMID 33380302
- Claudia Trenkwalder et al: Restless legs syndrome-current therapies and management of augmentation, in: Nat Rev Neurol. 2015 Aug;11(8):434-45. PMID 26215616
Einzelnachweise
- LL 06 2012 Restless-Legs-Syndrom (RLS) und Periodic Limb Movement Disorder (PLMD) - Deutsche Gesellschaft für Neurologie e. V. In: Deutsche Gesellschaft für Neurologie e. V. Abgerufen am 15. Januar 2022 (deutsch).
- ICD-10-GM-2022 G25.- Sonstige extrapyramidale Krankheiten und Bewegungsstörungen - ICD10. Abgerufen am 15. Januar 2022.
- Willis, T: The London Practice of Physick, Basset & Cooke 1685. (Zit nach Manconi Nat Rev Dis Primers. 2021)
- Karl-Axel Ekbom: Restless legs: A clinical study., in: Acta medica Scandinavica. Suppl. 158, 1-124, 1945. (Zit nach Manconi Nat Rev Dis Primers. 2021)
- Ulrich Moser, Jasmin Schwab: Restless arm syndrome: a rare disease? In: BMJ Case Reports CP. Band 14, Nr. 9, 1. September 2021, ISSN 1757-790X, S. e244890, doi:10.1136/bcr-2021-244890, PMID 34544716 (bmj.com [abgerufen am 15. Januar 2022]).
- RLS Allgemein | RLS e. V. - Deutsche Restless Legs Vereinigung. Abgerufen am 15. Januar 2022 (deutsch).
- J. Winkelmann, T.-C. Wetter, C. Trenkwalder: Das Restless-legs-Syndrom (RLS). In: Chronisches Müdigkeits- und Fibromyalgiesyndrom. Springer Berlin Heidelberg, Berlin, Heidelberg 1999, ISBN 978-3-540-65093-5, S. 96–109, doi:10.1007/978-3-662-00574-3_7 (springer.com [abgerufen am 15. Januar 2022]).
- Roland Depner: Alles Nervensache? Wie unser Nervensystem funktioniert - oder auch nicht. Stuttgart 2012, ISBN 978-3-7945-2887-5, S. 115.
- APA PsycNet. Abgerufen am 15. Januar 2022 (englisch).
- Sport mit RLS | RLS e. V. - Deutsche Restless Legs Vereinigung. Abgerufen am 15. Januar 2022 (deutsch).
- NDR: Chat-Protokoll: Restless Legs Syndrom. Abgerufen am 15. Januar 2022.
- RLS|Restless-Legs|Beratung - Dr. Goesmann. Abgerufen am 15. Januar 2022.
- Mauro Manconi, Diego Garcia-Borreguero, Barbara Schormair, Aleksandar Videnovic, Klaus Berger: Restless legs syndrome. In: Nature Reviews Disease Primers. Band 7, Nr. 1, Dezember 2021, ISSN 2056-676X, S. 80, doi:10.1038/s41572-021-00311-z (nature.com [abgerufen am 15. Januar 2022]).
- Richard P. Allen, Daniel L. Picchietti, Diego Garcia-Borreguero, William G. Ondo, Arthur S. Walters: Restless legs syndrome/Willis–Ekbom disease diagnostic criteria: updated International Restless Legs Syndrome Study Group (IRLSSG) consensus criteria – history, rationale, description, and significance. In: Sleep Medicine. Band 15, Nr. 8, August 2014, S. 860–873, doi:10.1016/j.sleep.2014.03.025 (elsevier.com [abgerufen am 15. Januar 2022]).
- Hans-Günter Weeß: Die schlafmedizinische Untersuchung im Schlaflabor. In: PiD - Psychotherapie im Dialog. Band 10, Nr. 02, Juni 2009, ISSN 1438-7026, S. 150–156, doi:10.1055/s-0029-1223315 (thieme-connect.de [abgerufen am 15. Januar 2022]).
- LL 06 2012 Restless-Legs-Syndrom (RLS) und Periodic Limb Movement Disorder (PLMD) - Deutsche Gesellschaft für Neurologie e. V. In: Deutsche Gesellschaft für Neurologie e. V. Abgerufen am 2. März 2022 (deutsch).
- Paulo Daubian-Nosé, Miriam K.Frank, Andrea Maculano Esteves: Sleep disorders: A review of the interface between restless legs syndrome and iron metabolism. In: Sleep Sci. 7(4), Dez 2014, S. 234–237, doi:10.1016/j.slsci.2014.10.002, PMC 4608891 (freier Volltext)
- F. Hohl-Radke, F. Aedtner, U. Domröse, K. H. Neumann, J. Staedt: Restless-Legs-Syndrom bei dialysepflichtiger Niereninsuffizienz: Einfluss der Medikation. In: Deutsche Medizinische Wochenschrift. 133, 3, 2008, S. 71–75.
- Romana Stehlik, Lennart Arvidsson, Jan Ulfberg: Restless Legs Syndrome Is Common among Female Patients with Fibromyalgia. In: European Neurology. Band 61, Nr. 2, 2009, ISSN 0014-3022, S. 107–111, doi:10.1159/000180313 (karger.com [abgerufen am 2. März 2022]).
- Torsten Gallwitz: Restless-Legs-Syndrom als Nebenwirkung bei „modernen“ Antidepressiva. (PDF; 299 kB) Dissertation. München 2007.
- José Carlos Pereira Júnior, João Luiz Pereira da Silva Neto, Márcia Pradella-Hallinan: Restless legs syndrome in subjects with a knee prosthesis: evidence that symptoms are generated in the periphery. In: Clinics. 66, 2011, S. 1955, doi:10.1590/S1807-59322011001100017.
- Raja Mehanna, Joseph Jankovic: Restless legs syndrome and cerebrovascular disease – Authors’ reply. In: The Lancet. 3. März 2014, doi:10.1016/S1474-4422(13)70126-1, thelancet.com (PDF; 56 kB).
- Richard P Allen, Christopher J Earley: Defining the phenotype of the restless legs syndrome (RLS) using age-of-symptom-onset. In: Sleep Medicine. Band 1, Nr. 1, 1. Februar 2000, ISSN 1389-9457, S. 11–19, doi:10.1016/S1389-9457(99)00012-X (sciencedirect.com [abgerufen am 2. März 2022]).
- S. Whittom, Y. Dauvilliers, M.-H. Pennestri, F. Vercauteren, N. Molinari: Age-at-onset in restless legs syndrome: A clinical and polysomnographic study. In: Sleep Medicine. Band 9, Nr. 1, Dezember 2007, S. 54–59, doi:10.1016/j.sleep.2007.01.017 (elsevier.com [abgerufen am 2. März 2022]).
- Giuseppe Didato et al: Restless Legs Syndrome across the Lifespan: Symptoms, Pathophysiology, Management and Daily Life Impact of the Different Patterns of Disease Presentation, in: Int J Environ Res Public Health. (2020) May 22;17(10):3658. (pg. 2) PMID 32456058.
- Olivia J Veatch et al: Pleiotropic genetic effects influencing sleep and neurological disorders, in: Lancet Neurol. 2017 Feb;16(2):158-170. PMID 28102151
- Valerio Brunetti et al: Sleep Disorders in Mitochondrial Diseases, in: Curr Neurol Neurosci Rep. 2021 May 5;21(7):30. PMID 33948737
- Luigi Ferini-Strambi et al: Restless Legs Syndrome and Parkinson Disease: A Causal Relationship Between the Two Disorders?, in: Front Neurol. (2018) Jul 24;9:551. PMID 30087647
- Claudia Trenkwalder et al: Comorbidities, treatment, and pathophysiology in restless legs syndrome, in: Lancet Neurol. 2018 Nov;17(11):994-1005. (Abschnitt Pathophysiology pg. 6) PMID 30244828
- Valerio Brunetti et al: Sleep Disorders in Mitochondrial Diseases., in: Curr Neurol Neurosci Rep. 2021 May 5;21(7):30. PMID 33948737.
- Olivia J Veatch et al: Pleiotropic genetic effects influencing sleep and neurological disorders., in: Lancet Neurol. 2017 Feb;16(2):158-170. (pg. 10) PMID 28102151.
- Hyatt Moore et al.: Periodic Leg Movements during Sleep Are Associated with Polymorphisms in BTBD9, TOX3/BC034767, MEIS1, MAP2K5/SKOR1, and PTPRD., in: Sleep. 2014 Sep 1; 37(9): 1535–1542. PMID 25142570.
- D Kemlink et al: Replication of restless legs syndrome loci in three European populations., in: J Med Genet. 2009 May; 46(5): 315–318. PMID 19279021.
- Eva C. Schulte und Juliane Winkelmann: Clinical Phenotype and Genetics of Restless Legs Syndrome, in: Movement Disorders (Second Edition), 2015.
- Olivia J Veatch et al: Pleiotropic genetic effects influencing sleep and neurological disorders., in: Lancet Neurol. 2017 Feb;16(2):158-170. (pg. 11) PMID 28102151.
- Luigi Ferini-Strambi et al: Restless Legs Syndrome and Parkinson Disease: A Causal Relationship Between the Two Disorders?, in: Front Neurol. (2018) Jul 24;9:551. PMID 30087647.
- Birgit Högl und Ambra Stefani: Restless legs syndrome and periodic leg movements in patients with movement disorders: Specific considerations., in: Mov Disord. 2017 May;32(5):669-681. PMID 28186669
- Ambra Stefani et al: Sleep in Parkinson's disease, in: Neuropsychopharmacology. 2020 Jan;45(1):121-128. PMID 31234200
- Claudia Trenkwalder et al: Comorbidities, treatment, and pathophysiology in restless legs syndrome, in: Lancet Neurol. 2018 Nov;17(11):994-1005. (pg. 1339) PMID 30244828
- Ambra Stefani et al: Sleep in Parkinson's disease, in: Neuropsychopharmacology. 2020 Jan;45(1):121-128. (pg. 123) PMID 31234200
- S1-Leitlinie Restless-Legs-Syndrom (RLS) und Periodic Limb Movement Disorder (PLMD) der Deutschen Gesellschaft für Neurologie (DGN). In: AWMF online (Stand 2012), dgn.org (PDF; 1,7 MB).
- Mauro Manconi, Diego Garcia-Borreguero, Barbara Schormair, Aleksandar Videnovic, Klaus Berger: Restless legs syndrome. In: Nature Reviews Disease Primers. Band 7, Nr. 1, Dezember 2021, ISSN 2056-676X, S. 80, doi:10.1038/s41572-021-00311-z (nature.com [abgerufen am 5. Dezember 2021]).
- Augmentation – Eine Erfahrung aus klinischer Forschung und Arzneimittelstudien. Deutsche RLS-Vereinigung.
- Mark Buchfuhrer: Allaying Augmentation. 2015.
- L. Ferini-Strambi u. a.: Effect of pramipexole on RLS symptoms and sleep: A randomized, double-blind, placebo-controlled trial. In: Sleep Med. 2008 Oct 24. J. Montplaisir u. a.: Ropinirole is effective in the long-term management of restless legs syndrome: a randomized controlled trial. In: Mov Disord. 21 (10), Okt 2006, S. 1627–1635.
- C. Trenkwalder u. a.; SP790 Study Group: Efficacy of rotigotine for treatment of moderate-to-severe restless legs syndrome: a randomised, double-blind, placebo-controlled trial. 2008.
- C. M. Baldwin, G. M. Keating: Rotigotine transdermal patch: in restless legs syndrome. In: CNS Drugs. 22(10), 2008, S. 797–806.
- Annett Deißler: Lisurid in der Therapie des Restless Legs Syndroms. Dissertation. Univ. Rostock, 2012. PPN 687954282.
- A. Walters u. a.: Langzeittherapie des Restless Legs Syndroms mit Opiaten (Memento vom 29. April 2005 im Internet Archive). In: Movement Disorders. 16, 2001, S. 1105–1109.
- Kathrin Helmschmied: Untersuchung des extrastriatalen dopaminergen Systems mit dem niedrigdosierten Apomorphintest von Patienten mit idiopathischem Parkinson-Syndrom und Restless Legs Syndrom. Dissertation. Göttingen 2006.
- Claudia Trenkwalder, Heike Beneš, Ludger Grote, Diego García-Borreguero, Birgit Högl, Michael Hopp, Björn Bosse, Alexander Oksche, Karen Reimer, Juliane Winkelmann, Richard P Allen, Ralf Kohnen: Prolonged release oxycodone–naloxone for treatment of severe restless legs syndrome after failure of previous treatment: a double-blind, randomised, placebo-controlled trial with an open-label extension. In: The Lancet Neurology. 12, 2013, S. 1141–1150, doi:10.1016/S1474-4422(13)70239-4.
- Beate Fessler: Oxycodon/Naloxon gegen Restless Legs. In: Deutsche Apotheker Zeitung. 20. Juni 2014.
- Sarah von Spiczak Brzezinski: The role of opioids in restless legs syndrome: an 11C-diprenorphine positron emission tomography study. Dissertation. Göttingen 2006.
- E. R. Sun, C. A. Chen, G. Ho, C. J. Earley, R. P. Allen: Iron and the restless legs syndrome. In: Sleep. 21, 1998, S. 371–377. PMID 9646381.
- Lynn M Trotti, Srinivas Bhadriraju, Lorne A Becker: Iron for restless legs syndrome. PMC 4070449 (freier Volltext)
- R. Allen, C. Chen, A. Soaita, C. Wohlberg, L. Knapp, B. T. Peterson, D. García-Borreguero, J. Miceli: A randomized, double-blind, 6-week, dose-ranging study of pregabalin in patients with restless legs syndrome. In: Sleep Med. 11(6), Jun 2010, S. 512–519.
- Thomas Müller: Große Vergleichsstudie – RLS-Therapie ohne Augmentation.
- Warnung wegen des hohen Missbrauchs-, Sucht- und Abhängigkeitspotentials von Pregabalin bei bestimmten Patienten (Memento vom 10. Juni 2016 im Internet Archive) Landesärztekammer Baden-Württemberg.
- Mark J. Buchfuhrer, Wayne A. Hening, Clete Anthony Kushida, Ann. E. Battenfield, Karla M. Dzienkowski: Restless Legs Syndrome: Coping with Your Sleepless Nights. American Academy of Neurology. Demos Medical Publishing, LLC, 2006, S. 98f. (eingeschränkte Vorschau in der Google-Buchsuche).
- Beate Mendelski: Wirksamkeit von Magnesium in der Behandlung des idiopathischen Restless Legs Syndroms.
- Ulrike H. Mitchell, Sterling C. Hilton, Erik Hunsaker, Jan Ulfberg: Decreased Symptoms without Augmented Skin Blood Flow in Subjects with RLS/WED after Vibration Treatment. In: J Clin Sleep Med. 12(7), 2016, S. 947–952.
- Diego Garcia-Borreguero, Ralf Kohnen, Lindsay Boothby, Desislava Tzonova, Oscar Larrosa, Elmar Dunkl: Validation of the Multiple Suggested Immobilization Test: A Test for the Assessment of Severity of Restless Legs Syndrome (Willis-Ekbom Disease). In: Sleep. Band 36, Heft 7, 1. Juli 2013, S. 1101–1109.
- M. Michaud u. a.: Circadian variation of the effects of immobility on symptoms of restless legs syndrome. In: Sleep. 28, 2005, S. 843–846. PMID 16124663.
- S. Woloshin, L. M. Schwartz: Giving legs to restless legs: a case study of how the media helps make people sick. In: PLoS Med. 3, 2006, S. e170–e170. PMID 16597175 PMC 1434499 (freier Volltext) (Review).
- James W. Dear, David J. Webb: Disease mongering – a challenge for everyone involved in healthcare. In: British Journal of Clinical Pharmacology. 64, 2007, S. 122–124, doi:10.1111/j.1365-2125.2006.02830.x. PMC 2000629 (freier Volltext).