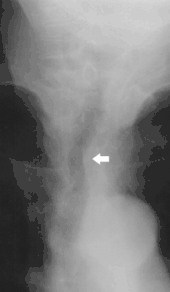
Hyperthyreose
Die Hyperthyreose ist eine krankhafte Überfunktion der Schilddrüse (Schilddrüsenüberfunktion), die sich in einer übermäßigen Produktion von Schilddrüsenhormonen äußert, sodass im Organismus ein entsprechendes Überangebot entsteht. Infolgedessen kann es zu einer Vielzahl von Krankheitserscheinungen wie starker Schweißproduktion, beschleunigtem Herzschlag und anderen Herzrhythmusstörungen, Gewichtsverlust, dauerndem Hungergefühl, Nervosität, rascher Ermüdung und Zittern kommen. Die häufigsten Ursachen der Hyperthyreose sind der Morbus Basedow (eine Autoimmunerkrankung der Schilddrüse) und die Schilddrüsenautonomie, die beide mit einer erhöhten Sekretionsleistung der Schilddrüse, möglicherweise auch mit einer Kropfbildung, einhergehen, und eine erhöhte Zufuhr von Schilddrüsenhormonen in Form von Medikamenten (Hyperthyreosis factitia oder Thyreotoxicosis factitia).[1] Im Extremfall einer krisenhaften lebensbedrohlichen Überfunktion spricht man von einer thyreotoxischen Krise (Synonym Thyreotoxikose, „Schilddrüsenhormonvergiftung“). Das Gegenteil der Hyperthyreose, ein Mangel an Schilddrüsenhormonen, wird als Hypothyreose (Schilddrüsenunterfunktion) bezeichnet. Die Gesamtheit der typischen Symptome einer Hyperthyreose wird als Hyperthyreoidismus bezeichnet.
Geschichte

Die Hyperthyreose wurde erstmals 1786 von Caleb Hillier Parry beschrieben.[2][3][4] Wie auch andere Ärzte seiner Zeit, beispielsweise Carl von Basedow[5][6] und Robert James Graves,[7] stellte er jedoch keinen Zusammenhang der Symptome mit einer Erkrankung der Schilddrüse her. Erst 1886 wies Paul Julius Möbius diesen Bezug nach.[8] Den Chirurgen Paul Jules Tillaux (1880)[9] und L. Rehn (1884)[10] gelang es dementsprechend durch operative Entfernung von Teilen der Schilddrüsen (Thyreoidektomie) und damit der Verringerung sekretbildenden Gewebes die Krankheit zu heilen.[11]
Zur Behandlung der Schilddrüsenüberfunktion wurde Anfang des 20. Jahrhunderts Röntgenstrahlung verwendet oder die Schilddrüse mit Radium gespickt, das heißt, kleine Stäbchen aus Radium wurden direkt in die Schilddrüse eingebracht.[12] 1942 wendeten Saul Hertz und Arthur Roberts erstmals die Radiojodtherapie beim Morbus Basedow an[13][14][15] und 1943 beschrieb Edwin Bennett Astwood den Einsatz der Substanz 2-Thiouracil zur Behandlung der Hyperthyreose:[8] das erste Thyreostatikum.
In den 1980er-Jahren wurde in den USA eine spezielle Form der alimentären Thyreotoxikose beobachtet, die unter der Bezeichnung hamburger thyrotoxicosis[16] bekannt geworden ist. Diese Erkrankung kann bei Hunden[17][18] und Menschen durch den Konsum von mit Schilddrüsenhormonen kontaminiertem Hackfleisch oder durch Wurst verursacht werden.
Grundlagen
Beim gesunden Menschen gibt die Schilddrüse bedarfsgerecht die Schilddrüsenhormone – Thyroxin (T4) und Trijodthyronin (T3) – ins Blut ab. Die Produktion dieser Hormone wird durch den thyreotropen Regelkreis gesteuert. In der Schilddrüse bewirkt das in der Hirnanhangsdrüse (Hypophyse) gebildete Hormon Thyreotropin (TSH) eine gesteigerte Produktion der Schilddrüsenhormone und übt zusätzlich einen Wachstumsreiz auf das Schilddrüsengewebe aus.
Zum Aufbau von Thyroxin und Trijodthyronin benötigt die Schilddrüse Jod. Der Jodbedarf des Erwachsenen liegt bei etwa 200 μg pro Tag. Eine ausreichende Jodzufuhr ist durch jodiertes Speisesalz in Deutschland im Allgemeinen gewährleistet. Die Jodversorgung der Bevölkerung Deutschlands wurde 2004 von der Weltgesundheitsorganisation (WHO) aufgrund der durchschnittlichen Jodausscheidung im Urin als „optimal“ bezeichnet.[19] Die Menge der produzierten Hormone schwankt innerhalb der Gruppe schilddrüsengesunder Personen (Normalpopulation) erheblich, das heißt, dass der Referenzbereich der laborchemischen Ergebnisse relativ groß ist. Die Schwankungen bei Messungen bei derselben Person sind wesentlich geringer.[20] Die aus der Schilddrüse ins Blut abgegebenen Schilddrüsenhormone (T3 und T4) werden dort größtenteils an unterschiedliche Proteine (hauptsächlich TBG, TBPA und Albumin) gebunden und dabei biologisch inaktiv. Nur etwa 1 ‰ der im Blut befindlichen Schilddrüsenhormone zirkuliert frei (fT3 und fT4). Die Schilddrüsenhormone steigern den Grundumsatz, die Empfindlichkeit des Herzens für Katecholamine, den Calcium- und den Phosphatumsatz sowie die Erregbarkeit von Muskel- und Nervenzellen und hemmen die Protein- und die Glykogenneubildung.
Einteilung
| Klassifikation nach ICD-10 | |
|---|---|
| E05.0 | Hyperthyreose mit diffuser Struma – Morbus Basedow |
| E05.1 | Hyperthyreose mit toxischem solitärem Schilddrüsenknoten |
| E05.2 | Hyperthyreose mit toxischer mehrknotiger Struma |
| E05.3 | Hyperthyreose durch ektopisches Schilddrüsengewebe |
| E05.4 | Hyperthyreosis factitia |
| E05.5 | Thyreotoxische Krise |
| E05.8 | Sonstige Hyperthyreose |
| E05.9 | Hyperthyreose, nicht näher bezeichnet |
| ICD-10 online (WHO-Version 2019) | |
Die Schilddrüsenüberfunktion kann nach Ursache und Schweregrad eingeteilt werden.
- Ursache sind häufig Verselbständigungs- (Autonomie-) und Autoimmunprozesse und selten auch entzündliche Erkrankungen, Überdosierung von Schilddrüsenhormonen (iatrogen) oder bösartige Tumoren der Schilddrüse. Sehr selten tritt sie als Begleiterscheinung anderer bösartiger Tumoren (Paraneoplasie) oder bei einer Hypophysenüberfunktion (TSH-Mehrproduktion) auf.
- Folgende Schweregrade werden unterschieden: die sogenannte latente beziehungsweise kompensierte Hyperthyreose (Schilddrüsenhormonspiegel normal, aber TSH-Wert vermindert), die subklinische Hyperthyreose (Schilddrüsenhormonspiegel erhöht, Patient aber symptomlos), die manifeste Hyperthyreose und die thyreotoxische Krise (syn. Thyreotoxikose[21] – krisenhafte Verschlimmerung einer Schilddrüsenüberfunktion, die aufgrund ihrer Symptome akut lebensbedrohlich ist).
Entstehung

Die Schilddrüsenautonomie, bei welcher der Einfluss des normalerweise regulierenden TSH auf die Hormonausschüttung in Teilen der Schilddrüse fehlt, ist besonders im höheren Lebensalter eine häufige Ursache der Hyperthyreose. Auch in einer „gesunden“ Schilddrüse sind bestimmte Bereiche autonom, arbeiten also unabhängig von den physiologischen Regulationsmechanismen. Bei einer Schilddrüsenvergrößerung durch Jodmangel (Jodmangelstruma) kann aber der autonome Schilddrüsenanteil relativ groß werden. Einer Hyperthyreose durch Schilddrüsenautonomie liegen dann zwei Faktoren zu Grunde: die Entwicklung eines großen autonomen Gewebeanteils (oft über Jahre) und dann eine plötzliche hohe Jodzufuhr (jodhaltige Kontrastmittel oder Medikamente, insbesondere Amiodaron).[22] Bei der Schilddrüsenautonomie unterscheidet man nach der Darstellung im Schilddrüsenszintigramm die unifokale (autonomes Adenom), die multifokale und die disseminierte Autonomie.
Eine Hyperthyreose kann auch Folge einer Autoimmunerkrankung sein. Die immunogene Hyperthyreose (zum Beispiel Morbus Basedow) tritt meist erst nach dem 35. Lebensjahr bevorzugt bei Frauen auf.[23] Die Schilddrüsenüberfunktion kann dabei sowohl ohne Struma (Kropf) als auch mit diffuser Struma oder Knotenstruma vorkommen. Familiär gehäuft (HLA-B8 und HLA-DR3) verursachen dabei TSH-Rezeptorautoantikörper eine Stimulation der Hormonproduktion. Zu den immunogenen Hyperthyreosen wird auch die Hashimoto-Thyreoiditis gerechnet, bei der es vorübergehend zu einer vermehrten Hormonausschüttung kommen kann.
Eine Hyperthyreose durch die Kombination aus autoimmunogener Schilddrüsenerkrankung und Autonomie der Schilddrüse wird als Marine-Lenhart-Syndrom bezeichnet.
Des Weiteren können eine Überdosierung von Schilddrüsenhormonen (Hyperthyreosis factitia), hormonproduzierende Tumoren von Schilddrüse (Schilddrüsenhormone) und Hypophyse (TSH), aber auch Entzündungen der Schilddrüse unterschiedlicher Ursache, Auslöser einer Schilddrüsenüberfunktion sein.[24] In den Holy Seven beschreibt Franz Alexander die Hyperthyreose als psychosomatische Krankheit. Der Schweregrad einer Hyperthyreose ist unabhängig von der Ursache.
Thyreotoxische Krise
Eine krisenhafte, lebensbedrohliche Verschlimmerung einer Schilddrüsenüberfunktion (thyreotoxische Krise) ist unabhängig von der Ursache bei jeder Form einer Hyperthyreose möglich; sie kann sich unerwartet und rasch innerhalb weniger Stunden oder Tage entwickeln. Als Auslöser werden größere Mengen von Jod, die vom Körper des Betroffenen ein bis vier Wochen zuvor – selten auch weiter zurückliegend – aufgenommen wurden (oft iatrogen durch Verabreichung jodhaltiger Medikamente, beispielsweise Amiodaron, oder Röntgenkontrastmittel), das Absetzen von Thyreostatika, Operationen (insbesondere die nicht in Euthyreose durchgeführte Strumaresektion), aber auch andere Begleiterkrankungen angesehen.[24] Eine thyreotoxische Krise erfordert in der Regel eine sofortige intensivmedizinische Behandlung.[25]
Klinisches Bild
Die Gesamtheit der typischen Symptome einer Hyperthyreose wird auch als Hyperthyreoidismus bezeichnet. Etwa vier von fünf betroffenen Patienten weisen eine Struma auf. Ist die Struma stark durchblutet, kann mit dem Stethoskop ein schwirrendes Geräusch abgehört werden. Typisch sind auch Schlaflosigkeit, Gereiztheit, Nervosität und Zittern (feinschlägiger Tremor) als Zeichen einer allgemeinen psychomotorischen Unruhe. Das Herz-Kreislauf-System weist neben einer gesteigerten Blutdruckamplitude (Differenz zwischen systolischem und diastolischem Messwert) eine veränderte Herztätigkeit (Sinustachykardie, Extrasystolen, Vorhofflimmern) auf. Trotz Heißhungers kann es durch die Steigerung des Grundumsatzes zu Gewichtsverlust kommen. Begleitend ist eine pathologische Glukosetoleranz, evtl. sogar eine Hyperglykämie infolge der Mobilisierung von Fett- und Glykogenreserven möglich. Zudem sind Hitzesymptome (Wärmeintoleranz, Schweißausbrüche, warme feuchte Haut, eventuell leichtes Fieber), eine gesteigerte Stuhlfrequenz, Schwäche der Muskulatur, Osteoporose (negative Calciumbilanz), Fettleber, Haarausfall und Zyklusstörungen bis hin zu vorübergehender Unfruchtbarkeit typisch.[24]
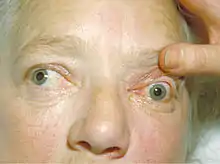
Bei immunogener Hyperthyreose vom Typ Basedow ist das auffällige Hervortreten der Augäpfel aus der Augenhöhle (Exophthalmus) das wohl bekannteste Symptom (endokrine Orbitopathie). Die Kombination aus Exophthalmus, Struma und Tachykardie wird als Merseburger Trias bezeichnet. Ursächlich für die Orbitopathie ist eine Einlagerung von Glukosaminoglykanen in das Bindegewebe der Augenhöhle. Durch den gleichen Mechanismus können sich an den Extremitäten Myxödeme entwickeln. Selten kann auch eine Akropachie (Hautveränderungen der Finger und Zehen)[26] auftreten.
Die dargestellten Symptome sind zwar typisch, bei der Mehrzahl der Patienten, insbesondere bei älteren Betroffenen, tritt aber nur jeweils ein Teil der Krankheitserscheinungen auf.
Die krisenhafte, lebensbedrohliche Verschlimmerung einer Schilddrüsenüberfunktion (thyreotoxische Krise) wird klinisch in drei Stadien (nach Herrmann) eingeteilt:[24][27]
| Stadium | Klinik | Letalität |
|---|---|---|
| Stadium I | Tachykardie > 150/min, Herzrhythmusstörungen, Hyperthermie (>41 °C), Adynamie, schwere Durchfälle, Dehydratation, verstärkter Tremor, Unruhe, Agitiertheit, Hyperkinese, eventuell stark erhöhte Schilddrüsenhormone in etwa 60 % der Fälle zusätzlich Zeichen einer Myopathie (Schwäche der proximalen Muskulatur und des Schultergürtels oder Bulbärparalyse) |
unter 10 % |
| Stadium II | zusätzlich Bewusstseinsstörungen, Stupor, Somnolenz, psychotische Zeichen, örtliche und zeitliche Desorientierung | |
| Stadium III IIIa: Patient < 50 Jahre IIIb: Patient > 50 Jahre |
zusätzlich Koma | über 30 % |
Diagnose
Hauptartikel: Untersuchung der Schilddrüse
.jpg.webp)
Da die Hyperthyreose durch ein Übermaß an Schilddrüsenhormonen definiert ist, spielt neben Anamnese, klinischen Symptomen und bildgebenden Verfahren (insbesondere Sonographie und Szintigraphie) die Labordiagnostik die entscheidende Rolle. Da die klinischen Symptome jedoch andererseits nicht immer mit nachweislichen Laborveränderungen korrelieren, können zum einen auch beschwerdefreie Patienten pathologisch veränderte Messwerte aufweisen und zum anderen bereits bei moderaten Veränderungen lebensbedrohliche Zustände auftreten; deshalb wurde, um die Wahrscheinlichkeit, dass eine thyreotoxische Krise vorliegt, laborwertunabhängig einschätzen zu können, der Burch-Wartofsky-Score[28] entwickelt.
In der Regel produziert die Schilddrüse bei der Hyperthyreose zu viele Schilddrüsenhormone. Der Organismus versucht über den thyreotropen Regelkreis die Produktion durch eine Minimierung der TSH-Ausschüttung zu reduzieren. Als Screening-Parameter eignet sich daher die alleinige Bestimmung des basalen TSH-Spiegels im Blut. Ist dieser normal, kann bei klinisch unauffälligen Patienten auf eine weitere Bestimmung der Schilddrüsenhormone verzichtet werden.[29]
Letztendlich beweisend für eine manifeste Hyperthyreose ist eine Erhöhung des freien Trijodthyronin (fT3) oder des Thyroxin (fT4) zusammen mit einer Erniedrigung des TSH-Spiegels und den entsprechenden klinischen Symptomen. Bei der Interpretation der Laborergebnisse ist zu beachten, dass es isolierte T3-Hyperthyreosen ohne erhöhtes fT4 gibt, bei extremem Jodmangel der TSH-Spiegel normal, aber das fT3 erhöht und fT4 erniedrigt, sowie bei einer latenten oder kompensierten Hyperthyreose trotz normaler fT3- und fT4-Spiegel der basale TSH-Spiegel erniedrigt sein kann.
Zur Differenzierung des Krankheitsbildes stehen weitere Laborparameter zur Verfügung. Thyreotropin-Rezeptor-Autoantikörper (TRAK) zeigen mit hoher Spezifität, ob es sich um eine immunogene Hyperthyreose (Morbus Basedow) handelt. Wird als Ursache eine vermehrte Jodbelastung vermutet, so kann der Jodgehalt des Urins bestimmt werden. Eine Erhöhung von fT3 und fT4 ohne Erniedrigung des basalen TSH-Spiegels findet sich typischerweise bei einer sogenannten „zentralen Hyperthyreose“ (zum Beispiel durch ein TSH-produzierendes Hypophysenadenom bedingt).[24][27][29][30][31] Diese Untersuchungsmöglichkeiten werden auch bei der „thyreotoxischen Krise“ eingesetzt, andere spielen nur in speziellen Fällen eine Rolle und werden im jeweiligen Hauptartikel dargestellt.
Therapie
Die Behandlung hängt von der Ursache der Hyperthyreose ab. Eine kausale Behandlung ist nicht bekannt.[24] Grundsätzlich unterscheidet man die medikamentöse, die operative und die Radiojodtherapie.
Medikamente
Bei der medikamentösen Therapie werden den Betroffenen Thyreostatika, die die Bildung der Schilddrüsenhormone hemmen, solange und so hoch dosiert verschrieben, bis eine Normalisierung der Laborwerte (Euthyreose) erreicht wird. Häufig werden schwefelhaltige Thyreostatika (Propylthiouracil, Carbimazol, Thiamazol und andere) eingesetzt, die jedoch eine etwa einwöchige Wirklatenz aufweisen; ist ein schneller Wirkeintritt nötig, so kann Natriumperchlorat, das die Aufnahme von Jod in die Schilddrüse hemmt, eingesetzt werden. Thyreostatika sind bei einer Hyperthyreose, die durch eine Schilddrüsenentzündung (Thyreoiditis) ausgelöst wird, unwirksam, da sie die Freisetzung der in der Schilddrüse gespeicherten Hormone („präformierte Hormone“) durch den Entzündungsprozess nicht beeinflussen können. Propranolol (ein nichtkardioselektiver β-Rezeptorenblocker) wird bei Tachykardie ergänzend eingesetzt, mildert aber auch die nichtkardialen Symptome der Hyperthyreose und hemmt die Umwandlung (Konversion) von T4 zu T3.
Pflanzenheilkunde
Im Bereich der Rationalen Phytotherapie kann bei einer leichten Überfunktion der Schilddrüse möglicherweise auch eine Behandlung mit einem Extrakt aus dem Wolfstrappkraut (Lycopi herba) in Betracht gezogen werden.[32]
Operation
Die operative Therapie hat das Ziel, das Wiederauftreten einer Hyperthyreose dauerhaft zu verhindern. Voraussetzung ist eine vorangehende, erfolgreiche medikamentöse Normalisierung der Laborwerte. Die Thyreoidektomie (vollständige Entfernung der Schilddrüse) ist bei einem Karzinom die Therapie der Wahl. Findet sich eine gutartige Vergrößerung der Schilddrüse, so kommt die subtotale Strumaresektion zum Einsatz; das postoperativ verbleibende Restvolumen richtet sich nach der Ursache, die der Hyperthyreose zugrunde liegt. Nach der Operation ist in der Regel zur Prophylaxe eines Rezidivs eine Hormontherapie mit oraler Jodzufuhr (Suppressionstherapie) oder (nach Thyreoidektomie) eine Hormonersatztherapie (Substitutionstherapie) zur Vermeidung einer Hypothyreose erforderlich.
Radiojodtherapie
Die Radiojodtherapie bietet sich in vielen Fällen als Alternative zur Operation nach einer erfolgreichen medikamentösen Normalisierung der Laborwerte an. Aufgrund des möglichen Übertritts des Radiopharmakons in den kindlichen Organismus ist sie für schwangere und stillende Patientinnen kontraindiziert.
Sonderfall der thyreotoxischen Krise
Bei der thyreotoxischen Krise handelt es sich um ein akut lebensbedrohliches, notfallmedizinisches Krankheitsbild. Ihre Inzidenz beträgt in Deutschland etwa 100 bis 1100 Fälle pro Jahr[33][34], die Letalität liegt unerkannt bei 90 %[35] und trotz intensivmedizinischer Behandlung noch über 20 %. Daher beginnt die Therapie unverzüglich mit einer symptombezogenen Stabilisierung der Lebensfunktionen, ohne das Ergebnis laborchemischer Hormonanalysen abzuwarten.[24]
Patienten mit den klinischen Zeichen einer thyreotoxischen Krise sollen sofort auf einer Intensivstation aufgenommen und behandelt werden. Die Therapie umfasst allgemein Bilanzierung und Ersatz von Flüssigkeit, Elektrolyten und Nährstoffen (erhöhter Grundumsatz), wenn nötig Senkung der Körpertemperatur, Gabe von Sauerstoff (O2), eventuell Antibiotika und Thromboembolieprophylaxe. Bei kardialer Symptomatik wird ergänzend mit β-Blockern behandelt – bevorzugt Propranolol, da es zusätzlich die Konversion von T4 zum zehnfach stärker wirksamen T3 hemmt – und Digitalisierung (bei Herzinsuffizienz). Die Thyreostatika werden in diesem Fall intravenös gegeben, eventuell in Ergänzung mit Natriumperchlorat, Lithium-Ionen (Hemmung der Freisetzung von Thyroxin)[36] und Gallensäurebindern (Unterbrechung des enterohepatischen Kreislaufs von Schilddrüsenhormonen).[34] Ergänzend erfolgt die ebenfalls intravenöse Gabe von Glukokortikoiden, die unter anderem ebenfalls die Konversion von T4 zu T3 hemmen. Die Plasmapherese als Notfallmaßnahme hat durch die Möglichkeit der notfallmäßigen Strumaresektion an Bedeutung verloren. Diese kann nach Stabilisierung der Vitalparameter, möglichst innerhalb der ersten 48 Stunden, durchgeführt werden.[37]
Sonderfall der Thyreotoxicosis factitia
Da die Thyreotoxicosis factitia durch die Einnahme von Schilddrüsenhormonen in zu hoher Dosis[38] bedingt ist, genügt zur Behandlung eine kurze Therapiepause beziehungsweise eine Anpassung der Hormondosis.
Plummern
Die Jodaufnahme der Schilddrüse ist nicht nur vom TSH-Spiegel abhängig, sondern unterliegt auch einer jodabhängigen Autoregulation. Gaben großer Mengen von Jodid (mehrere hundert Milligramm – der Tagesbedarf des Gesunden wird von der WHO mit 200 Mikrogramm angegeben) hemmen Jodidaufnahme, Hormonsynthese und Hormonausschüttung (Wolff-Chaikoff-Effekt, nach Louis Wolff, 1898–1972, US-amerikanischer Kardiologe und I. L. Chaikoff, US-amerikanischer Physiologe[39]). Diesen Effekt, der nur wenige Tage anhält, machte man sich früher zur Behandlung einer Hyperthyreose vor Schilddrüsenoperation zunutze („Plummern“, nach Henry Stanley Plummer).[40][41]
Dasselbe Prinzip wird auch zum Schutz vor radioaktivem Jod im Falle einer Kernreaktorkatastrophe angewendet, um das Risiko von Krebserkrankungen der Schilddrüse zu verringern (siehe Jodblockade).
Weblinks
Einzelnachweise
- N. Mathioudakis, D.S. Cooper: Exogenous Thyrotoxicosis. In: T. Davies (eds): A Case-Based Guide to Clinical Endocrinology. Springer, New York NY 2015.
- Schilddrüse und Herzerkrankungen. Deutscher Ärztinnenbund, 2004; abgerufen 5. Februar 2008.
- M. Dietlein, H. Schicha: Schilddrüse 2003. Walter de Gruyter, 2004, ISBN 3-11-018147-9, books.google.com
- Louis J. Acierno: The history of cardiology. Parthenon Pub., London 1994, ISBN 1-85070-339-6, S. 144.
- J. Hädecke, U. Schneyer: Endokrinologische Befunde bei der endokrinen Orbitopathie. In: Klin Monatsbl Augenheilkd. 222, 2005, S. 15–18. doi:10.1055/s-2004-813646
- Stadt Merseburg (Memento vom 2. Februar 2014 im Internet Archive), abgerufen am 24. März 2008.
- Robert James Graves. (Memento vom 13. März 2006 im Internet Archive) whonamedit.com; abgerufen 23. März 2008.
- Malte H. Stoffregen: Basedowsche Krankheit. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4, S. 152 (Google books).
- Tillaux: Thyroidectomie pour un goitre exopht. Bull, de l’acad. de med. 1880, IX. S. 401.
- Rehn: Ueber die Exstirpation des Kropfes bei Morbus Basedowii. In: Berl. klin. Woch. 1884, Nr. 11.
- Otto Westphal, Theodor Wieland, Heinrich Huebschmann: Lebensregler. Von Hormonen, Vitaminen, Fermenten und anderen Wirkstoffen. Societäts-Verlag, Frankfurt am Main 1941 (= Frankfurter Bücher. Forschung und Leben. Band 1), S. 22 f.
- R. Abbe: Exophthalmic goiter reduced by radium. In: Arch. Roentg. Ray. 9, 1904, S. 214–218.
- S. Hertz, A. Roberts: Application of radioactive iodine in therapy of Grave’s disease. In: J div. 21 (624) 1942.
- Martin Metten: Die Auswirkung der Dosisleistung auf den Therapieerfolg der Radiojodtherapie bei funktionellen Schilddrüsenautonomien. Dissertation. Justus-Liebig-Universität, Gießen 2002.
- R. Paschke u. a.: Therapie der uni- oder multifokalen Schilddrüsenautonomie. In: Dtsch Arztebl., 2000.
- C. W. Hedberg u. a.: An outbreak of thyrotoxicosis caused by the consumption of bovine thyroid in ground beef. In: N Engl J Med. 316, 1987, S. 993–998, PMID 3561455.
- B. Köhler, C. Stengel, R. Neiger: Dietary hyperthyroidism in dogs. In: J Small Anim Pract., 53(3), Mar 2012, S. 182–184. doi:10.1111/j.1748-5827.2011.01189.x, PMID 22931400
- L. Steinhoff, B. Ruhmann, A. Mösseler, M. Schmicke (Piechotta): Alimentäre Hyperthyreose beim Hund – eine prospektive Studie. In: Der Praktische Tierarzt, 98, Heft 09/2017, S. 898–907.
- Iodine status worldwide. (PDF; 1,3 MB) WHO, 2004, ISBN 92-4-159200-1.
- K. Miehle, R. Paschke: Sind TSH-Rezeptor Polymorphismen eine mögliche Ursache für die interindividuell unterschiedlichen Normalbereiche der TSH-, fT3- und fT4-Werte in einer Normalpopulation? (Memento vom 10. Juni 2008 im Internet Archive) Universität Leipzig, Forschungsbericht 2004.
- EN Pearce: Diagnosis and management of thyrotoxicosis. In: BMJ, 2006 Jun 10, 332(7554), S. 1369–1373, PMC 1476727 (freier Volltext).
- Frank Grünwald, Karl-Michael Derwahl: Diagnostik und Therapie von Schilddrüsenerkrankungen. Frankfurt / Berlin 2014, ISBN 978-3-86541-538-7, S. 50 und S. 52.
- J. Feldkamp: Epidemiologie von Autoimmunthyreopathien. In: K. Mann, B. Weinheimer, O. E. Janßen (Hrsg.): Schilddrüse und Autoimmunität. Berlin / New York 2002, ISBN 3-11-017476-6, S. 66–73.
- Gerd Herold: Innere Medizin. 2007.
- Thyreotoxische Krise und Myxödemkoma. Abgerufen am 19. Juni 2021.
- B. Müller, U. Bürgi: Akropachie bei Hyperthyreose. (Memento vom 11. Dezember 2007 im Internet Archive) In: Schweiz Med Wochenschr. 129/1999, S. 1560; abgerufen 14. Februar 2009.
- Praktisches Vorgehen bei thyreotoxischer Krise. (PDF) Universitätsklinik Freiburg (Flussdiagramm); abgerufen 30. März 2014.
- Online-Rechner zur Berechnung des Burch-Wartosky-Scores, abgerufen am 8. Februar 2008.
- AWMF-Leitlinien-Register Nr. 031/001 Schilddrüsendiagnostik. (Memento vom 15. Dezember 2007 im Internet Archive)
- M. Schott u. a.: Diagnostik bei autoimmunen Schilddrüsenerkrankungen. auf: dgkl.org, abgerufen 5. Februar 2008.
- Matthias Schott, Jochen Seißler, Werner A. Scherbaum: Diagnostik bei autoimmunen Schilddrüsenerkrankungen / Diagnostic testing for autoimmune thyroid diseases. In: LaboratoriumsMedizin. 30, 2006, S. 254, doi:10.1515/JLM.2006.033.
- Webartikel über das Wolfstrappkraut mit weiteren Nachweisen
- J. Rendl, B. Saller: Schilddrüse und Röntgenkontrastmittel: Pathophysiologie, Häufigkeit und Prophylaxe der jodinduzierten Hyperthyreose. In: Dtsch Arztebl. 98(7), 2001, S. A-402 / B-339 / C-316.
- J. W. Dietrich: Thyreotoxische Krise [Thyroid Storm.] In: Med Klin Intensivmed Notfmed. 107, 2012, S. 448–453. PMID 22878518 doi:10.1007/s00063-012-0113-2
- K. Reschke, H. Lehnert: Die thyreotoxische Krise. In: Der Internist. Verlag Springer, Berlin/ Heidelberg, 44/2003, S. 1221–1230. doi:10.1007/s00108-003-1051-0
- Heinz Lüllmann u. a.: Pharmakologie und Toxikologie. 16. Auflage. Thieme Verlag, Stuttgart 2006, ISBN 3-13-368516-3.
- R. Hörmann, K. Mann: Erkrankungen der Schilddrüse. In: Gerhard Steinbeck, Gustav Paumgartner (Hrsg.): Therapie innerer Krankheiten. Springer, 2006, ISBN 3-540-23750-X, S. 960–982.
- Geraldo Medeiros-Neto: Thyroxine Poisoning. In: Endotext, Created: July 17, 2018.
- jrank.org
- Roche Lexikon Medizin. 4. Auflage. Urban & Fischer Verlag, München 1984/1987/1993/1999
- T. Kuwert: Schilddrüse. In: T. Kuwert, F. Grünwald, U. Haberkorn, T. Krause: Nuklearmedizin. Stuttgart / New York 2008, ISBN 978-3-13-118504-4.