Pregabalin
Pregabalin ist ein Arzneistoff aus der Gruppe der Gabapentinoide[3] und gehört als Wirkstoff zu den Antikonvulsiva. Zugelassen ist es EU-weit seit 2004 zur Behandlung neuropathischer Schmerzen, der Epilepsie sowie der Generalisierten Angststörung. Die bekannteste Handelsmarke ist Lyrica. Seit dem 1. Dezember 2014 sind in Deutschland Generika verfügbar.[4]
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
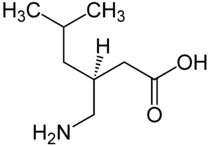 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Pregabalin | |||||||||||||||||||||
| Andere Namen |
(S)-3-(Aminomethyl)-5-methylhexansäure (IUPAC) | |||||||||||||||||||||
| Summenformel | C8H17NO2 | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
N03AX16 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 159,23 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt |
186–188 °C[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Pregabalin war 2009 auf Platz 12 der umsatzstärksten patentgeschützten Arzneimittel in Deutschland, mit einem Umsatz von ca. 220 Millionen Euro.[5] Das Medikament wurde von Richard Bruce Silverman entwickelt.
Chemie
Pregabalin ist ein Derivat der γ-Aminobuttersäure (GABA). Es kann auch als strukturverwandt mit L-Leucin aufgefasst werden. Beide strukturellen Ähnlichkeiten werden im Zusammenhang mit seiner pharmakologischen Wirkung diskutiert. Das Pregabalinmolekül ist ein Zwitterion mit einem isoelektrischen Punkt bei 7,4:[6]
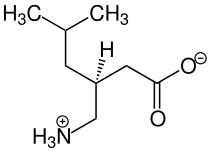
In wässrigen Medien ist es bei pH-Werten unterhalb von 3,7 leicht löslich.
Synthese
Bei der enantioselektiven Synthese von Pregabalin wird zunächst ausgehend von Isobutyraldehyd und Acrylnitril mehrstufig das Salz aus dem tert-Butylammonium-Kation und dem Anion 3-Cyano-5-methyl-3-hexenoat hergestellt, dessen C=C-Doppelbindung dann einer enantioselektiven Hydrierung unterworfen wird und (S)-3-Cyano-5-methylhexansäure liefert. Die Reduktion der Nitrilgruppe liefert dann Pregabalin.[7] Es gibt auch alternative Synthesen, bei denen eine Racematspaltung der Schlüsselschritt ist.[7]
Pharmakologie
Der Wirkmechanismus von Pregabalin wurde erst vor wenigen Jahren entdeckt. Er unterscheidet sich von demjenigen der γ-Aminobuttersäure (GABA), denn Pregabalin wirkt nicht an den GABA-Rezeptoren, sondern die GABA-ähnliche Wirkung wird über andere Mechanismen hervorgerufen.
Pregabalin bindet im zentralen Nervensystem (ZNS) an die Alpha-2-delta-Untereinheit von spannungsabhängigen Calcium-Kanälen vom P/Q-Typ. Das Einströmen von Calcium in die Nervenendigung wird gedrosselt, so dass eine gesteigerte Freisetzung der Neurotransmitter Glutaminsäure, Noradrenalin und Substanz P normalisiert wird. Dieser Wirkansatz als Calciumkanalblocker verbindet die so unterschiedlichen Anwendungsgebiete neuropathischer Schmerz, generalisierte Angststörung und Epilepsie.
Pregabalin wird rasch resorbiert und hat eine geschätzte Bioverfügbarkeit von über 90 Prozent. Es wird so gut wie nicht metabolisiert und unverändert über die Nieren ausgeschieden. Die Plasmahalbwertszeit beträgt 6,3 Stunden.[8]
Medizinische Verwendung
Anwendungsgebiete
Pregabalin wird bei erwachsenen Menschen als Zusatztherapie bei partiellen epileptischen Anfällen (mit und ohne sekundäre Generalisierung), bei peripheren und zentralen neuropathischen Schmerzen (beispielsweise bei Diabetes mellitus, Gürtelrose, Fibromyalgie oder Rückenmarksverletzungen) und generalisierter Angststörung eingesetzt. Die Einstellung der Dosierung erfolgt individuell. Pregabalin wurde auch im Rahmen von chirurgischen Operationen zur Behandlung akuter Schmerzen eingesetzt.[9]
Pregabalin ist in der Lage, Entzugssymptome bei Opiatabhängigkeit zu reduzieren.[10]
Einige Studien haben gezeigt, dass Pregabalin ebenfalls erfolgreich (als Off-Label-Therapie) bei der Behandlung der sozialen Phobie eingesetzt werden kann.[11]
Neuropathische Schmerzen
Die Wirksamkeit konnte in Studien bei diabetischer Neuropathie, postherpetischer Neuralgie und nach Rückenmarkverletzung gezeigt werden. In anderen Modellen zum neuropathischen Schmerz wurde die Wirksamkeit nicht untersucht. Pregabalin wurde in 10 kontrollierten klinischen Studien untersucht, bei zweimal täglicher Gabe bis zu 13 Wochen und bei dreimal täglicher Gabe bis zu 8 Wochen. Insgesamt waren die Sicherheits- und Wirksamkeitsprofile bei zweimaliger und bei dreimaliger Gabe ähnlich. In klinischen Studien über bis zu 12 Wochen wurde sowohl bei peripheren als auch zentralen neuropathischen Schmerzen eine Schmerzverringerung innerhalb der 1. Woche festgestellt und blieb während der gesamten Behandlungsperiode erhalten.
In kontrollierten klinischen Studien bei peripheren neuropathischen Schmerzen kam es bei 35 % der mit Pregabalin behandelten Patienten und bei 18 % der Patienten unter Placebo zu einer 50%igen Verbesserung des Schmerzscores. Unter den Patienten, bei denen es nicht zu Schläfrigkeit kam, kam es bei 33 % der mit Pregabalin behandelten Patienten zu einer derartigen Verbesserung und bei 18 % der Patienten unter Placebo. Bei den Patienten, bei denen es zu Schläfrigkeit kam, betrugen die Responder-Raten unter Pregabalin 48 % und 16 % unter Placebo.
In der kontrollierten klinischen Studie bei zentralen neuropathischen Schmerzen kam es bei 22 % der mit Pregabalin behandelten Patienten und 7 % der Patienten unter Placebo zu einer 50%igen Verbesserung des Schmerzscores.[12]
Zusatztherapie
Pregabalin wurde in drei kontrollierten klinischen Studien sowohl bei zweimal täglicher als auch bei dreimal täglicher Gabe über jeweils 12 Wochen untersucht. Insgesamt war das Verträglichkeits- und Wirksamkeitsprofil bei zweimal und bei dreimal täglicher Gabe ähnlich. Eine Reduktion der Anfallshäufigkeit wurde innerhalb der ersten Woche beobachtet.[13]
Kinder und Jugendliche
Die Wirksamkeit und Sicherheit von Pregabalin als Zusatztherapie von Epilepsie wurden bei pädiatrischen Patienten unter 12 Jahren und Jugendlichen nicht nachgewiesen. Die Nebenwirkungen, die in einer Studie zur Pharmakokinetik und Verträglichkeit unter Beteiligung von Patienten ab einem Alter von 3 Monaten bis 16 Jahren (n = 65) beobachtet wurden, waren jenen, die bei Erwachsenen beobachtet wurden, ähnlich. Die Ergebnisse einer einjährigen unverblindeten Sicherheitsstudie unter Beteiligung von 54 pädiatrischen Epilepsiepatienten ab einem Alter von 3 Monaten bis 16 Jahren zeigen, dass die Nebenwirkungen Fieber und Infektionen der oberen Atemwege häufiger als in Studien bei Erwachsenen beobachtet wurden. Monotherapie (neu diagnostizierte Patienten): In einer kontrollierten klinischen Studie über 56 Wochen wurde Pregabalin bei zweimal täglicher Gabe untersucht. Bezogen auf den Endpunkt einer sechsmonatigen Anfallsfreiheit zeigte Pregabalin im Vergleich zu Lamotrigin keine Nichtunterlegenheit. Pregabalin und Lamotrigin waren gleichermaßen sicher und gut verträglich.[14]
Generalisierte Angststörungen
Pregabalin wurde in 6 kontrollierten Studien über einen Zeitraum von 4 bis 6 Wochen sowie in einer 8-wöchigen Studie mit älteren Patienten und in einer Langzeitstudie zur Rückfallprävention mit einer doppelblinden Rückfallpräventionsphase von 6 Monaten untersucht. Eine Besserung der Symptome von generalisierten Angststörungen gemäß der Hamilton-Angst-Skala (HAM-A) wurde innerhalb der 1. Woche beobachtet. In kontrollierten klinischen Studien über 4 bis 8 Wochen zeigten 52 % der mit Pregabalin behandelten Patienten und 38 % der Patienten unter Placebo eine im Vergleich zu den Ausgangswerten mindestens 50%ige Verbesserung des HAM-A-Gesamt-Scores.[15]
Nebenwirkungen und Anwendungsbeschränkungen
Zu den häufigsten Nebenwirkungen zählen Schwindel, Müdigkeit, Benommenheit, nachlassende Aufmerksamkeit, Trunkenheitsgefühl, insbesondere zu Beginn der Behandlung. Des Weiteren kann es zu verschwommenem Sehen, Doppeltsehen, Gleichgewichtsstörungen, Erektionsstörungen, Ödemen, Übelkeit und Erbrechen kommen. Eine Gewichtszunahme ist häufig. Gelegentliche Nebenwirkungen sind Muskelzucken, Muskelkrämpfe, Herzrhythmusstörungen, Kraftlosigkeit und Stürze. Selten auftretende Nebenwirkungen sind Schluckbeschwerden, hoher Blutzucker, Muskelschäden, Nierenversagen, Brustschmerzen und Veränderungen der Sicht (Tiefenwahrnehmung, Lichtblitze, optische Helligkeit). Weitere Nebenwirkungen, die nach Markteinführung berichtet wurden und deren Häufigkeit nicht bestimmt werden kann, sind Herzmuskelschwäche (Herzinsuffizienz), Änderung der Aufnahme von elektrischen Veränderungen (EKG) des Herzens, die mit Herzrhythmusstörungen zusammenhängen, Flüssigkeit in der Lunge, Verlust des Bewusstseins, Krampfanfälle sowie Überempfindlichkeits- und allergische Reaktionen.
Nach Absetzen einer Pregabalin-Therapie wurden bei einigen Patienten zum Teil schwere Entzugs-Symptome festgestellt. Pregabalin sollte deshalb nicht plötzlich abgesetzt, sondern ausschleichend dosiert werden, da es sonst auch zu einer Häufung epileptischer Anfälle kommen kann. Benommenheit und Schläfrigkeit können vor allem bei älteren Patienten zu Stürzen führen.
Es bestehen Hinweise auf ein Abhängigkeitspotenzial von Pregabalin, entsprechende Berichte gibt es aus Deutschland[16][17][18] und Schweden.[19] Die Fachinformationen wurden um den Hinweis erweitert: „Fälle von nicht bestimmungsgemäßem Gebrauch, Missbrauch und Abhängigkeit wurden berichtet. Bei Patienten mit Drogenmissbrauch in der Vorgeschichte ist Vorsicht geboten und der Patient sollte hinsichtlich Symptomen eines nicht bestimmungsgemäßen Gebrauchs, des Missbrauchs oder der Abhängigkeit von Pregabalin (…) überwacht werden.“
Der Wirkstoff Pregabalin kann die Wirkung von ZNS-dämpfenden Substanzen wie Lorazepam und Alkohol verstärken, bis hin zu Atemschwäche (respiratorischer Insuffizienz) und Koma. Er verstärkt vermutlich auch kognitive und grobmotorische Beeinträchtigungen nach Einnahme von Oxycodon.[20]
Eine gleichzeitige Verwendung von Pregabalin und oralen hormonellen Kontrazeptiva („Antibabypille“) ist möglich.
Bei Niereninsuffizienz muss die Dosierung reduziert werden.
Anwendung bei Kindern und Jugendlichen
Es liegen keine Untersuchungen zur Anwendung bei Kindern und Jugendlichen unter 18 Jahren vor. Es kann deswegen nicht empfohlen werden, dass diese Personengruppen Pregabalin anwenden.[21]
Anwendung bei Schwangeren und in der Stillzeit
Es gibt keine kontrollierten klinischen Studien zur Anwendung von Pregabalin bei schwangeren Frauen. Tierversuche lassen jedoch vermuten, dass möglicherweise Gefahren für den Fötus bestehen könnten. Pregabalin sollte deshalb in der Schwangerschaft nur angewendet werden, wenn es unbedingt notwendig ist.[21] Nach Angabe des Herstellers Pfizer ist die Anwendung bei Schwangerschaft ausgeschlossen, es wird explizit darauf hingewiesen, dass gebärfähige Frauen eine „wirksame Verhütungsmethode“ anwenden müssen.[22]
Auswirkungen auf die Fahrtüchtigkeit
Durch die Einnahme von Pregabalin kann es zu Benommenheit und Schläfrigkeit kommen. Deshalb wird Patienten davon abgeraten, Auto zu fahren, komplexe Maschinen zu bedienen oder andere potenziell gefährliche Tätigkeiten auszuführen, solange nicht bekannt ist, ob die Fähigkeit zur Ausübung solcher Tätigkeiten beeinträchtigt wird.[21]
Siehe auch
Weblinks
- Gebrauchsinformation (Rote Liste Patienteninfoservice)
- Lyrica auf der Website der Europäischen Arzneimittelagentur
- Bewertung
Einzelnachweise
- The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage, 2006, S. 1327–1328, ISBN 978-0-911910-00-1.
- Datenblatt Pregabalin bei Sigma-Aldrich, abgerufen am 15. Februar 2022 (PDF).
- Arznei-News.de: Liste der Gabapentinoide. 13. Juni 2019, abgerufen am 10. März 2021.
- Kassenärztliche Vereinigung Westfalen-Lippe (Letzte Veröffentlichung: 19. Dezember 2014).
- U. Schwabe, D. Paffrath (Herausgeber): Arzneiverordnungs-Report 2010 (Springer Medizin Verlag, Heidelberg).
- J. Cook, W. Addicks, Y.i H. Wu: Application of the Biopharmaceutical Classification System in Clinical Drug Development—An Industrial View, I.: AAPS J. 2008 Jun; 10(2): 306–310. doi:10.1208/s12248-008-9036-5, PMC 2751386 (freier Volltext).
- Axel Kleemann, Jürgen Engel, Bernd Kutscher und Dieter Reichert: Pharmaceutical Substances, Thieme-Verlag Stuttgart, 5. Auflage (2009), S. 1135–1138, ISBN 978-3-13-558405-8; zusätzlich online mit halbjährlichen Ergänzungen und Aktualisierungen.
- Pharmazeutische Zeitung online, abgerufen am 23. Januar 2015.
- N. Eipe, J. Penning, F. Yazdi und andere: Perioperative use of pregabalin for acute pain – a systematic review and meta-analysis. In: Pain. Band 156, 2015, S. 1284–1300.
- N. Kämmerer, T. Lemenager, M. Grosshans, F. Kiefer, D. Hermann: [Pregabalin for the reduction of opiate withdrawal symptoms]. In: Psychiatrische Praxis. Band 39, Nummer 7, Oktober 2012, S. 351–352, doi:10.1055/s-0032-1305042. PMID 22689280.
- P. Kawalec, A. Cierniak, A. Pilc, G. Nowak: Pregabalin for the treatment of social anxiety disorder. In: Expert opinion on investigational drugs. Band 24, Nummer 4, April 2015, S. 585–594, doi:10.1517/13543784.2014.979283, PMID 25361817 (Review).
- Fachinformation (Zusammenfassung der Merkmale des Arzneimittels/SPC) „Lyrica“ (Pfizer), März 2015, Satz-Rechen-Zentrum Berlin, Fachinformationsdienst.
- Fachinformation (Zusammenfassung der Merkmale des Arzneimittels/SPC) „Lyrica“ (Pfizer), März 2015, Satz-Rechen-Zentrum Berlin, Fachinformationsdienst.
- Fachinformation (Zusammenfassung der Merkmale des Arzneimittels/SPC) „Lyrica“ (Pfizer), März 2015, Satz-Rechen-Zentrum Berlin, Fachinformationsdienst.
- Fachinformation (Zusammenfassung der Merkmale des Arzneimittels/SPC) „Lyrica“ (Pfizer), März 2015, Satz-Rechen-Zentrum Berlin, Fachinformationsdienst.
- Mitteilung der Arzneimittelkommission der deutschen Ärzteschaft zum Abhängigkeitspotenzial von Pregabalin, 5. Juni 2011.
- Landesärztekammer Baden-Württemberg: Lyrica® (Pregabalin) – Das neue Suchtmittel, 25. Oktober 2012.
- M. Grosshans, J. Mutschler, D. Hermann et al.: Pregabalin abuse, dependence, and withdrawal: a case report. American Journal of Psychiatry 167 (2010), S. 869.
- S. Schwan, A. Sundstrom, E. Stjernberg et al.: A signal for an abuse liability for pregabalin results from the Swedish spontaneous adverse drug reaction reporting system, European Journal of Clinical Pharmacology 66 (2010), S. 947–953.
- Fachinformation zu Lyrica-Hartkapseln (Memento des Originals vom 7. August 2015 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis., Fa. Pfizer, Februar 2013.
- Fachinformation des Arzneimittel-Kompendium der Schweiz: Lyrica®; Stand: Juli 2007.
- Gebrauchsinformation „Lyrica“ (Pfizer), Januar 2012.