Danishefsky-Dien
Das Danishefsky-Dien (nach Samuel Danishefsky) ist eine chemische Verbindung aus der Stoffklasse der Diene. Es besitzt das Grundgerüst des 1,3-Butadiens, das in der 1-Position eine Methoxygruppe und in der 3-Position einen Trimethylsilylether besitzt.[3]
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Danishefsky-Dien | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C8H16O2Si | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 172,30 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
0,89 g·cm−3 (20 °C)[1] | |||||||||||||||
| Siedepunkt | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Eigenschaften
Es handelt sich um eine farblose Flüssigkeit mit einem Brechungsindex von 1,454 (20 °C). Der Flammpunkt liegt bei 59 °C.[2]
Herstellung
Das Danishefsky-Dien kann aus kommerziell erhältlichem trans-4-Methoxybut-3-en-2-on synthetisiert werden. Dieses wird zunächst durch eine Base, zum Beispiel Triethylamin, deprotoniert. Das entstandene Enolat wird mit Zinkchlorid stabilisiert und mit Chlortrimethylsilan zum Danishefsky-Dien umgesetzt.
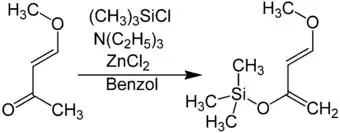
Verwendung
Das Danishefsky-Dien wird zur Diels-Alder-Reaktion verwendet. Es ermöglicht die Synthese von Produkten mit einer Carbonylfunktion in einer Position, die mit anderen Dienen nicht in einer Diels-Alder-Reaktion zugänglich sind. Dies wird durch die Aufarbeitung gesteuert: Nach der Diels-Alder-Reaktion kann der Silylether mit verdünnter Salzsäure abgespalten werden, wodurch zunächst ein Enol entsteht, das dann zum Keton tautomerisiert. Das entstandene Keton kann eine nützliche Funktionalisierung für folgende Reaktionsschritte sein. Auch die Methoxygruppe kann sauer abgespalten werden, falls sie nicht erwünscht ist, wobei eine Doppelbindung resultiert.
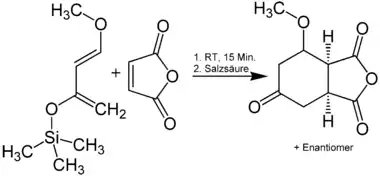
Das Danishefsky-Dien ist ein elektronenreiches Dien und zeigt in Reaktionen eine hohe Regioselektivität. Die elektronenreichste Position befindet sich an C-1, an das die Methoxygruppe gebunden ist. Werden unsymmetrische Dienophile eingesetzt, so reagiert diese Position bevorzugt mit der elektronenärmeren Position des eingesetzten Dienophils. Auch in Hetero-Diels-Alder-Reaktionen kann das Danishefsky-Dien verwendet werden. Ein Beispiel hierfür ist eine Aza-Diels-Alder-Reaktion, bei der die C=N-Doppelbindung eines Imins als Dienophil reagiert:
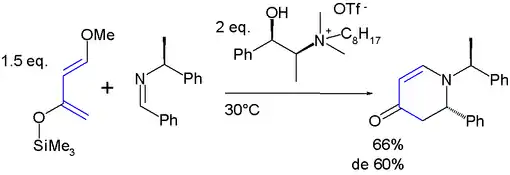
Varianten
Es existieren auch Abwandlungen des Danishefsky-Diens. Hierbei werden meist andere Reste am Silylether und am Ether eingesetzt. Diese werden unter dem Sammelbegriff Danishefsky-Diene zusammengefasst.
Weblinks
Einzelnachweise
- Datenblatt Danishefsky-Dien (PDF) bei Merck, abgerufen am 19. Januar 2011.
- Datenblatt trans-1-Methoxy-3-trimethylsiloxy-1,3-butadiene bei Sigma-Aldrich, abgerufen am 25. Mai 2011 (PDF).
- S. Danishefsky, T. Kitahara, J. Am. Chem. Soc. 1974, 96, 7807–7808.
