Bindungsenergie
Bindungsenergie muss aufgebracht werden, um ein gebundenes System aus zwei oder mehr Bestandteilen (beispielsweise einen Himmelskörper, ein Molekül, ein Atom, einen Atomkern), die durch Anziehungskräfte zusammengehalten werden, in seine Bestandteile zu zerlegen. Eine ebenso große Energie wird freigesetzt, wenn sich das gebundene System aus den Einzelteilen bildet. Manchmal wird unter Bindungsenergie nicht diese Energiemenge selbst, sondern die Änderung des Energieinhalts des Systems verstanden, wenn seine Teile sich miteinander verbinden; dann hat sie den gleichen Betrag, ist aber negativ. So ist z. B. die in der Chemie gebräuchliche Reaktionsenthalpie negativ, wenn bei der Reaktion Energie frei wird.
Die Bezeichnung Bindungsenergie ist ein gängiger Fachausdruck, aber sprachlich etwas unglücklich gewählt. Sie führt – besonders mit einem nachfolgenden Genitiv, wie z. B. Bindungsenergie „des Uran-Atomkerns“ oder „des ATP-Moleküls“ – leicht zu dem Missverständnis, es handele sich um einen Energiebetrag, der in dem gebundenen System vorhanden ist und aus ihm freigesetzt werden kann. Richtig ist, wie oben gesagt, das Gegenteil: Die Bindungsenergie ist bereits bei der Bildung des gebundenen Systems freigesetzt und abgegeben worden, ist also nun nicht mehr verfügbar.
Veranschaulichung
Wenn beispielsweise der Abstand zweier Dauermagnete hinreichend gering ist, ziehen sie einander an und bewegen sich aufeinander zu. Augenblicke vor dem Zusammenstoß besitzen beide Magnete ihre höchste kinetische Energie, welche dann in Schallenergie und Wärme umgewandelt wird. Um die Magnete wieder voneinander zu trennen, muss die Bindungsenergie aufgebracht werden. Sie stimmt vom Betrag her mit der insgesamt vorher freigesetzten Energie überein.
Chemie
Die chemische Bindungsenergie ist das Maß für die Stärke einer kovalenten Bindung. Die molare Bindungsenergie von Ionenkristallen wird unter Gitterenergie und Gitterenthalpie beschrieben.
Bindungsenergien zwischen Atomen liegen bei Molekülen zwischen 200 und 700 kJ·mol−1 (2 bis 7 eV pro Bindung). Besonders geringe Bindungsenergien beobachtet man bei Wasserstoffbrückenbindungen. Sie sind mit nur 17 bis 167 kJ/mol[1] (0,18 bis 1,7 eV pro Bindung) deutlich schwächer als die Bindungskraft innerhalb eines Moleküls.
Atomphysik
In der Atomphysik wird als Bindungsenergie die Energie bezeichnet, die zum Zerlegen eines Atoms/Ions in ein (anderes) Ion und ein Elektron nötig ist. Sie kommt durch die elektrische Anziehung zwischen Elektron und Atomkern zustande. Beim Einfangen eines Elektrons wird der gleiche Energiebetrag frei. Chemiker bevorzugen anstelle von Bindungsenergie oft den Terminus Ionisierungsenergie.
Besonders geringe Bindungsenergien besitzen die Valenzelektronen der ersten Hauptgruppe, von 13,6 eV beim Wasserstoffatom über 5,14 eV für Natrium bis 3,9 eV für Caesium. Je höher geladen ein Ion wird, desto höher wird auch die Bindungsenergie der verbliebenen Elektronen. So betragen die zweite und dritte Ionisierungsenergie bei Natrium schon 47 beziehungsweise 72 eV.[2]
Um ein Elektron aus einem ungeladenen Festkörper zu entfernen, muss Energie aufgewendet werden, die als Austrittsarbeit bezeichnet wird. Sie ist oft erheblich geringer als die Bindungsenergie im isolierten Atom und beträgt z. B. beim Caesium nur 2,14 eV. Ihr Wert lässt sich durch den Schottky-Effekt verringern. Die Austrittsarbeit ist z. B. beim Edison-Richardson-Effekt, Sekundärelektronenvervielfacher, Sekundärelektronenmikroskop und photoelektrischen Effekt von Bedeutung.
Auch bei einem gleichrichtenden Metall-Halbleiter-Übergang wie in der Schottky-Diode müssen Elektronen die Schottky-Barriere überwinden, diese liegt meist zwischen 0,5 und 0,9 eV. Die Bandlücke im Bändermodell eines Halbleiters entspricht der Bindungsenergie eines Elektrons im Valenzband.
Manchmal ist mit Bindungsenergie diejenige des gesamten Atoms (also nicht nur die eines einzelnen Elektrons) gemeint. Wir bezeichnen mit die Bindungsenergie aller Elektronen der Hülle eines Atoms. Sie ist gleich der Differenz der Energieäquivalente der Summe aller Massen ohne Bindung und des Energieäquivalents der Masse des neutralen Atoms
- .
Dabei bedeuten
- die Kernmasse des Atoms,
- seine Ordnungszahl,
- die Masse eines Elektrons,
- die Masse des neutralen Atoms,
- die Lichtgeschwindigkeit.
Die gesamte Bindungsenergie der Elektronenhülle kann nicht leicht im Experiment gemessen werden. Man ist stattdessen weitgehend auf theoretische Abschätzungen[3] angewiesen. Für Uran-Isotope 92U, also , zum Beispiel ergibt sich aus Rechnungen eine totale elektronische Bindungsenergie von etwa 760 keV.[4] Zum Vergleich sei daran erinnert, dass das Energieäquivalent der Masse eines Elektrons 511 keV beträgt.
Kernphysik
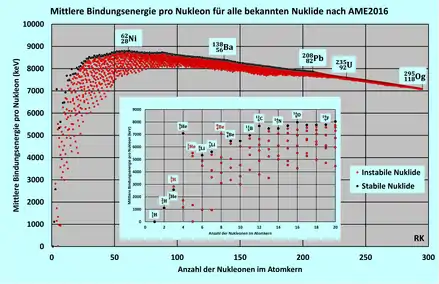
In der Kernphysik ist die Bindungsenergie die Energiemenge, die aufgewandt werden muss, um den Atomkern in seine Nukleonen zu zerlegen.[5] Umgekehrt wird eine ebenso große Energie frei, wenn sich Nukleonen zu einem Kern vereinigen.
Die Bindung kommt durch die anziehende Kraft der starken Wechselwirkung zwischen benachbarten Nukleonen zustande. Diese überwiegt die gegenseitige Coulomb-Abstoßung der elektrisch positiv geladenen Protonen im Kern. Die maximale Bindungsenergie pro Nukleon wird bei Nickel-62[6] erreicht. Die geringere Bindungsenergie pro Nukleon außerhalb dieses Maximums ist anschaulich verständlich:
- Leichtere Kerne haben einen größeren Bruchteil ihrer Nukleonen an der Oberfläche, wo sie weniger bindende Nachbarn haben.
- Bei schwereren Kernen überwiegt die abstoßende Coulombkraft aller Protonen mit ihrer langen Reichweite die starke, aber kurzreichweitige anziehende Kraft der nächsten Nachbarn.
Daher kann im Gebiet der leichten Kerne durch Kernverschmelzung (Kernfusion), im Gebiet der schweren Kerne durch Kernspaltung technisch nutzbare Energie gewonnen werden.
Die Bindungsenergie von Atomkernen kann im Rahmen des Tröpfchenmodells mit der Bethe-Weizsäcker-Formel abgeschätzt werden. Die Zacken in der Graphik hängen mit den Magischen Zahlen zusammen.
Die Bindung ist wegen der Äquivalenz von Masse und Energie mit einem Massendefekt verbunden: Der gebundene Kern hat zwischen 0,1 % (Deuteron) und 0,9 % (Ni-62) weniger Masse als alle seine Nukleonen zusammengenommen. Aus einer genauen Bestimmung der Masse eines Atoms lässt sich daher die Bindungsenergie des Kerns ableiten:
Dabei ist
- die Masse des Atoms,
- seine Massenzahl,
- seine Ordnungszahl,
- die Masse eines freien Protons,
- die Masse eines Elektrons,
- die Masse eines freien Neutrons,
- die Lichtgeschwindigkeit.
Die Bindungsenergie kurzlebiger Kerne lässt sich beispielsweise durch Messung der Energien ihrer Zerfallsprodukte bestimmen.
Gravitation
Die gravitative Bindungsenergie ist diejenige Energie, die benötigt wird, um einen durch Gravitation zusammengehaltenen Körper (z. B. die Erde) in sehr viele winzige Bestandteile zu zerlegen und diese unendlich weit voneinander zu entfernen. Umgekehrt wird die gleiche Energiemenge freigesetzt, wenn sich diese Bestandteile zu einem gravitativ gebundenen Körper zusammenfügen. Dies geschieht beim Kollaps einer Gaswolke zu einem kompakteren Himmelskörper, etwa einem Stern (s. auch Jeans-Kriterium), und führt zu einer Erwärmung der Wolke.
Rechenbeispiel
Idealisiert man einen Himmelskörper als Kugel mit Radius und homogener Dichte , so ergibt sich die Bindungsenergie folgendermaßen:
Man lässt zunächst auf eine Kugel mit Radius (mit ) und Dichte aus unendlicher Entfernung weitere Materie fallen, so dass sich eine Kugelschale der Dicke auf der Oberfläche bildet und man eine neue Kugel mit Radius und Dichte erhält.
Das Gravitationspotential der bisherigen Kugel ist (mit außerhalb der Kugel)
- ,
wobei
die Masse der bisherigen Kugel ist. Die hinzuzufügende Kugelschale der Dicke soll die gleiche Dichte haben. Es muss also eine Masse
aus dem Unendlichen auf die Kugeloberfläche gebracht werden. Die dabei freiwerdende Energie ist
- .
Baut man so Schicht für Schicht eine Kugel mit Radius zusammen, so wird insgesamt die folgende Bindungsenergie frei:
Die Bindungsenergie beträgt also
- .
Eine homogene Kugel mit Masse und Radius der Erde besäße nach dieser Formel eine gravitative Bindungsenergie von etwa 2,24 · 1032 J. Die Erde ist allerdings keine Kugel homogener Dichte: Der Erdkern hat eine fast doppelt so hohe Dichte wie der Erdmantel. Nach dem „Preliminary Reference Earth Model“ (PREM) für die Dichteverteilung im Erdinnern errechnet sich eine Bindungsenergie der Erde von 2,489 · 1032 J.
Weblinks
- Was ist Bindungsenergie? aus der Fernseh-Sendereihe alpha-Centauri (ca. 15 Minuten). Erstmals ausgestrahlt am 12. Mai 2004.
Einzelnachweise
- George A. Jeffrey: An Introduction to Hydrogen Bonding. Oxford University Press, 1997, ISBN 0-19-509549-9.
- Eigenschaften von Natriumatomen bei webelements.com.
- Keh-Ning Huang et al.: Neutral-atom electron binding energies from relaxed-orbital relativistic Hartree-Fock-Slater calculations 2 ≤ Z ≤ 106. In: Atomic Data and Nuclear Data Tables. Band 18, Nr. 3, 1976, S. 243–291, doi:10.1016/0092-640X(76)90027-9.
- Georges Audi: A Lecture on the Evaluation of Atomic Masses. 2004, S. 11 (31 S., [PDF; abgerufen am 11. Januar 2017]).
- Wolfgang Demtröder: Experimentalphysik 4: Kern-, Teilchen- und Astrophysik, Springer DE 2009, ISBN 3-642-01597-2, S. 26; eingeschränkte Vorschau in der Google-Buchsuche
- M. P. Fewell: The atomic nuclide with the highest mean binding energy. In: American Journal of Physics. 63, Nr. 7, 1995, S. 653–658. bibcode:1995AmJPh..63..653F. doi:10.1119/1.17828. Darin wird auch dargestellt, wie die falsche, aber immer noch verbreitete Zuschreibung der festesten Bindung zu Eisen-56 entstanden sein könnte. Tatsächlich ist Ni-62 pro Nukleon um 0,04% fester gebunden.