2,5-Hexandion
2,5-Hexandion (Summenformel C6H10O2) ist ein Diketon und ein für den menschlichen Körper toxischer Metabolit des n-Hexans.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
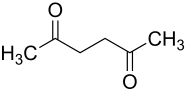 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 2,5-Hexandion | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C6H10O2 | ||||||||||||||||||
| Kurzbeschreibung |
klare, farblose, aromatisch riechende Flüssigkeit[2][3] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 114,14 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Brechungsindex |
1,423 (20 °C, 589 nm)[4] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Gewinnung und Darstellung
2,5-Hexandion lässt sich durch alkalische Hydrolyse von Diacetylbernsteinsäureester und anschließendes Erhitzen (Keton-Spaltung) darstellen.[2] Es kann auch durch Oxidation von Allylaceton hergestellt werden.[5]
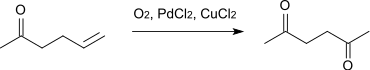
Die Synthese ist auch durch Oxidation von 2,5-Dimethylfuran möglich.[6][5]
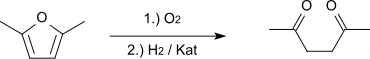
Ein weiterer Syntheseweg, ausgehend von Acetessigester und Propylenoxid, wurde ebenfalls beschrieben. Das Kondensationsprodukt, α-Aceto-γ-valerolacton, wird mit verdünnter Salzsäure zu 5-Hydroxy-2-hexanon umgesetzt (saure Verseifung und anschließende Decarboxylierung), das schließlich mit Natriumdichromat und Schwefelsäure zu 2,5-Hexandion oxidiert wird.[7][5]
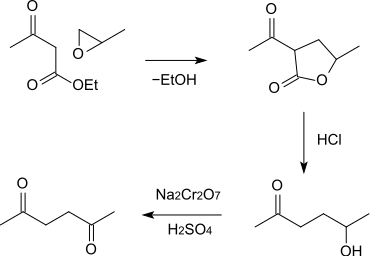
Sogar auf direktsynthetische Weise kann man zum Acetonylaceton gelangen. Dies meint die radikalisch verlaufende Dehydrodimerisierung von Aceton nach Klaus Schwetlick.[8]
Eigenschaften
2,5-Hexandion reagiert unter anderem mit der funktionellen Gruppe der Amine, wie sie zum Beispiel in Proteinen vorkommen. Dort bewirkt es eine Vernetzung der Moleküle und Verlust der Proteinfunktionalität. Vernetzung mit der α-Aminosäure Lysin führt in weiterer Folge zur Bildung des aromatischen 2,5-Dimethylpyrrol.[9]
Verwendung
2,5-Hexandion wird als Lösungsmittel für Celluloseacetat, Gerbmittel, Lacke und Farben verwendet. Auch als Schutzgruppe für primäre Amine und als Zwischenprodukt für die organische Synthese sowie zur Herstellung von Pharmazeutika wird es verwendet.[2][10]
Biologische Bedeutung
Der Metabolit 2,5-Hexandion ist ein Zwischenprodukt im Verlauf der Umwandlung von n-Hexan zu 3-Methylcyclopent-2-en-1-on durch intramolekulare Aldolkondensation.[11][12]
Sicherheitshinweise
Der Stoff kann beim Menschen Reizung der Augen, der Haut und der Schleimhäute, Entfettung und orange-braune Hautentzündungen und Bewusstlosigkeit hervorrufen.[13][14] Im menschlichen Körper kommt 2,5-Hexandion als Metabolit des Hexans vor und wird über den Urin ausgeschieden. 2,5-Hexandion ist wesentlich toxischer als n-Hexan selbst und führt durch die Quervernetzungsreaktionen zu irreparablen Nervenschädigungen.[15][16]
2,5-Hexandion wirkt auch toxisch auf die Spermatogenese über eine Schädigung der Sertoli-Zellen, die das Epithel der Samenkanälchen in den Tubuli seminiferi contorti bilden.[17]
Einzelnachweise
- Eintrag zu ACETONYLACETONE in der CosIng-Datenbank der EU-Kommission, abgerufen am 28. Dezember 2020.
- Eintrag zu 2,5-Hexandion. In: Römpp Online. Georg Thieme Verlag, abgerufen am 26. Mai 2014.
- Eintrag zu 2,5-Hexandion in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2020. (JavaScript erforderlich)
- Datenblatt 2,5-Hexandion (PDF) bei Merck, abgerufen am 16. Mai 2011.
- Patent US3972942A: Oxidation of allylacetone to 2,5-hexanedione in a water-carbon tetrachloride solvent system. Angemeldet am 8. April 1974, veröffentlicht am 3. August 1976, Anmelder: Diamond Shamrock Corp, Erfinder: Ralph H. Lasco.
- G. O. Schenck: Über Autoxydation in der Furanreihe, II. Mitteil.: Über Autoxydation von Furan und 2.5-Dimethyl-furan. In: Berichte der deutschen chemischen Gesellschaft 1945, 77(9–10), S. 661–668. doi:10.1002/cber.19450770902
- R. M. Adams, C. A. Van der Werf: Condensation of Acetoacetic Ester with Some Unsymmetrical Epoxides. In: J. Am. Chem. Soc. 1950, 72(10), S. 4368–4373. doi:10.1021/ja01166a010
- K. Schwetlick, J. Jentzsch, R. Karl, D. Wolter: Dehydrodimerisierungen mit Di-tert.-butylperoxid. In: Journal für praktische Chemie. Band 25, Nr. 1–2, 1964, S. 95–100, doi:10.1002/prac.19640250112.
- cobocards.com: Giftigkeit von Kohlenwasserstoffen (n-Hexan)
- Deutsche Bundesstiftung Umwelt: Biokatalytische Synthese chiraler Synthesebausteine, abgerufen am 28. Januar 2020.
- Lawrence P. Wackett and C. Douglas Hershberger: Biocatalysis and Biodegradation: Microbial Transformation of Organic Compounds, ASM Press, Wash. DC., 2001 .
- T. Soriano, M. Menéndez, P. Sanz, M. Repetto: Method for the simultaneous quantification of n-hexane metabolites: application to n-hexane metabolism determination, in: Human & Experimental Toxicology, 1996, 15 (6), S. 497–503; PMID 8793533.
- Daunderer-Klinische Toxikologie-50. Erg. Lfg. 1/90.
- KÜHN, BlRETT: Merkblätter Gefährliche Arbeitsstoffe, ecomed, Landsberg, 1986, Erg. Lfg.
- Schadstofflexikon: Aliphatische Kohlenwasserstoffe
- cobocards.com: CBP
- Philippe Gorlier: SICHERHEITSUNTERWEISUNG 2008 - REPRODUKTIONSTOXIZITÄT (PDF; 562 kB)

