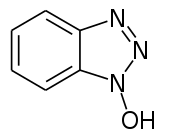
1-Hydroxybenzotriazol
1-Hydroxybenzotriazol (abgekürzt auch oft als HOBt) ist ein in 1-Stellung mit einer Hydroxygruppe substituiertes Derivat des Benzotriazols. Resultierend aus der Struktur mit einem Triazolring und einer Stickstoff-Sauerstoff-Bindung ist die Verbindung thermisch instabil und gilt als explosionsgefährlich. Die wichtigste Anwendung erfolgt als Reagenz in der Peptidsynthese. Die Verbindung enthält die Basisstruktur für weitere in der Peptidsynthese wichtige Benzotriazolderivate wie TBTU und HBTU.
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||
| Allgemeines | ||||||||||
| Name | 1-Hydroxybenzotriazol | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C6H5N3O | |||||||||
| Kurzbeschreibung |
Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse |
| |||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte |
1,438 g·cm−3[2] | |||||||||
| Schmelzpunkt | ||||||||||
| Dampfdruck |
0,009 Pa[2] | |||||||||
| pKS-Wert |
4,6[6] | |||||||||
| Löslichkeit |
4,201 g·l−1 in Wasser (29 °C)[2] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Darstellung und Gewinnung
Die Herstellung von 1-Hydroxybenzotriazol 2 gelingt durch die Oxidation von Benzotriazol 1 mit Wasserstoffperoxid in Gegenwart von Natriumwolframat.[9]
_%C3%9CV1.svg.png.webp)
Eine weitere Synthesevariante ist die Zyklisierung von 2-Chlornitrobenzol 1 mittels Hydrazinhydrat.[10]
_%C3%9CV2.svg.png.webp)
Eigenschaften
1-Hydroxybenzotriazol kann in zwei tautomeren Formen vorliegen.[4] Das Gleichgewicht liegt zwischen den N-Oxid- und N-Hydroxy-Tautomeren. Ein drittes mögliches Tautomer als 1-Oxy-2H-benzotriazol ist thermodynamisch instabil und spielt praktisch keine Rolle.[11][12] Die Gleichgewichtslage hängt von der Art der Lösungsmittel ab. In wässrigem Medium ist das N-Oxid-Tautomer bevorzugt, in organischen Lösungsmitteln wie Methanol, Ethanol, Aceton, Formamid und Dimethylsulfoxid dominiert das N-Hydroxy-Tautomer.[4][11][12] Das N-Oxid-Tautomer kristallisiert aus wässrigem Methanol und fällt als Monohydrat mit 11,7 % Wasser an.[3] Die farblosen Kristalle zeigen einen Schmelzpunkt bei 159–161 °C und bilden ein monoklines Kristallgitter mit der Raumgruppe P21/C.)[3] Das N-Hydroxy-Tautomer kann aus wasserfreien Ethanol/Ether-Gemischen gewonnen werden.[4] Es bildet ebenfalls farblose Kristalle, die bei 169–170 °C schmelzen. Das Kristallgitter ist monoklin mit der Raumgruppe C2/c.[3]

Oberhalb des Schmelzpunktes wird eine stark exotherme Zersetzung mit einer Zersetzungswärme von −2259 kJ·kg−1 bzw. −305 kJ·mol−1 beobachtet.[13] In Deutschland ist 1-Hydroxybenzotriazol entsprechend den Regelungen des Sprengstoffgesetzes als explosionsgefährlicher Stoff eingestuft.[14] Der wasserfreie Stoff ist dabei der Stoffgruppe B zugeordnet. Mischungen mit einem Wassergehalt zwischen 20 % und 47 % fallen noch in die Stoffgruppe C.[14] Im Stahlhülsentest liegt der Grenzdurchmesser der Lochplatte für wasserfreies Material bei 10 mm.[13] Der Grenzdurchmesser sinkt mit zunehmenden Wassergehalt. Mit einem Wassergehalt von 50 % wird allerdings noch ein im Sinne des Sprengstoffgesetzes relevanter Grenzdurchmesser von 2 mm beobachtet.[15] Die Verbindung ist schlagempfindlich. Für wasserfreies 1-Hydroxybenzotriazol reicht eine Schlagenergie von 10 J. Mit einem Wassergehalt bis 20 % ist eine Schlagenergie von 20 J notwendig.[15] Kommerziell ist HOBt ausschließlich als Hydrat im Handel, da dieses als Gefahrgut der Klasser 4.1 als brennbarer Feststoff eingestuft ist. Reines HOBt fällt unter die Gefahrgutklasse 1.3C Explosivstoffe.[15] Der hieraus resultierende erhöhte Aufwand für den Transport und auch die Lagerung ist meist unwirtschaftlich.
Verwendung
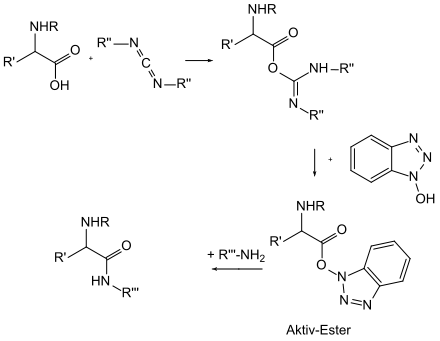
1-Hydroxybenzotriazol (abgekürzt HOBt) ist ein wichtiges Reagenz in der Peptidsynthese sowohl in Lösung als auch in fester Phase. HOBt wird benutzt, um einen sogenannten Aktivester aus einer durch ein Carbodiimid aktivierten Carbonsäure (meist einer geschützten Aminosäure) herzustellen.[16] Diese Aktivester reagieren mit Aminen zu den entsprechenden Peptidbindungen (oder besser Amiden). Die Reaktion mit HOBt als Hilfsreagenz zeichnet sich durch eine racemisierungsarme Reaktion aus, findet bei Raumtemperatur statt und hat in der Regel bessere Ausbeuten im Vergleich zu direkten Kupplungen. Alternativ wird unter anderem HATU, HBTU, TBTU oder 1-Hydroxy-7-azabenzotriazol (HOAT) verwendet.[17]
Literatur
- W. C. Chan, P. D. White: Fmoc Solid Phase Peptide Synthesis. Reprint 2004, Oxford University Press, ISBN 0-19-963724-5.
Einzelnachweise
- Eintrag zu 1-Hydroxybenzotriazol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2020. (JavaScript erforderlich)
- ECHA Substance Information, abgerufen am 27. November 2018.
- Bosch, R.; Jung, G.; Winter, W.: Benzotriazole 1-oxide and 1-hydroxybenzotriazole, C6H5N3O: structures of both tautomeric forms in Acta Crystallogr. Sect. C 39 (1983) 1089–1092, doi:10.1107/S0108270183007490.
- Pfister-Guillouzo, G.; Gracian, F.; Paez, J.A.; Gomez, C.G.; Elguero, J.: Study of 1-hydroxybenzotriazole/benzotriazole N-oxide tautomerism in gas phase by photoelectron spectroscopy in Spectrochim. Acta A51 (1995) 1801–1807, doi:10.1016/0584-8539(95)01441-V.
- Boyle, F.T.; Jones, R.A.Y.: Azole N-oxides. Part I. The tautomerism of benzotriazole 1-oxide and its 4- and 6-nitro-derivatives with the corresponding 1-hydroxybenzotriazoles in J. Chem. Soc. Perkin Trans. 2, 1973, 160–164, doi:10.1039/P29730000160.
- Koppel, I.; Koppel, J.; Leito, I.; Pihl, V.; Grehn, L.; Ragnarsson, U.: in J. Chem. Res. 11 (1993) 3008-3028.
- Eintrag zu 1-hydroxybenzotriazole im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Datenblatt 1-Hydroxybenzotriazol bei Sigma-Aldrich, abgerufen am 25. Januar 2020 (PDF).
- Kruglik, A. P.; Rakhman'ko, E. M.; Asratyan, G. V.: in J. Appl. Chem. USSR (Engl. Transl.) 62 (1989) 2385–2386, 2216–2218.
- Fu, Jie; Yang, Ying; Zhang, Xue-Wei; Mao, Wen-Jun; Zhang, Zhi-Ming; Zhu, Hai-Liang: Discovery of 1H-benzo[d][1,2,3]triazol-1-yl 3,4,5-trimethoxybenzoate as a potential antiproliferative agent by inhibiting histone deacetylase. In: Bioorganic & Medicinal Chemistry 18 (2010) 8457–8462, doi:10.1016/j.bmc.2010.10.049.
- Fruchier, A.; Elguero; J.; Hagarty, A.F.; McGarthy, D.G.: NMR studies in the heterocyclic series. XX—a carbon-13 NMR study of the structures of N-hydroxybenzotriazole and its acylated derivatives in Org. Magn. Reson. 13 (1980) 339–342, doi:10.1002/mrc.1270130508.
- Schilf, W.; Stefaniak, L.; Witanowski, M.; Webb, G.A.: 15N NMR studies of the tautomeric equilibrium of some 1-hydroxybenzotriazoles in Magn. Reson. Chem. 23 (1985) 181–184, doi:10.1002/mrc.1260230310.
- Wehrstedt, K.D.; Wandrey, P.A.; Heitkamp, D.: Explosive properties of 1-hydroxybenzotriazoles in J. Hazard. Mat. A126 (2005) 1–7, doi:10.1016/j.jhazmat.2005.05.044.
- BAM-Bescheide Nr. 416 vom 21. Mai 2002, Nr. 435 vom 23. Januar 2003 und Nr. 471 vom 6. Juni 2010 (PDF; 345 kB).
- UNECE ECOSOC Sub-Committee of Experts on the Transport of Dangerous Goods (TDG) – UN/SCETDG/29/INF.22 – (Germany) – Classification of 1-hydroxybenzotriazole, anhydrous (HOBt), under a division of Class 1 (PDF; 136 kB).
- Wolfgang König, Rolf Geiger: Eine neue Methode zur Synthese von Peptiden: Aktivierung der Carboxylgruppe mit Dicyclohexylcarbodiimid unter Zusatz von 1-Hydroxy-benzotriazolen. In: Chemische Berichte. 103, 1970, S. 788, doi:10.1002/cber.19701030319.
- R. Subirós-Funosas, R. Prohens, R. Barbas, A. El-Faham, F. Albericio: Oxyma: an efficient additive for peptide synthesis to replace the benzotriazole-based HOBt and HOAt with a lower risk of explosion. In: Chemistry. Band 15, Nummer 37, September 2009, S. 9394–9403, doi:10.1002/chem.200900614. PMID 19575348.

