HBTU
HBTU (2-(1H-Benzotriazol-1-yl)-1,1,3,3-tetramethyluronium-hexafluorophosphat) ist ein Kupplungsreagenz, welches in der Peptidsynthese zur Erzeugung von Peptiden verwendet wird.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
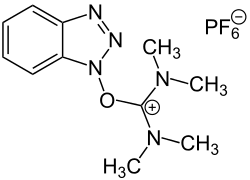 | |||||||||||||||||||
| HBTU (O-Form) | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | HBTU | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C11H16F6N5OP | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 379,24 g·mol−1[1] | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt |
200 °C (Zersetzung)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Die Kupplung von aktivierten Aminosäuren mit Peptiden unter Verwendung von HBTU als Hilfreagenz verläuft racemisierungsarm.[2] HBTU ist ein vergleichsweise mildes Kupplungsreagenz.[3] Alternative Kupplungsreagenzien sind z. B. HATU, HCTU,[4] TBTU, COMU,[5] TOMBU und COMBU.[6]
HBTU kann in zwei Formen vorliegen, als Uroniumsalz (O-Form) oder als das bevorzugte, aber weniger reaktive Iminiumsalz (N-Form):[7]
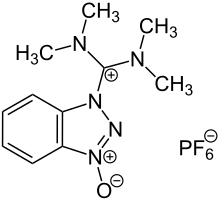
Die Verbindung ist thermisch instabil und kann sich stark exotherm zersetzen. Eine DSC-Messung zeigt ab 173 °C eine Zersetzungsreaktion mit einer Reaktionswärme von −1032 J·g−1 bzw. −391 kJ·mol−1.[8]
Einzelnachweise
- Datenblatt HBTU ≥98.0% (T) bei Sigma-Aldrich, abgerufen am 21. April 2015 (PDF).
- Reinhard Knorr, Arnold Trzeciak, Willi Bannwarth, Dieter Gillessen: New coupling reagents in peptide chemistry. In: Tetrahedron Letters. 30, 1989, S. 1927, doi:10.1016/S0040-4039(00)99616-3.
- Solange Adam: HBTU: a mild activating agent of muramic acid. In: Bioorganic & Medicinal Chemistry Letters. 2, 1992, S. 571, doi:10.1016/S0960-894X(01)81199-9.
- C. U. Hjørringgaard, A. Brust, P. F. Alewood: Evaluation of COMU as a coupling reagent for in situ neutralization Boc solid phase peptide synthesis. In: Journal of Peptide Science. Band 18, Nummer 3, März 2012, S. 199–207, doi:10.1002/psc.1438, PMID 22252935.
- R. Subirós-Funosas, L. Nieto-Rodriguez, K. J. Jensen, F. Albericio: COMU: scope and limitations of the latest innovation in peptide acyl transfer reagents. In: Journal of Peptide Science. Band 19, Nummer 7, Juli 2013, S. 408–414, doi:10.1002/psc.2517, PMID 23712932.
- Y. E. Jad, S. N. Khattab, B. G. de la Torre, T. Govender, H. G. Kruger, A. El-Faham, F. Albericio: TOMBU and COMBU as Novel Uronium-type peptide coupling reagents derived from Oxyma-B. In: Molecules. Band 19, Nummer 11, 2014, S. 18953–18965, doi:10.3390/molecules191118953, PMID 25412042.
- Iman Abdelmoty, Fernando Albericio u. a.: Structural studies of reagents for peptide bond formation: Crystal and molecular structures of HBTU and HATU. In: Letters in Peptide Science. 1, 1994, S. 57, doi:10.1007/BF00126274.
- J. B. Sperry, C. J. Minteer, JingYa Tao, R. Johnson, R. Duzguner, M. Hawksworth, S. Oke, P. F. Richardson, R. Barnhart, D. R. Bill, R. A. Giusto, J. D. Weaver: Thermal Stability Assessment of Peptide Coupling Reagents Commonly Used in Pharmaceutical Manufacturing. In: Organic Process Research & Development. Band 22, 2020, S. 1262–1275, doi:10.1021/acs.oprd.8b00193.

