Azobis(isobutyronitril)
AIBN ist der Kurzname der chemischen Verbindung Azobis(isobutyronitril), die zu den Stoffklassen der Azoverbindungen und Nitrile zählt. Es wird in der Organischen Chemie als Initiator für die Radikal-Kettenreaktion bei der Herstellung von Kunststoffen eingesetzt.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
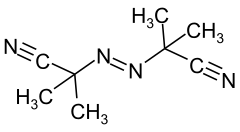 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Azobis(isobutyronitril) | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C8H12N4 | ||||||||||||||||||
| Kurzbeschreibung |
farbloser geruchloser Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 164,21 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Dichte |
1,11 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Darstellung und Eigenschaften
AIBN wird aus Acetoncyanhydrin und Hydrazin hergestellt; das durch Kondensation entstehende 1,2-Bis(2-methylpropionitrilo-2-yl-)hydrazin wird anschließend zu AIBN oxidiert (zum Beispiel durch Chlor). Wegen der Giftigkeit des Zerfallsprodukts Tetramethylbernsteinsäuredinitril wird es in großtechnischen Anlagen nicht mehr genutzt. AIBN ist ein farbloses bis graues, geruchloses, wasserunlösliches Pulver, welches in organischen Lösemitteln und Vinyl-Monomeren gelöst werden kann. Je nach Darstellungsmethode entsteht auch ein feinkristalliner, weißer Feststoff.
AIBN zersetzt sich ab einer Temperatur von über 25 °C unter Abgabe von molekularem Stickstoff in zwei Isobutyronitril-Radikale.[2] Die Entstehung des Stickstoffs liefert die nötige Triebkraft für die Zerfallsreaktion. Dieser Zerfall kann bereits durch Schlag oder Reibung geschehen.[1]
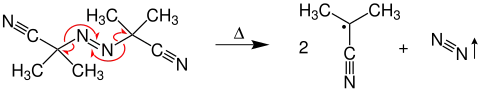
Aufgrund seiner Zersetzlichkeit enthält kommerziell erhältliches AIBN oft Verunreinigungen und muss vor der Verwendung gereinigt werden. Die Reinigung erfolgt meistens durch Umkristallisation, wobei wegen des Anstiegs der Zersetzung bei höherer Temperatur darauf geachtet werden muss, dass beim Auflösen nicht zu stark geheizt wird. Bei zügiger Arbeitsweise kann beispielsweise aus Methanol (Löslichkeit 6,1 g pro 100 g Lösungsmittel[4]) bei maximal 45–50 °C umkristallisiert werden. Setzt man das AIBN dieser Temperatur nur wenige Minuten lang aus, so bilden sich nur geringe Mengen Zersetzungsprodukte, die beim anschließenden Auskristallisieren im Methanol gelöst bleiben.
Beim Einsatz von AIBN als Initiator für radikalische Polymerisationen oder auch bei anderen radikalisch verlaufenden Reaktionen ist die temperaturabhängige Halbwertszeit von großer Bedeutung. Die Temperatur wird üblicherweise so gewählt, dass das AIBN nicht zu schnell zerfällt. Bei zu schnellem Zerfall stiege die Radikalkonzentration im Reaktionsgemisch an, und damit auch die Wahrscheinlichkeit, dass Radikale mit sich selbst rekombinieren, anstatt die eigentlich erwünschte (Ketten-)Reaktion zu initiieren. Die Halbwertszeit beim thermischen Zerfall von AIBN beträgt etwa 10 h bei 65 °C,[4] kann aber mit der Wahl des Lösungsmittels der Reaktion etwas schwanken.
Einzelnachweise
- Eintrag zu 2,2′-Dimethyl-2,2′-azodipropiononitril in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- Eintrag zu Azobis(isobutyronitril). In: Römpp Online. Georg Thieme Verlag, abgerufen am 13. April 2014.
- Eintrag zu 2,2′-dimethyl-2,2′-azodipropiononitrile im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Azo-Initiatoren von Otsuka Chemicals, abgerufen am 29. Januar 2018.

