Sulfonylharnstoffe
Sulfonylharnstoffe sind orale Antidiabetika, Arzneistoffe, die bei Diabetes mellitus Typ 2 (Zuckerkrankheit) eingesetzt werden. Sie ermöglichen die erhöhte Freisetzung von Insulin durch Blockade von Kalium-Kanälen in den β-Zellen der Bauchspeicheldrüse. Sie sind strukturell mit den Sulfonamiden verwandt. Einige Sulfonylharnstoffe sind auch als Herbizid wirksam.
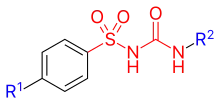
Einsatz als Antidiabetikum
Pharmakologie
Sulfonylharnstoffe stimulieren die Insulinfreisetzung aus den β-Zellen des Pankreas unabhängig von der Blutglucosekonzentration (insulinotrope Wirkung). Sie blockieren die ATP-sensitiven Kaliumkanäle der β-Zelle durch Bindung an spezifische SUR-1 Bindungsstellen. Als Folge der Depolarisation der Zelle öffnen sich spannungsgesteuerte Calciumkanäle. Der Calciumeinstrom führt zu einer Entleerung des Insulins aus den Speichervesikeln und somit zu einer erhöhten Insulinfreisetzung ins Blut. Sie sind wirksam zur Risikosenkung mikrovaskulärer Ereignisse (Glibenclamid). Gliquidon wird als einziger Vertreter der Sulfonylharnstoffe nur über die Leber abgebaut und kann daher bei Niereninsuffizienz gegeben werden.[1][2]
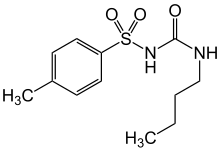
Erste Antidiabetika auf Basis von Sulfonylharnstoffen kamen um 1956 auf den Markt, wichtig war die Entwicklung bei Boehringer Mannheim unter Erich Haack (und zuvor seine Entwicklungen bei der Pharmafirma von Heyden in Radebeul), die zu Oranil (Carbutamid, klinische Tests Hellmuth Kleinsorge) führten, es kamen aber etwa gleichzeitig mehrere andere Medikamente auf den Markt. Die blutzuckersenkende Wirkung von Sulfonamiden stellte zuerst in den 1930er Jahren in Frankreich Auguste Loubatières fest. Die blutzuckersenkende Wirkung wurde zunächst als störende Nebenwirkung der im Vordergrund stehenden antibiotischen Wirkung betrachtet.
Nebenwirkungen
Sulfonylharnstoffe können zu einer Unterzuckerung führen, eventuell auch zu gastrointestinalen Beschwerden. Sie fördern die Gewichtszunahme durch die antilipolytische Wirkung des Insulins. Seltene Nebenwirkungen sind Störungen der Blutbildung oder hepatische Cholestase (wie bei den Sulfonamiden).
Sulfonylharnstoffe erzwingen eine Insulinausschüttung aus den β-Zellen des Pankreas, damit können sie zur Hypoglykämie führen. Weiterhin deuten Studien darauf hin, dass Sulfonylharnstoffe zu einem Versagen der β-Zellen führen können.[3][4][5]
Nach neuesten Studien kann es zu kardialen Risiken durch Sulfonylharnstoffe kommen.[6]
Kontraindikationen
Kontraindiziert sind Sulfonylharnstoffe und deren Derivate bei Diabetes mellitus Typ 1, schwerer Leber- bzw. Niereninsuffizienz (dies gilt nicht für Gliquidon und Repaglinid) und Pankreatektomie. Bei Schwangerschaft müssen Diabetikerinnen auf Insulin umgestellt werden. Weitere Kontraindikationen bestehen bei größeren operativen Eingriffen oder bei schweren Infekten.[7]
Vertreter
Der bekannteste Vertreter ist Glibenclamid. Glimepirid hat eine längere Wirkdauer als Glibenclamid. Ältere, deutlich schwächer wirksame Sulfonylharnstoffe sind Tolbutamid und Carbutamid.
Sulfonylharnstoffe der ersten Generation:
Sulfonylharnstoffe der zweiten Generation:
- Glibenclamid (Handelsnamen zum Beispiel Euglucon N, Normoglucon, Glucobene und Dia-Eptal)
- Glibornurid (Gluborid, Glutril)
- Gliclazid (Handelsname Diamicron UNO)
- Glipizid (Glibenese, Minidiab)
- Gliquidon (Glurenorm)
- Glisoxepid (Pro-Diaban)
- Glycodiazin (Redul)
Sulfonylharnstoffe der dritten Generation:
- Glimepirid (Handelsname zum Beispiel Amaryl)
Einsatz als Herbizid
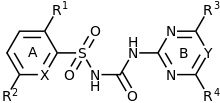
Y = N oder CH
Die Sulfonylharnstoffe (SU) sind eine der wichtigsten Herbizidgruppen. 2010 wurden über 30 % der deutschen Getreide-Anbauflächen mit ihnen behandelt.[8]
Die Einführung der Sulfonylharnstoffe führte zu einer Reduzierung der Aufwandmengen von vorher etwa 2000 g·ha−1 auf 3–60 g·ha−1. Dieses Niveau ist bis heute unübertroffen.[8]
Im Vergleich zu anderen Wirkstoffklassen der Herbizide (Wuchsstoffe, Triazine, ACCase-Hemmer) gibt es bei den Sulfonylharnstoffen eine große Variabilität in den Wirkungsspektren.[8]
Die Sulfonylharnstoffe sind schwach sauer. Abhängig vom pH-Wert liegen sie entweder als Anion oder neutral vor. Bei Zimmertemperatur sind sie kristalline Feststoffe mit extrem niedrigem Dampfdruck, weshalb sich trockene Formulierungen anbieten. Viele Sulfonylharnstoff-Herbizide sind als wasserdispergierbare Granulate (WG) formuliert.[8]
Aufgrund ihres hochspezifischen Wirkmechanismus als Hemmer der Acetolactat-Synthase sind die Sulfonylharnstoffe durch Punktmutationen des Zielenzyms resistenzgefährdet.[8]
| Name | Einsatzbereich: Selektivität für[9] |
Aufwandmenge in g·ha−1[9] | Hersteller |
|---|---|---|---|
| Amidosulfuron | Getreide | 30–60 | Bayer CropScience |
| Azimsulfuron | Reis | DuPont | |
| Bensulfuron-methyl | Reis | 20–75 | DuPont |
| Chlorimuron-ethyl | Sojabohnen | 8–13 | DuPont |
| Chlorsulfuron | Getreide | 9–25 | DuPont |
| Cinosulfuron | Reis | 20–40 | Syngenta |
| Cyclosulfamuron | |||
| Ethametsulfuron-methyl | Raps | 15–20 | DuPont |
| Ethoxysulfuron | |||
| Flazasulfuron | Obst, Wein, Nichtkulturland | 15–20 | Ishihara |
| Foramsulfuron | |||
| Flupyrsulfuron-methyl-Na | Getreide (spez. gegen Acker- Fuchsschwanz, Windhalm) |
||
| Halosulfuron-methyl | Mais, Grünland | 18–25 | Nissan |
| Imazosulfuron | Reis, Grünland | 50–100 | Takeda |
| Iodosulfuron | |||
| Mesosulfuron | Getreide (spez. gegen Acker-Fuchsschwanz) |
||
| Metsulfuron-methyl | Getreide, Reis Nichtkulturland |
3–8 14–168 |
DuPont |
| Nicosulfuron | Mais | 35–70 | DuPont / Ishihara |
| Oxasulfuron | |||
| Primisulfuron-methyl | Mais | 20–40 | Syngenta |
| Prosulfuron | Getreide, Mais | 20–40 | Syngenta |
| Pyrazosulfuron-ethyl | Reis | 15–30 | Nissan |
| Rimsulfuron | Kartoffeln, Mais | 5–25 | DuPont |
| Sulfometuron-methyl | Nichtkulturland, Forst | 26–420 | DuPont |
| Sulfosulfuron | Getreide (spez. gegen Trespe, Quecke, Windhalm)[10] |
Monsanto | |
| Thifensulfuron-methyl | Grünland | 2–30 | DuPont |
| Triasulfuron | Getreide | 10–30 | Syngenta |
| Tribenuron-methyl | Getreide | 9–18 | DuPont |
| Trifloxysulfuron-Natrium | |||
| Triflusulfuron-methyl | Rüben | 15–30 | DuPont |
Einzelnachweise
- S. Matthaei u. a.: Medikamentöse antihyperglykämische Therapie des Diabetes mellitus Typ 2. (PDF; 815 kB), In: Diabetologie. 4, 2009, S. 32–64.
- Onmeda: Sulfonylharnstoffe (Seite nicht mehr abrufbar, Suche in Webarchiven) Info: Der Link wurde automatisch als defekt markiert. Bitte prüfe den Link gemäß Anleitung und entferne dann diesen Hinweis.
- Richard K. Bernstein: Dr. Bernstein's Diabetes Solution. 1997, ISBN 0-316-09906-6, S. 225.
- Y. N. Chen, S. Y. Chen, L. J. Zeng, J. M. Ran, M. Y. Wu: Progressive decrease of proinsulin secretion in sulphonylurea-treated type 2 diabetes. In: Br J Biomed Sci. 62(1), 2005, S. 5–8. PMID 15816204.
- A. Takahashi, K. Nagashima, A. Hamasaki, N. Kuwamura, Y. Kawasaki, H. Ikeda, Y. Yamada, N. Inagaki, Y. Seino: Sulfonylurea and glinide reduce insulin content, functional expression of K(ATP) channels, and accelerate apoptotic beta-cell death in the chronic phase. In: Diabetes Res Clin Pract. 77(3), Sep 2007, S. 343–350. Epub 2007 Feb 20. PMID 17316868.
- Typ-2-Diabetes mellitus: Kardiale Risiken von Sulfonylharnstoffen. In: Deutsches Ärzteblatt. 4. Dezember 2009. Studie dazu: Ioanna Tzoulaki, Mariam Molokhia u. a.: Risk of cardiovascular disease and all cause mortality among patients with type 2 diabetes prescribed oral antidiabetes drugs: retrospective cohort study using UK general practice research database. In: BMJ. 339, 2009, S. b4731.
- Klaus Aktories (Hrsg.): Spezielle und allgemeine Pharmakologie und Toxikologie. 9. Auflage. Urban & Fischer, 2005, ISBN 3-437-42521-8.
- Hans G. Drobny, Martin Schulte, Harry J. Strek: 25 Jahre Sulfonylharnstoff-Herbizide – ein paar Gramm veränderten die Welt der chemischen Unkrautbekämpfung. In: Julius-Kühn-Archiv. Band 434, 2012, S. 21–33, doi:10.5073/jka.2012.434.002 (PDF).
- Modern Crop Protection Compounds. Chapter 2: Acetohydroxyacid Synthase Inhibitors (AHAS/ALS). doi:10.1002/9783527619580.ch2
- Gebrauchsanleitung Monitor (Memento des Originals vom 4. März 2016 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.