Schwefeltetrafluorid
Schwefeltetrafluorid ist eine chemische Verbindung aus der Gruppe der anorganischen Schwefelverbindungen und Fluoride.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
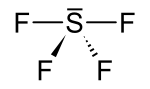 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Schwefeltetrafluorid | |||||||||||||||
| Andere Namen |
Schwefel(IV)-fluorid | |||||||||||||||
| Summenformel | SF4 | |||||||||||||||
| Kurzbeschreibung |
farbloses Gas mit stechendem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 108,05 g·mol−1 | |||||||||||||||
| Aggregatzustand |
gasförmig | |||||||||||||||
| Dichte |
1,919 g·cm−3 (flüssig bei −73 °C)[2] | |||||||||||||||
| Schmelzpunkt |
−121 °C[2] | |||||||||||||||
| Siedepunkt |
−40,4 °C[2] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
Zersetzt sich in Wasser mit heftiger Reaktion[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
Schweiz: 0,1 ml·m−3 bzw. 0,4 mg·m−3[3] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Geschichte
Schwefeltetrafluorid wurde 1929 von Joseph Fischer und Werner Jaenckner entdeckt. Die Darstellung gelang aus Cobalt(III)-fluorid und Schwefel, wobei der Reaktionsmischung zur Herabsetzung der Reaktivität Flussspat zugesetzt wurde. Das entstandene Schwefeltetrafluorid kondensierten sie in flüssiger Luft.[4]
Gewinnung und Darstellung
Schwefeltetrafluorid wird durch direkte Fluorierung von Schwefel mit Fluor in einem schmalen Temperaturbereich hergestellt.[1] Die Fluorierung kann auch bei −78 °C in Trichlorfluormethan erfolgen.[5]
Im Labor kann es auch durch Reaktion von Schwefeldichlorid mit Natriumfluorid (bzw. zusätzlich mit Chlor) hergestellt werden.[1]
oder nach einer neueren Reaktion aus Brom, Schwefel und Kaliumfluorid:
Eigenschaften
Schwefeltetrafluorid ist ein farbloses, nicht brennbares Gas mit stechendem Geruch. Es zersetzt sich in Wasser mit heftiger Reaktion sowie bei Erhitzung, wobei Fluorwasserstoff und Schwefeldioxid entstehen[6]. Es besitzt eine kritische Temperatur von 91 °C, der Tripelpunkt liegt bei einer Temperatur von −121 °C und einem Druck von 1,7 mbar.[2] Es wirkt als schwache Lewis-Säure und bildet zum Beispiel 1:1-Addukte mit organischen Basen wie Pyridin und Triethylamin.
Struktur
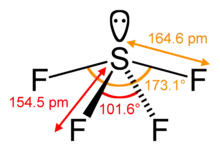
Schwefeltetrafluorid besitzt neben seinen Fluorsubstituenten ein nicht bindendes Elektronenpaar und bildet somit insgesamt eine – auf die axialen Positionen bezogene – verzerrte trigonale Bipyramide. Das freie Elektronenpaar besetzt hierbei eine der drei äquatorialen Position und zwei Fluorsubstituenten die beiden anderen. Im 19F-NMR-Spektrum wird bei Raumtemperatur jedoch nur ein einziges F-Signal beobachtet, da alle Fluoratome schnell ihre Plätze tauschen.[7]
Verwendung
Schwefeltetrafluorid wird als Fluorierungsmittel anorganischer Oxide, Sulfide oder Carbonyle[8] bzw. besonders der Ketogruppe >C=O zu >CF2 verwendet.[2]
Einzelnachweise
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 183–184.
- Eintrag zu Schwefeltetrafluorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 7783-60-0 bzw. Schwefeltetrafluorid), abgerufen am 2. November 2015.
- Joseph Fischer, Werner Jaenckner: Eine neue Fluor-Schwefelverbindung, das Schwefel-4-fluorid (vorläufige Mitteilung). In: Zeitschrift für Angewandte Chemie. Band 42, Nr. 31, 3. August 1929, S. 810–811, doi:10.1002/ange.19290423105.
- D. Naumann 1, Dr. (Mrs.) D. K. Padma: Die Darstellung von Schwefeltetrafluorid aus den Elementen bei tiefer Temperatur in einem inerten Lösungsmittel. In: Zeitschrift für anorganische und allgemeine Chemie. 1973, 401, 1, S. 53–56, doi:10.1002/zaac.19734010108.
- Greenwood, Norman N.; Earnshaw, Alan: Chemistry of the Elements. Band 2. Butterworth-Heinemann, 1997, ISBN 0-08-037941-9.
- M. Pavone, V. Barone, I. Ciofini, C. Adamo: First-principle molecular dynamics of the Berry pseudorotation: insights on 19F NMR in SF4. In: The Journal of chemical physics. Band 120, Nummer 19, Mai 2004, S. 9167–9174, doi:10.1063/1.1707012, PMID 15267853.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9, S. 564.


