Prostaglandin E2
Prostaglandin E2 gehört zu der Gruppe der Prostaglandine. Es wird durch die Prostaglandin-E-Synthase aus Prostaglandin H2 synthetisiert.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
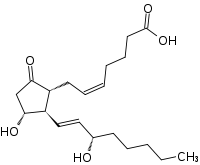 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Prostaglandin E2 | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C20H32O5 | |||||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
G02AD02 | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 352,47 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Wirkungen
Prostaglandin E2 bindet an vier Unterformen von G-Protein-gekoppelten Membranrezeptoren EP1 - EP4 und entfaltet darüber unterschiedliche Wirkungen.
Entzündung
PGE2 ist zusammen mit PGI2 das Hauptprostaglandin, welches in das Entzündungsgeschehen involviert ist. Es erhöht die Gefäßpermeabilität (Gewebeschwellung), ist an der Entstehung der Rötung beteiligt und verstärkt den Schmerz (welcher durch andere Entzündungsstoffe wie Bradykinin oder Histamin hervorgerufen wird), indem es nozizeptive Nervenendigungen sensibilisiert (indem es die Aktivierungsschwelle für Tetrodotoxin-resistente Natriumkanäle an sensiblen Nerven herabsetzt[3]).
Fieber
Fieber wird durch PGE2 mitverursacht, welches von Endothelzellen der Gefäße des Hypothalamus freigesetzt wird. Bakterielle Lipopolysaccharide und Interleukin-1β stimulieren die Cyclooxygenase-2 und die Prostaglandin-E-Synthase in den Endothelzellen, die die Blut-Hirn-Schranke bilden. Das PGE2 diffundiert in die Region des Organum vasculosum laminae terminalis (OLVT) des Hypothalamus, von wo die Fieberreaktion gesteuert wird. Dort wird durch das PGE2 der EP3-Rezeptor aktiviert.
Immunsystem
Zellen des Immunsystems wie Makrophagen und Monozyten, die durch Entzündungsmediatoren stimuliert werden, sezernieren große Mengen von PGE2 zusammen mit TXA2. Neutrophile bilden mäßige Mengen an PGE2. Lymphozyten und Mastzellen (diese bilden Prostaglandin D2) bilden kein PGE2.
Da PGE2 zu einer cAMP-Erhöhung führt, kann die Sekretion von PGE2 durch Makrophagen als negative Rückkoppelung dienen, um die Entzündungsaktivität zu begrenzen. PGE2 hemmt die Interleukin-2-Bildung und die Interferon-γ-Bildung durch T-Lymphozyten sowie die Interleukin-1β-Freisetzung und TNFα-Freisetzung aus Makrophagen. PGE2 steigert dagegen die Interleukin-6-Synthese.
Unreife Thymozyten werden durch PGE2 zur Reifung und Differenzierung angeregt.[3]
Verschiedene Tumorzellen bilden große Mengen an PGE2. Es wird vermutet, dass deshalb das Immunsystem bei Krebserkrankungen gehemmt sein kann.[3]
Magen
PGE2 wird durch die Schleimhautzellen und Zellen der glatten Muskulatur des Magens gebildet und schützt ihn, was vor allem durch eine Kombination aus drei Mechanismen bewirkt wird:
- PGE2 (über die EP3-Rezeptoren) reduziert (zusammen mit PGI2 über den Prostacyclin-Rezeptor) die Sekretion der Magensäure durch die Belegzellen des Magens.
- PGE2 (wie PGI2) steigert die Durchblutung der Magenschleimhaut.
- PGE2 (welches durch die Magenschleimhautzellen gebildet wird oder in den Magen gegeben wird) stimuliert (ebenfalls über die EP3-Rezeptoren) die Freisetzung von viskösem Schleim und neutralisierendem Bikarbonat, was die Magenschleimhaut vor ihrer eigenen Säure schützt.
Die Gefahr, Magengeschwüre zu bilden, steigt dann, wenn beide Cyclooxygenasen (COX-1 und COX-2) medikamentös gehemmt werden und so die Prostaglandinbildung im Magen stark eingeschränkt ist.[3]
PGE2 stimuliert ferner die EP1-Rezeptoren der glatten Muskelzellen des Magens und führt so zu deren Kontraktion.
Kardiovaskuläres System
- Im Gegensatz zu Prostacyclin kann PGE2 entweder eine Gefäßverengung oder Gefäßerweiterung auslösen: Was von dem Gefäß und der Art der Prostaglandin E-Rezeptoren abhängt, die in ihren glatten Muskelzellen exprimiert sind.
- PGE2 regt die Gefäßneubildung an, indem es den vaskulären endothelialen Wachstumsfaktor induziert. In welchem Rahmen und mit welcher Relevanz dies geschieht, ist noch unklar (Stand 2004[3]).
- Verschließt den Ductus arteriosus (über den EP4-Rezeptor) frühzeitig in der pränatalen Entwicklung und kann auch postnatal zur medikamentösen Therapie des persistierenden Ductus arteriosus botalli eingesetzt werden.
Nieren
PGE2 ist das Hauptprostaglandin (neben geringeren Mengen Prostacyclin und ganz kleinen Mengen TXA2), welches in der Nierenrinde gebildet wird. Das Nierenmark produziert aber noch bis zu 20-mal mehr PGE2 als die Nierenrinde. An der Urinausscheidung von PGE2 kann man die PGE2-Bildung in der Niere abschätzen.
- PGE2 und Prostacyclin haben in der Niere eine gefäßerweiternde und durchblutungssteigernde Funktion. Die Durchblutung der Nieren ist bei verschiedenen Grundkrankheiten (Herzinsuffizienz, Leberzirrhose, Niereninsuffizienz) abhängig von PGE2 und Prostacyclin. Daher besteht bei diesen Patienten das Risiko einer schwerwiegenden Nierendurchblutungsstörung, wenn die Prostaglandinsynthese durch NSAIDs gehemmt wird. Hierbei ist vor allem die Cyclooxygenase-1 maßgeblich, nur einige Zellen der Macula densa enthalten Cyclooxygenase-2.
- Sie hemmen die Rückresorption des Natriums in dem Nierentubulussystem.
- In den Epithelzellen des Glomerulums und im Mesangium werden ebenfalls (vor allem durch die Cyclooxygenase-2) PGE2 und Prostacyclin gebildet; dort stimulieren sie die Reninsekretion.
Lungen
PGE2 ist (wie Prostacyclin) ein schwacher Bronchodilatator (während Thromboxan, PGD2 und PGF2α starke Bronchokonstriktoren sind). Entzündungsmediatoren in den Lungen stimulieren vor allem die Cyclooxygenase-2, deren Stimulation vor allem zu einer Mehrbildung von PGE2 führt (zusammen mit kleineren Mengen von Prostacyclin, Thromboxan und PGF2α). Diese Prostaglandinbildung wird durch Dexamethason unterdrückt. Allerdings bleibt die Rolle der Prostaglandine bei Asthma für die praktische Medizin bisher unklar, da durch COX-2-Hemmer in der Praxis kein wesentlicher Effekt erreicht werden kann. Acetylsalicylsäure verschlechtert Asthma oft (durch eine vermehrte Bildung von Leukotrienen bei einer Hemmung der Cyclooxygenasen).
Zentralnervensystem
Im Rückenmark wirkt PGE2 schmerzverstärkend. Im Hypothalamus bewirkt es eine Steigerung der Körpertemperatur (u. a. Fieber) und Wachheit (und ist damit dort ein Gegenspieler zum PGD2).
Hemmung der Biosynthese
Das Flavonoid Taxifolin hemmt u. a. die Lipopolysaccharid-induzierte Bildung von Prostaglandin E.[5]
Handelsnamen
Minprostin E2 (D), Prepidil (D, A), Propess (D, A, CH), Prostin (A, CH)
Einzelnachweise
- Datenblatt Prostaglandin E2 bei Sigma-Aldrich, abgerufen am 18. Oktober 2016 (PDF).
- Datenblatt Prostaglandin E2 (PDF) bei Calbiochem, abgerufen am 8. Dezember 2015.
- D. Simmons u. a.: Cyclooxygenase Isoenzymes: The Biology of Prostaglandin Synthesis and Inhibition. In: Pharmacol Rev. 2004; 56, S. 387–437.
- S. M. Plaza, D. W. Lamson: Vitamin K2 in bone metabolism and osteoporosis. In: Alternative medicine review: a journal of clinical therapeutic. Band 10, Nummer 1, März 2005, S. 24–35, PMID 15771560 (Review).
- Y. Woo, S. Y. hin, J. Hyun u. a.: Flavanones inhibit the clonogenicity of HCT116 cololectal cancer cells. In: International journal of molecular medicine. 2012 Mar;29(3), S. 403–408, PMID 22160193.