Perfluoroctansulfonsäure
Perfluoroctansulfonsäure (Anion Perfluoroctansulfonat oder kurz PFOS) ist eine chemische Verbindung aus der Gruppe der per- und polyfluorierte Alkylverbindungen (PFAS). Üblicherweise wird bzw. wurde es im Handel als Kalium-[6], Lithium-[7], Ammonium-[8], Diethanolammonium-[9] oder Tetraethylammoniumsalz[10] angeboten. PFOS wurde 2009 als Schadstoff in den Anhang B des Stockholmer Übereinkommens aufgenommen.[11]
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
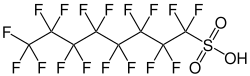 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Perfluoroctansulfonsäure | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel |
| |||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | ||||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Schmelzpunkt |
90 °C[1] | |||||||||||||||
| Siedepunkt |
258–260 °C[1] | |||||||||||||||
| Löslichkeit |
570 mg·l−1 (bei 24–25 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
Schweiz: 0,01 mg·m−3 (gemessen als einatembarer Staub)[5] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Geschichte
1953 entdeckte Patsy O’Connell Sherman bei 3M zufällig die Reinigungswirkung eines Fluorpolymeres. Zusammen mit Samuel Smith wurde bis 1956 Perfluoroctansulfonat zur Produktreife gebracht.[12][13]
Gewinnung und Darstellung
Die Darstellung von PFOS erfolgt durch die elektrochemische Fluorierung von Octansulfonylchlorid in wasserfreiem Hydrogenfluorid. Dabei entstehen drei Viertel lineares und ein Viertel verzweigtes Perfluoroctansulfonylfluorid.
Durch Hydrolyse von Perfluoroctansulfonylfluorid wird PFOS erhalten.[14][15]
Eigenschaften
Die Besonderheit von PFOS liegt darin, dass die perfluorierte Gruppe unpolar ist, die polare anionische Gruppe dagegen hydrophil. Es ist damit ein Tensid.
PFOS ist umweltpersistent, bioakkumulierbar und für Säugetiere giftig. Aus diesem Grund haben alle deutschen Chemieunternehmen die Produktion von PFOS im Jahr 2002 weltweit eingestellt[16] und viele Produkte auf die kürzerkettige Perfluorbutansulfonsäure (PFBS) umformuliert.
Verwendung
PFOS wurde hauptsächlich dazu verwendet, um Materialien wie Textilien, Teppiche und Papier fett-, öl- und wasserfest zu imprägnieren (3M Scotchgard). Daneben wurde und wird es bei der Verchromung, in der Analogfotografie, in älteren Feuerlöschschäumen (AFFF) und in Hydraulikflüssigkeiten für die Luft- und Raumfahrt verwendet.
In die Umwelt wird PFOS weiterhin emittiert. Die wichtigsten Quellen sind Metallverarbeitung (Verchromung) und Feuerlöschschäume.[17]
Als Ersatz von PFOS wird 6:2-FTS in Hart- und Dekorativverchromungsverfahren in der Galvanotechnik eingesetzt.[18][19][20] Bei Löschschäumen kommen 6:2-FTS und seine Derivate sowie fluorfreie Alternativen zum Einsatz.[21][22]
Nachweis
Der zuverlässige qualitative und quantitative Nachweis von PFOS in unterschiedlichen Untersuchungsmaterialien gelingt nach adäquater Probenvorbereitung durch die Kopplung der HPLC mit der Massenspektrometrie.[23][24]
Grenzwerte
Die EFSA hat die tolerierte Wochendosis (engl. tolerable weekly intake, TWI) im Dezember 2018 auf 13 ng pro kg Körpergewicht und Woche gesenkt. Es wurde festgestellt, dass die Exposition eines namhaften Anteils der Bevölkerung höher ist als dieser Wert.[25]
Laut Wasserrahmenrichtlinie betragen die Jahresdurchschnitts-Umweltqualitätsnormen 0,65 ng·l−1 für Binnenoberflächengewässer bzw. 0,13 ng·l−1 für sonstige Oberflächengewässer. Die Umweltqualitätsnorm für Biota (Fische) beträgt 9,1 μg·kg−1 Nassgewicht.[26]
Vorkommen in der Umwelt
Im Sommer 2006 wurden im Rhein und in der Ruhr hohe PFOS-Werte gemessen. Klärschlämme aus Belgien, die falsch deklariert waren, brachten die Stoffe nach Deutschland. Nachforschungen ergaben den Verdacht, dass Landwirte dafür bezahlt wurden, den belasteten Klärschlamm auf ihren Feldern auszubringen. Von dort gelangten Bestandteile in Grund- und Flusswasser.[27][28]
2012 wurden im Badesee Stoibermühle nördlich des Flughafens München sowie im Lindacher See nördlich des Fliegerhorstes Ingolstadt/Manching erhöhte Werte von verschiedenen perfluorierten Tensiden nachgewiesen, darunter auch PFOS (1 µg/l, Grenzwert: 0,3 µg/l).[29]
2015 wurden im Badesee Birkensee östlich von Nürnberg erhöhte Werte von verschiedenen PFAS nachgewiesen (3 µg/l), darunter auch PFOS. Zeitweilig wurde ein Badeverbot erlassen.[30]
Das US-Verteidigungsministerium gab im November 2019 bekannt, dass es über die 401 bislang benannten inzwischen weitere Standorte identifiziert habe, die mit PFOS bzw. PFOA kontaminiert seien.[31]
Auch Muttermilch aus allen Kontinenten enthält PFOS.[32]
Fische
Bei Fischen aus der Moosach warnte die Behörde 2019 vor dem häufigen Verzehr.[33]
Das Niedersächsische Verbraucherschutzministerium riet im April 2020 in einer Verzehrempfehlung auf den regelmäßigen Verzehr von niedersächsischen Flussfischen zu verzichten. Bei einer Untersuchung von Fischproben betrug der Median der PFOS-Konzentrationen im Muskelgewebe der Fische 7,8 μg/kg.[34]
In Fischfilets aus zehn Seen südlich und westlich der Alpen lagen die PFOS-Konzentrationen im Bereich von 0,2–50 μg/kg, während die Konzentrationen in den Innereien und den übrigen Körperteilen etwas höher waren.[35]
Verbot
Das Europäische Parlament hat im Oktober 2006 beschlossen, die Verwendung von PFOS auf wenige Einsatzbereiche einzuschränken. Die „Richtlinie 2006/122/EG des Europäischen Parlaments und des Rates“ ist am 27. Dezember 2006 durch Veröffentlichung im Amtsblatt der Europäischen Union (2006 / L 372) in Kraft getreten.[36]
In der 4. Vertragsparteienkonferenz des Stockholmer Übereinkommens (Genf, 4. bis 8. Mai 2009) wurde entschieden, PFOS in den Anhang B der unter dieser Konvention eingeschränkten Stoffe aufzunehmen.[37]
Siehe auch
- Perfluoroctansäure (PFOA)
- F-53
- F-53B
Weblinks
- Fragen und Antworten zu perfluorierten und polyfluorierten Alkylsubstanzen (PFAS) vom Bundesinstitut für Risikobewertung (BfR)
- Perfluorierte Tenside – ein globales Umweltproblem – Artikel vom 27. September 2006 in der NZZ
- PFOS Risk Assessment (englisch; PDF-Datei; 924 kB)
- Perfluoroctansulfonate Fachinformationen des Bundesamts für Umwelt
Einzelnachweise
- Dictionary of Organic Compounds. CRC Press, 1996, ISBN 978-0-412-54090-5, S. 3397 (books.google.com).
- OECD (Hrsg.): Hazard Assessment of Perfluorooctane Sulfonate (PFOS) and its Salts. 2002, ENV/JM/RD(2002)17/FINAL, S. 11 (oecd.org [PDF]).
- Eintrag zu Perfluoroctansulfonsäure im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 9. Juni 2017. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag zu Perfluoroctansulfonsäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. November 2021. (JavaScript erforderlich)
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte, abgerufen am 2. November 2015.
- Externe Identifikatoren von bzw. Datenbank-Links zu Kaliumperfluoroctansulfonat: CAS-Nummer: 2795-39-3, EG-Nummer: 220-527-1, ECHA-InfoCard: 100.018.661, GESTIS-Stoffdatenbank: 113462, PubChem: 23669238, ChemSpider: 68535, Wikidata: Q27276914.
- Externe Identifikatoren von bzw. Datenbank-Links zu Lithiumperfluoroctansulfonat: CAS-Nummer: 29457-72-5, EG-Nummer: 249-644-6, ECHA-InfoCard: 100.045.117, GESTIS-Stoffdatenbank: 137396, PubChem: 23677927, ChemSpider: 118370, Wikidata: Q27251563.
- Externe Identifikatoren von bzw. Datenbank-Links zu Ammoniumperfluoroctansulfonat: CAS-Nummer: 29081-56-9, EG-Nummer: 249-415-0, ECHA-InfoCard: 100.044.908, GESTIS-Stoffdatenbank: 137199, PubChem: 15607692, ChemSpider: 107238, Wikidata: Q72443080.
- Externe Identifikatoren von bzw. Datenbank-Links zu Diethanolammoniumperfluoroctansulfonat: CAS-Nummer: 70225-14-8, EG-Nummer: 274-460-8, ECHA-InfoCard: 100.067.670, GESTIS-Stoffdatenbank: 159177, PubChem: 112394, ChemSpider: 100740, Wikidata: Q81985372.
- Externe Identifikatoren von bzw. Datenbank-Links zu Tetraethylammoniumperfluoroctansulfonat: CAS-Nummer: 56773-42-3, EG-Nummer: 260-375-3, ECHA-InfoCard: 100.054.869, GESTIS-Stoffdatenbank: 146734, PubChem: 92531, ChemSpider: 83538, Wikidata: Q72481197.
- Press Release - COP4 - Geneva, 8 May 2009: Governments unite to step-up reduction on global DDT reliance and add nine new chemicals under international treaty
- Fascinating facts about the invention of Scotchgard™ by Patsy Sherman and Sam Smith in 1956.
- Patent US2732398: Fluorocarbon sulfonic acids and derivatives. Angemeldet am 9. August 1954, veröffentlicht am 24. Januar 1956, Anmelder: Minnesota Mining & Manufacturing, Erfinder: Thomas J. Brice, Paul W. Trott (Zitat: “The n-perfluorooctane compounds, which have a normal chain of eight perfluorinated carbon atoms, CF3(CF2)7−, are of particular noteworthy value as surface active agents and as starting compounds for making surface active compounds.”).
- Robert C Buck, James Franklin, Urs Berger, Jason M Conder, Ian T Cousins: Perfluoroalkyl and Polyfluoroalkyl Substances in the Environment: Terminology, Classification, and Origins. In: Integrated Environmental Assessment and Management. Band 7, Nr. 4, Oktober 2011, ISSN 1551-3777, S. 513–541, doi:10.1002/ieam.258, PMID 21793199, PMC 3214619 (freier Volltext).
- Hans-Joachim Lehmler: Synthesis of environmentally relevant fluorinated surfactants—a review. In: Chemosphere. Band 58, Nr. 11, 1. März 2005, ISSN 0045-6535, S. 1471–1496, doi:10.1016/j.chemosphere.2004.11.078.
- Presseinformation des VCI vom 6. Oktober 2005: Daten und Fakten zur Stoffliste des WWF-Bluttests (PDF; 33 kB)
- Substance flow analysis for Switzerland – Perfluorinated surfactants perfluorooctanesulfonate (PFOS) and perfluorooctanoic acid (PFOA). Federal Office for the Environment, 2009.
- H. Hauser, L. Füglister, T. Scheffelmaier: Verwendung von Fluortensiden in der Galvanikbranche, 2020.
- Wolfram Willand, Yifaat Baron, Markus Blepp, Roland Weber, Christine Herold: Beste verfügbare Techniken für die PFOS-Substitution in der Oberflächenbehandlung von Metallen und Kunststoffen sowie Analyse der alternativen Substanzen zu PFOS beim Einsatz in Anlagen zur Verchromung und Kunststoffbeize. Umweltbundesamt, November 2020 (umweltbundesamt.de).
- Xiaoling Yang, Jun Huang, Kunlun Zhang, Gang Yu, Shubo Deng: Stability of 6:2 fluorotelomer sulfonate in advanced oxidation processes: degradation kinetics and pathway. In: Environmental Science and Pollution Research. Band 21, Nr. 6, März 2014, S. 4634–4642, doi:10.1007/s11356-013-2389-z.
- laenderfinanzierungsprogramm.de: 01_Anhang_A_Grundlagen PFC-Arbeitshilfe (Memento vom 23. September 2016 im Internet Archive), abgerufen am 23. September 2016.
- The use of PFAS and fluorine-free alternatives in fire-fighting foams. 2020 (europa.eu [PDF]).
- F. Pérez, M. Llorca, M. Köck-Schulmeyer, B. Skrbić, L. S. Oliveira, K. da Boit Martinello, N. A. Al-Dhabi, I. Antić, M. Farré, D. Barceló: Assessment of perfluoroalkyl substances in food items at global scale. In: Environ Res. 135C, 1 Okt 2014, S. 181–189. PMID 25282275
- Z. Lu, L. Song, Z. Zhao, Y. Ma, J. Wang, H. Yang, H. Ma, M. Cai, G. Codling, R. Ebinghaus, Z. Xie, J. P. Giesy: Occurrence and trends in concentrations of perfluoroalkyl substances (PFASs) in surface waters of eastern China. In: Chemosphere. 119C, 11 Sep 2014, S. 820–827. PMID 25218980
- EFSA Panel on Contaminants in the Food Chain (CONTAM), Helle Katrine Knutsen, Jan Alexander, Lars Barregårdet al.: Risk to human health related to the presence of perfluorooctane sulfonic acid and perfluorooctanoic acid in food. In: EFSA Journal. Band 16, Nr. 12, Dezember 2018, doi:10.2903/j.efsa.2018.5194.
- Richtlinie 2013/39/EU des Europäischen Parlaments und des Rates vom 12. August 2013 zur Änderung der Richtlinien 2000/60/EG und 2008/105/EG in Bezug auf prioritäre Stoffe im Bereich der Wasserpolitik
- Fall von Umwelt-Kriminalität – Trinkwasser mit Chemikalie PFT belastet (Memento vom 28. November 2006 im Internet Archive). In: WDR. 2006.
- ES&T Science News: Perfluorinated surfactants contaminate German waters. 2006. doi:10.1021/es062811u.
- Ist Löschschaum vom Flughafen der Grund? Chemie-Alarm im Stoibermühlsee. tz, 25. Juli 2012
- PFT im Birkensee: Badeverbot bleibt weiter bestehen. (Memento vom 29. November 2015 im Internet Archive) BR, 28. August 2015
- The list of military sites with suspected ‘forever chemicals’ contamination has grown
- Heidelore Fiedler, Mohammad Sadia: Regional occurrence of perfluoroalkane substances in human milk for the global monitoring plan under the Stockholm Convention on Persistent Organic Pollutants during 2016–2019. In: Chemosphere. Band 277, August 2021, S. 130287, doi:10.1016/j.chemosphere.2021.130287.
- Birgit Grundner, Rüdiger Kronthaler: PFOS-belastete Fische in der Moosach: Warnung vor Verzehr. In: br.de. 8. August 2019, abgerufen am 23. September 2019.
- Aktualisierung der Verzehrempfehlung für Fische | Nds. Ministerium für Ernährung, Landwirtschaft und Verbraucherschutz. Abgerufen am 18. April 2020.
- Sara Valsecchi, Marc Babut, Michela Mazzoni, Simona Pascariello, Claudia Ferrario: Per‐ and Polyfluoroalkyl Substances (PFAS) in Fish from European Lakes: Current Contamination Status, Sources, and Perspectives for Monitoring. In: Environmental Toxicology and Chemistry. Band 40, Nr. 3, 2021, S. 658–676, doi:10.1002/etc.4815.
- Amtsblatt der Europäischen Union: RICHTLINIE 2006/122/EG DES EUROPÄISCHEN PARLAMENTS UND DES RATES vom 12. Dezember 2006 zur dreißigsten Änderung der Richtlinie 76/769/EWG des Rates zur Angleichung der Rechts- und Verwaltungsvorschriften der Mitgliedstaaten für Beschränkungen des Inverkehrbringens und der Verwendung gewisser gefährlicher Stoffe und Zubereitungen (Perfluoroctansulfonate) (PDF). 27. Dezember 2006 / L 372.
- Governments unite to step-up reduction on global DDT reliance and add nine new chemicals under international treaty, Pressecommuniqué, 8. Mai 2009.



